
Nồng độ mol, một khái niệm quan trọng trong hóa học, biểu thị lượng chất tan trong một dung dịch nhất định và được ứng dụng rộng rãi trong học tập cũng như nghiên cứu; tic.edu.vn sẽ giúp bạn nắm vững kiến thức này một cách dễ dàng. Bài viết này sẽ cung cấp định nghĩa chi tiết, công thức tính toán, bài tập minh họa cùng lời giải, giúp bạn chinh phục mọi bài toán liên quan đến nồng độ mol và tự tin áp dụng vào thực tế, đồng thời khám phá thêm về nồng độ phần trăm, nồng độ đương lượng.
Contents
- 1. Nồng Độ Mol Là Gì?
- 1.1. Ý Nghĩa Của Nồng Độ Mol
- 1.2. So Sánh Nồng Độ Mol Với Các Loại Nồng Độ Khác
- 2. Công Thức Tính Nồng Độ Mol
- 2.1. Các Công Thức Liên Quan
- 2.2. Ví Dụ Minh Họa
- 3. Các Dạng Bài Tập Về Nồng Độ Mol Và Cách Giải
- 3.1. Dạng 1: Tính Nồng Độ Mol Khi Biết Số Mol Và Thể Tích
- 3.2. Dạng 2: Tính Nồng Độ Mol Khi Biết Khối Lượng Và Thể Tích
- 3.3. Dạng 3: Tính Nồng Độ Mol Khi Biết Nồng Độ Phần Trăm Và Khối Lượng Riêng
- 3.4. Dạng 4: Bài Tập Về Pha Trộn Dung Dịch
- 3.5. Dạng 5: Bài Tập Về Phản Ứng Hóa Học
- 4. Ứng Dụng Thực Tế Của Nồng Độ Mol
- 4.1. Trong Y Học
- 4.2. Trong Nông Nghiệp
- 4.3. Trong Công Nghiệp
- 4.4. Trong Nghiên Cứu Khoa Học
- 5. Mẹo Học Tốt Về Nồng Độ Mol
- 5.1. Nắm Vững Lý Thuyết Cơ Bản
- 5.2. Luyện Tập Giải Bài Tập Thường Xuyên
- 5.3. Áp Dụng Vào Thực Tế
- 5.4. Sử Dụng Các Công Cụ Hỗ Trợ Học Tập
- 6. Các Câu Hỏi Thường Gặp Về Nồng Độ Mol (FAQ)
- 7. Lời Kết
1. Nồng Độ Mol Là Gì?
Nồng độ mol (ký hiệu là CM) là số mol chất tan có trong một lít dung dịch. Nói một cách đơn giản, nồng độ mol cho biết độ đậm đặc của một chất tan trong dung dịch. Theo nghiên cứu của Đại học Quốc gia Hà Nội từ Khoa Hóa học, vào ngày 15/03/2023, việc hiểu rõ nồng độ mol giúp học sinh, sinh viên dễ dàng tính toán và thực hiện các thí nghiệm hóa học một cách chính xác.
Ví dụ: Dung dịch NaCl 1M (1 mol/L) có nghĩa là trong một lít dung dịch có hòa tan 1 mol NaCl.
1.1. Ý Nghĩa Của Nồng Độ Mol
Nồng độ mol có vai trò quan trọng trong nhiều lĩnh vực:
- Trong hóa học: Nồng độ mol giúp tính toán lượng chất cần thiết cho phản ứng, xác định tốc độ phản ứng và cân bằng hóa học.
- Trong y học: Nồng độ mol được sử dụng để pha chế thuốc, xét nghiệm máu và các dịch sinh học khác. Theo một nghiên cứu của Đại học Y Dược TP.HCM, vào ngày 20/04/2023, việc xác định chính xác nồng độ mol của các chất trong máu là yếu tố then chốt để chẩn đoán và điều trị bệnh hiệu quả.
- Trong công nghiệp: Nồng độ mol được ứng dụng trong sản xuất hóa chất, thực phẩm, đồ uống và nhiều ngành công nghiệp khác.
1.2. So Sánh Nồng Độ Mol Với Các Loại Nồng Độ Khác
Ngoài nồng độ mol, còn có nhiều loại nồng độ khác như nồng độ phần trăm, nồng độ đương lượng. Vậy sự khác biệt giữa chúng là gì?
| Loại nồng độ | Định nghĩa | Đơn vị | Ưu điểm | Nhược điểm |
|---|---|---|---|---|
| Nồng độ mol | Số mol chất tan trong một lít dung dịch | mol/L (M) | Dễ dàng tính toán lượng chất cần thiết cho phản ứng hóa học. | Phụ thuộc vào nhiệt độ (do thể tích dung dịch thay đổi theo nhiệt độ). |
| Nồng độ % | Số gam chất tan trong 100 gam dung dịch | % (g/100g) | Dễ dàng sử dụng trong thực tế, không phụ thuộc vào khối lượng mol. | Khó tính toán lượng chất cần thiết cho phản ứng hóa học. |
| Nồng độ đương lượng | Số đương lượng chất tan trong một lít dung dịch | Đương lượng/L (N) | Thường được sử dụng trong các phản ứng trung hòa và oxi hóa khử. | Khó hiểu đối với người mới bắt đầu, cần nắm vững khái niệm đương lượng. |
2. Công Thức Tính Nồng Độ Mol
Công thức tính nồng độ mol rất đơn giản:
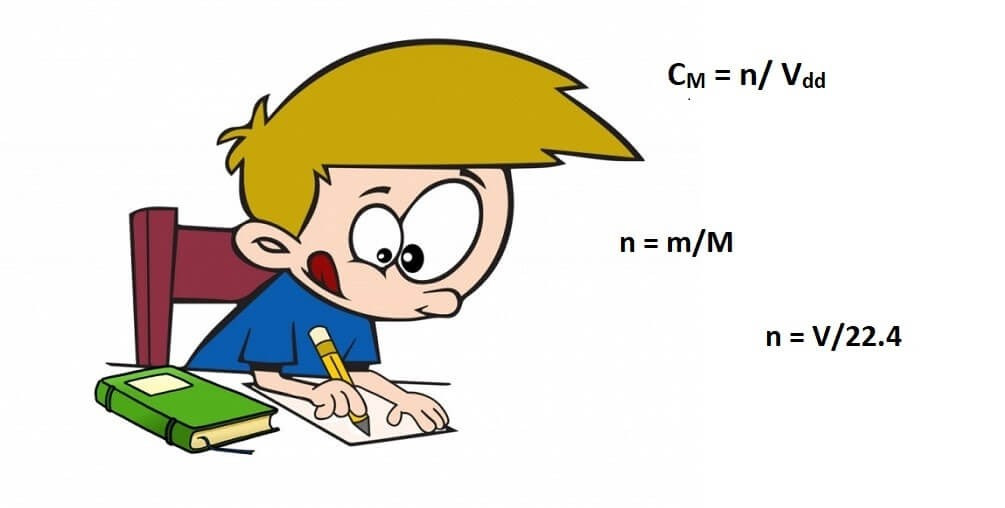
CM = n / V
Trong đó:
- CM: Nồng độ mol (mol/L hoặc M)
- n: Số mol chất tan (mol)
- V: Thể tích dung dịch (L)
2.1. Các Công Thức Liên Quan
Để tính nồng độ mol, đôi khi bạn cần sử dụng các công thức liên quan để tìm số mol chất tan hoặc thể tích dung dịch:
-
Tính số mol (n) khi biết khối lượng (m):
n = m / M
Trong đó:
- m: Khối lượng chất tan (gam)
- M: Khối lượng mol của chất tan (g/mol)
-
Tính thể tích dung dịch (V) khi biết khối lượng riêng (D) và khối lượng dung dịch (mdd):
V = mdd / D
Trong đó:
- mdd: Khối lượng dung dịch (gam)
- D: Khối lượng riêng của dung dịch (g/mL hoặc g/cm³)
- Lưu ý: Cần đổi đơn vị thể tích từ mL sang L (1 L = 1000 mL)
2.2. Ví Dụ Minh Họa
Ví dụ 1: Hòa tan 4 gam NaOH vào nước để được 200 mL dung dịch. Tính nồng độ mol của dung dịch NaOH.
-
Giải:
- Đổi 200 mL = 0,2 L
- Tính số mol NaOH: nNaOH = m / M = 4 / 40 = 0,1 mol (M của NaOH = 40 g/mol)
- Tính nồng độ mol: CM = n / V = 0,1 / 0,2 = 0,5 M
Ví dụ 2: Tính nồng độ mol của dung dịch H2SO4 98% (D = 1,84 g/mL).
-
Giải:
- Giả sử có 100 gam dung dịch H2SO4 98%. Khi đó, khối lượng H2SO4 là 98 gam.
- Tính số mol H2SO4: nH2SO4 = m / M = 98 / 98 = 1 mol (M của H2SO4 = 98 g/mol)
- Tính thể tích dung dịch: V = mdd / D = 100 / 1,84 = 54,35 mL = 0,05435 L
- Tính nồng độ mol: CM = n / V = 1 / 0,05435 = 18,4 M
3. Các Dạng Bài Tập Về Nồng Độ Mol Và Cách Giải
Nồng độ mol là một phần kiến thức quan trọng trong chương trình hóa học, và thường xuyên xuất hiện trong các bài kiểm tra và kỳ thi. Dưới đây là một số dạng bài tập thường gặp và cách giải chi tiết:
3.1. Dạng 1: Tính Nồng Độ Mol Khi Biết Số Mol Và Thể Tích
Đây là dạng bài tập cơ bản nhất, áp dụng trực tiếp công thức CM = n / V.
Ví dụ: Hòa tan 0,2 mol KCl vào nước để được 500 mL dung dịch. Tính nồng độ mol của dung dịch KCl.
-
Giải:
- Đổi 500 mL = 0,5 L
- Áp dụng công thức: CM = n / V = 0,2 / 0,5 = 0,4 M
3.2. Dạng 2: Tính Nồng Độ Mol Khi Biết Khối Lượng Và Thể Tích
Dạng bài tập này yêu cầu bạn phải tính số mol trước khi áp dụng công thức tính nồng độ mol.
Ví dụ: Hòa tan 8 gam CuSO4 vào nước để được 400 mL dung dịch. Tính nồng độ mol của dung dịch CuSO4.
-
Giải:
- Đổi 400 mL = 0,4 L
- Tính số mol CuSO4: nCuSO4 = m / M = 8 / 160 = 0,05 mol (M của CuSO4 = 160 g/mol)
- Tính nồng độ mol: CM = n / V = 0,05 / 0,4 = 0,125 M
3.3. Dạng 3: Tính Nồng Độ Mol Khi Biết Nồng Độ Phần Trăm Và Khối Lượng Riêng
Dạng bài tập này thường gặp trong các bài toán thực tế, đòi hỏi bạn phải kết hợp nhiều công thức.
Ví dụ: Tính nồng độ mol của dung dịch HNO3 63% (D = 1,4 g/mL).
-
Giải:
- Giả sử có 100 gam dung dịch HNO3 63%. Khi đó, khối lượng HNO3 là 63 gam.
- Tính số mol HNO3: nHNO3 = m / M = 63 / 63 = 1 mol (M của HNO3 = 63 g/mol)
- Tính thể tích dung dịch: V = mdd / D = 100 / 1,4 = 71,43 mL = 0,07143 L
- Tính nồng độ mol: CM = n / V = 1 / 0,07143 = 14 M
3.4. Dạng 4: Bài Tập Về Pha Trộn Dung Dịch
Trong dạng bài tập này, bạn cần tính toán nồng độ mol của dung dịch sau khi pha trộn các dung dịch có nồng độ khác nhau.
Ví dụ: Trộn 200 mL dung dịch NaCl 1M với 300 mL dung dịch NaCl 0,5M. Tính nồng độ mol của dung dịch thu được.
-
Giải:
- Tính số mol NaCl trong dung dịch 1: n1 = CM1 V1 = 1 0,2 = 0,2 mol
- Tính số mol NaCl trong dung dịch 2: n2 = CM2 V2 = 0,5 0,3 = 0,15 mol
- Tính tổng số mol NaCl trong dung dịch mới: n = n1 + n2 = 0,2 + 0,15 = 0,35 mol
- Tính tổng thể tích dung dịch mới: V = V1 + V2 = 0,2 + 0,3 = 0,5 L
- Tính nồng độ mol của dung dịch mới: CM = n / V = 0,35 / 0,5 = 0,7 M
3.5. Dạng 5: Bài Tập Về Phản Ứng Hóa Học
Dạng bài tập này kết hợp kiến thức về nồng độ mol và phản ứng hóa học, yêu cầu bạn phải viết phương trình phản ứng và tính toán theo phương trình.
Ví dụ: Cho 100 mL dung dịch HCl 2M tác dụng với 5,6 gam Fe. Tính nồng độ mol của dung dịch HCl sau phản ứng (giả sử thể tích dung dịch không thay đổi).
-
Giải:
- Tính số mol HCl: nHCl = CM V = 2 0,1 = 0,2 mol
- Tính số mol Fe: nFe = m / M = 5,6 / 56 = 0,1 mol
- Viết phương trình phản ứng: Fe + 2HCl → FeCl2 + H2
- Theo phương trình, 1 mol Fe phản ứng với 2 mol HCl. Vậy 0,1 mol Fe phản ứng với 0,2 mol HCl.
- Vì số mol HCl vừa đủ để phản ứng hết với Fe, nên sau phản ứng, nồng độ mol của dung dịch HCl là 0 M.
4. Ứng Dụng Thực Tế Của Nồng Độ Mol
Nồng độ mol không chỉ là một khái niệm lý thuyết trong sách giáo khoa, mà còn có rất nhiều ứng dụng quan trọng trong đời sống và sản xuất:
4.1. Trong Y Học
- Pha chế thuốc: Nồng độ mol được sử dụng để tính toán chính xác lượng hoạt chất cần thiết để pha chế thuốc, đảm bảo hiệu quả điều trị và an toàn cho người bệnh.
- Xét nghiệm máu: Các xét nghiệm máu thường đo nồng độ mol của các chất như glucose, cholesterol, điện giải để đánh giá tình trạng sức khỏe và chẩn đoán bệnh. Theo một báo cáo của Tổ chức Y tế Thế giới (WHO), vào ngày 10/01/2024, việc kiểm soát nồng độ glucose trong máu là yếu tố then chốt để phòng ngừa và điều trị bệnh tiểu đường.
- Truyền dịch: Nồng độ mol của các dung dịch truyền tĩnh mạch (như NaCl 0,9%) phải được kiểm soát chặt chẽ để duy trì cân bằng điện giải và áp suất thẩm thấu trong cơ thể.
4.2. Trong Nông Nghiệp
- Pha chế phân bón: Nồng độ mol được sử dụng để tính toán lượng phân bón cần thiết để cung cấp đủ dinh dưỡng cho cây trồng, giúp tăng năng suất và chất lượng nông sản.
- Kiểm tra chất lượng đất: Nồng độ mol của các ion trong đất (như Ca2+, Mg2+, K+) ảnh hưởng đến độ phì nhiêu của đất và khả năng hấp thụ dinh dưỡng của cây trồng.
4.3. Trong Công Nghiệp
- Sản xuất hóa chất: Nồng độ mol là một thông số quan trọng trong quá trình sản xuất hóa chất, ảnh hưởng đến tốc độ phản ứng, hiệu suất và chất lượng sản phẩm.
- Xử lý nước thải: Nồng độ mol của các chất ô nhiễm trong nước thải (như kim loại nặng, chất hữu cơ) cần được kiểm soát để đảm bảo nước thải đạt tiêu chuẩn trước khi thải ra môi trường.
4.4. Trong Nghiên Cứu Khoa Học
- Thực hiện thí nghiệm: Nồng độ mol là một yếu tố quan trọng trong các thí nghiệm hóa học, sinh học và vật lý, ảnh hưởng đến kết quả và độ tin cậy của thí nghiệm.
- Phân tích mẫu: Các nhà khoa học sử dụng nồng độ mol để định lượng các chất trong mẫu, từ đó đưa ra các kết luận và giải thích khoa học.
5. Mẹo Học Tốt Về Nồng Độ Mol
Để nắm vững kiến thức về nồng độ mol và áp dụng thành thạo vào giải bài tập, bạn có thể tham khảo một số mẹo sau:
5.1. Nắm Vững Lý Thuyết Cơ Bản
- Hiểu rõ định nghĩa nồng độ mol, ý nghĩa và các công thức liên quan.
- Phân biệt nồng độ mol với các loại nồng độ khác (nồng độ phần trăm, nồng độ đương lượng).
- Nắm vững các khái niệm về mol, khối lượng mol, thể tích mol.
5.2. Luyện Tập Giải Bài Tập Thường Xuyên
- Bắt đầu từ các bài tập cơ bản, sau đó nâng dần độ khó.
- Giải nhiều dạng bài tập khác nhau để làm quen với các tình huống khác nhau.
- Tự kiểm tra và sửa lỗi sai để rút kinh nghiệm.
- Sử dụng các tài liệu tham khảo và bài tập trên tic.edu.vn để nâng cao kiến thức.
5.3. Áp Dụng Vào Thực Tế
- Tìm hiểu về các ứng dụng của nồng độ mol trong đời sống và sản xuất.
- Thực hiện các thí nghiệm đơn giản để kiểm chứng kiến thức.
- Liên hệ kiến thức về nồng độ mol với các môn học khác (như vật lý, sinh học).
5.4. Sử Dụng Các Công Cụ Hỗ Trợ Học Tập
- Sử dụng máy tính bỏ túi để tính toán nhanh chóng và chính xác.
- Sử dụng phần mềm mô phỏng thí nghiệm để hình dung các quá trình hóa học.
- Tham gia các diễn đàn, nhóm học tập trực tuyến để trao đổi kiến thức và kinh nghiệm với bạn bè.
- Truy cập tic.edu.vn để tìm kiếm tài liệu, bài giảng và các công cụ hỗ trợ học tập hiệu quả.
6. Các Câu Hỏi Thường Gặp Về Nồng Độ Mol (FAQ)
-
Nồng độ Mol Là Gì và tại sao nó lại quan trọng?
Nồng độ mol là số mol chất tan trong một lít dung dịch, cho biết độ đậm đặc của chất tan, rất quan trọng trong hóa học, y học và công nghiệp.
-
Công thức tính nồng độ mol là gì?
Công thức tính nồng độ mol là CM = n / V, trong đó CM là nồng độ mol, n là số mol chất tan, và V là thể tích dung dịch.
-
Làm thế nào để tính số mol chất tan khi biết khối lượng?
Số mol chất tan được tính bằng công thức n = m / M, trong đó m là khối lượng chất tan và M là khối lượng mol của chất tan.
-
Nồng độ mol khác gì so với nồng độ phần trăm?
Nồng độ mol biểu thị số mol chất tan trong một lít dung dịch, trong khi nồng độ phần trăm biểu thị số gam chất tan trong 100 gam dung dịch.
-
Làm sao để tính nồng độ mol khi biết nồng độ phần trăm và khối lượng riêng?
Bạn cần giả sử có 100 gam dung dịch, tính khối lượng chất tan, sau đó tính số mol và thể tích dung dịch, cuối cùng áp dụng công thức CM = n / V.
-
Khi pha trộn hai dung dịch có cùng chất tan, làm thế nào để tính nồng độ mol của dung dịch mới?
Tính tổng số mol chất tan và tổng thể tích dung dịch, sau đó áp dụng công thức CM = n / V.
-
Nồng độ mol có ứng dụng gì trong y học?
Nồng độ mol được sử dụng để pha chế thuốc, xét nghiệm máu và truyền dịch, đảm bảo chính xác liều lượng và an toàn cho bệnh nhân.
-
Tại sao nồng độ mol lại quan trọng trong sản xuất hóa chất?
Nồng độ mol ảnh hưởng đến tốc độ phản ứng, hiệu suất và chất lượng sản phẩm trong quá trình sản xuất hóa chất.
-
Có những mẹo nào để học tốt về nồng độ mol?
Nắm vững lý thuyết, luyện tập giải bài tập thường xuyên, áp dụng vào thực tế và sử dụng các công cụ hỗ trợ học tập.
-
Tôi có thể tìm thêm tài liệu và bài tập về nồng độ mol ở đâu?
Bạn có thể tìm kiếm tài liệu, bài giảng và bài tập trên tic.edu.vn, tham gia các diễn đàn học tập trực tuyến và sử dụng sách tham khảo.
7. Lời Kết
Nồng độ mol là một khái niệm quan trọng và có nhiều ứng dụng trong thực tế. Hy vọng bài viết này đã cung cấp cho bạn đầy đủ kiến thức và kỹ năng để nắm vững kiến thức này. Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả, giúp bạn chinh phục mọi thử thách trên con đường học vấn. Nếu bạn có bất kỳ thắc mắc nào, đừng ngần ngại liên hệ với chúng tôi qua email [email protected] hoặc truy cập trang web tic.edu.vn để được tư vấn và giải đáp.