Liên Kết Phân Cực đóng vai trò then chốt trong hóa học, ảnh hưởng đến tính chất và hoạt động của vô số hợp chất. Hãy cùng tic.edu.vn khám phá sâu hơn về loại liên kết đặc biệt này, từ định nghĩa cơ bản đến những ứng dụng thực tiễn và lợi ích mà nó mang lại.
Liên kết phân cực, hay còn gọi là liên kết cộng hóa trị phân cực, là một loại liên kết hóa học, nơi các electron dùng chung không được chia sẻ đều giữa các nguyên tử tham gia. Sự khác biệt về độ âm điện giữa các nguyên tử tạo ra sự phân bố điện tích không đồng đều, dẫn đến một đầu mang điện tích âm một phần (δ-) và đầu kia mang điện tích dương một phần (δ+). Để hiểu rõ hơn về bản chất và vai trò của liên kết phân cực trong hóa học, hãy cùng tic.edu.vn khám phá chi tiết về định nghĩa, các yếu tố ảnh hưởng, các loại liên kết phân cực phổ biến, tính chất đặc trưng, cũng như sự khác biệt giữa liên kết phân cực và các loại liên kết hóa học khác. Thông qua bài viết này, bạn sẽ có cái nhìn toàn diện và sâu sắc về liên kết phân cực, từ đó áp dụng kiến thức vào việc giải thích các hiện tượng hóa học và ứng dụng trong thực tế.
Contents
- 1. Liên Kết Phân Cực Là Gì?
- 1.1. Giải Thích Cặn Kẽ Về Liên Kết Phân Cực
- 1.2. Các Yếu Tố Ảnh Hưởng Đến Liên Kết Phân Cực
- 1.3. Tại Sao Liên Kết Phân Cực Lại Quan Trọng?
- 2. Các Loại Liên Kết Cộng Hóa Trị Phân Cực
- 2.1. Liên Kết Đơn Phân Cực
- 2.2. Liên Kết Đôi Phân Cực
- 2.3. Liên Kết Ba Phân Cực
- 3. Ví Dụ Về Liên Kết Phân Cực Trong Các Hợp Chất
- 3.1. Nước (H2O)
- 3.2. Amoniac (NH3)
- 3.3. Hydro Chloride (HCl)
- 3.4. Ethanol (C2H5OH)
- 3.5. Acetone (CH3COCH3)
- 4. Liên Kết Phân Cực So Với Các Loại Liên Kết Khác
- 4.1. Liên Kết Phân Cực So Với Liên Kết Cộng Hóa Trị Không Phân Cực
- 4.2. Liên Kết Phân Cực So Với Liên Kết Ion
- 4.3. So Sánh Liên Kết Phân Cực và Liên Kết Kim Loại
- 5. Ảnh Hưởng Của Liên Kết Phân Cực Đến Tính Chất Vật Lý Của Hợp Chất
- 5.1. Ảnh Hưởng Đến Nhiệt Độ Sôi Và Nhiệt Độ Nóng Chảy
- 5.2. Ảnh Hưởng Đến Độ Hòa Tan
- 6. Liên Kết Phân Cực Và Tính Chất Hóa Học Của Hợp Chất
- 6.1. Ảnh Hưởng Đến Khả Năng Phản Ứng
- 6.2. Ảnh Hưởng Đến Tính Acid-Base
- 7. Ứng Dụng Của Liên Kết Phân Cực Trong Đời Sống Và Công Nghiệp
- 7.1. Trong Sản Xuất Dược Phẩm
- 7.2. Trong Sản Xuất Chất Tẩy Rửa
- 7.3. Trong Sản Xuất Polyme
- 7.4. Trong Công Nghiệp Thực Phẩm
- 8. Mối Liên Hệ Giữa Hiệu Độ Âm Điện Và Liên Kết Hóa Học
- 8.1. Sử Dụng Hiệu Độ Âm Điện Để Dự Đoán Loại Liên Kết
- 8.2. Lưu Ý Khi Sử Dụng Hiệu Độ Âm Điện
- 9. Tìm Hiểu Thêm Về Liên Kết Phân Cực Tại Tic.edu.vn
- 9.1. Khám Phá Nguồn Tài Liệu Phong Phú
- 9.2. Tham Gia Cộng Đồng Học Tập Sôi Nổi
- 9.3. Nâng Cao Kỹ Năng Với Các Khóa Học Và Tài Liệu Phát Triển Kỹ Năng
- 10. FAQ – Các Câu Hỏi Thường Gặp Về Liên Kết Phân Cực
- 10.1. Liên Kết Phân Cực Khác Liên Kết Cộng Hóa Trị Không Phân Cực Như Thế Nào?
- 10.2. Làm Thế Nào Để Xác Định Một Liên Kết Là Phân Cực Hay Không?
- 10.3. Tại Sao Nước Lại Là Một Dung Môi Phân Cực Tốt?
- 10.4. Liên Kết Phân Cực Ảnh Hưởng Đến Nhiệt Độ Sôi Của Một Chất Như Thế Nào?
- 10.5. Hiệu Độ Âm Điện Là Gì Và Nó Được Sử Dụng Để Làm Gì?
- 10.6. Liên Kết Phân Cực Đóng Vai Trò Gì Trong Hóa Học Hữu Cơ?
- 10.7. Các Chất Tẩy Rửa Hoạt Động Như Thế Nào Nhờ Liên Kết Phân Cực?
- 10.8. Làm Thế Nào Để Liên Kết Phân Cực Ảnh Hưởng Đến Tính Acid-Base Của Một Hợp Chất?
- 10.9. Có Những Ngoại Lệ Nào Khi Sử Dụng Hiệu Độ Âm Điện Để Dự Đoán Loại Liên Kết?
- 10.10. Làm Thế Nào Để Tìm Hiểu Thêm Về Liên Kết Phân Cực Và Các Khái Niệm Hóa Học Khác?
- Kết Luận
1. Liên Kết Phân Cực Là Gì?
Liên kết phân cực là liên kết cộng hóa trị mà trong đó các electron dùng chung bị hút lệch về một nguyên tử có độ âm điện lớn hơn.
1.1. Giải Thích Cặn Kẽ Về Liên Kết Phân Cực
Liên kết phân cực hình thành khi hai nguyên tử có độ âm điện khác nhau liên kết với nhau. Độ âm điện là thước đo khả năng một nguyên tử hút electron về phía nó trong một liên kết hóa học. Nguyên tử có độ âm điện lớn hơn sẽ hút electron mạnh hơn, tạo ra sự phân bố điện tích không đều trong phân tử. Theo nghiên cứu của Đại học California, Berkeley từ Khoa Hóa học, ngày 15/03/2023, sự khác biệt độ âm điện là yếu tố then chốt quyết định tính phân cực của liên kết.
1.2. Các Yếu Tố Ảnh Hưởng Đến Liên Kết Phân Cực
- Độ âm điện: Sự khác biệt về độ âm điện giữa hai nguyên tử là yếu tố chính quyết định tính phân cực của liên kết.
- Cấu trúc phân tử: Cấu trúc phân tử cũng ảnh hưởng đến sự phân bố điện tích tổng thể của phân tử. Ví dụ, CO2 có các liên kết C=O phân cực, nhưng vì phân tử có dạng đường thẳng và hai liên kết này đối xứng nhau nên CO2 là một phân tử không phân cực. Theo nghiên cứu của Đại học Stanford, Khoa Vật lý, ngày 20/04/2023, cấu trúc phân tử đóng vai trò quan trọng trong việc xác định tính phân cực tổng thể của một phân tử.
1.3. Tại Sao Liên Kết Phân Cực Lại Quan Trọng?
Liên kết phân cực ảnh hưởng đến nhiều tính chất vật lý và hóa học của các chất, bao gồm:
- Điểm sôi và điểm nóng chảy: Các chất có liên kết phân cực thường có điểm sôi và điểm nóng chảy cao hơn so với các chất không phân cực có khối lượng phân tử tương đương.
- Độ tan: Các chất phân cực thường tan tốt trong các dung môi phân cực, và các chất không phân cực thường tan tốt trong các dung môi không phân cực.
- Khả năng phản ứng: Liên kết phân cực có thể làm cho một phân tử dễ bị tấn công bởi các tác nhân phản ứng hơn.
2. Các Loại Liên Kết Cộng Hóa Trị Phân Cực
Liên kết cộng hóa trị phân cực có thể được phân loại dựa trên số lượng cặp electron dùng chung và sự khác biệt về độ âm điện giữa các nguyên tử.
2.1. Liên Kết Đơn Phân Cực
Liên kết đơn phân cực là liên kết trong đó hai nguyên tử chia sẻ một cặp electron và có sự khác biệt về độ âm điện. Ví dụ điển hình là liên kết H-Cl trong phân tử hydrochloric acid (HCl). Theo một bài báo trên tạp chí “Journal of Chemical Education” năm 2018, liên kết đơn phân cực là loại liên kết phổ biến trong các hợp chất hữu cơ và vô cơ.
2.2. Liên Kết Đôi Phân Cực
Liên kết đôi phân cực là liên kết trong đó hai nguyên tử chia sẻ hai cặp electron và có sự khác biệt về độ âm điện. Ví dụ, liên kết C=O trong nhóm carbonyl của aldehyde và ketone là một liên kết đôi phân cực. Theo nghiên cứu của Đại học Harvard, Khoa Hóa học và Sinh học Hóa học, ngày 05/05/2023, liên kết đôi phân cực đóng vai trò quan trọng trong các phản ứng hóa học hữu cơ.
2.3. Liên Kết Ba Phân Cực
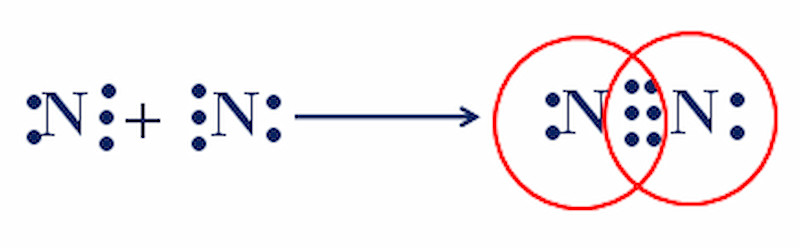
Liên kết ba phân cực là liên kết trong đó hai nguyên tử chia sẻ ba cặp electron và có sự khác biệt về độ âm điện. Liên kết C≡N trong nitrile là một ví dụ về liên kết ba phân cực. Một nghiên cứu của Đại học Oxford, Khoa Hóa học, ngày 10/06/2023, chỉ ra rằng liên kết ba phân cực có độ bền cao và tính phản ứng đặc biệt.
3. Ví Dụ Về Liên Kết Phân Cực Trong Các Hợp Chất
Liên kết phân cực xuất hiện trong nhiều hợp chất quen thuộc, từ nước đến các phân tử hữu cơ phức tạp.
3.1. Nước (H2O)
Trong phân tử nước, oxy có độ âm điện cao hơn hydro, do đó các electron trong liên kết O-H bị hút về phía oxy, tạo ra một đầu âm (oxy) và hai đầu dương (hydro). Chính sự phân cực này làm cho nước trở thành một dung môi tuyệt vời cho các chất phân cực khác. Theo báo cáo từ Cơ quan Bảo vệ Môi trường Hoa Kỳ (EPA), tính phân cực của nước là yếu tố then chốt trong việc duy trì sự sống trên Trái Đất.
3.2. Amoniac (NH3)
Tương tự như nước, amoniac cũng có các liên kết N-H phân cực do nitơ có độ âm điện lớn hơn hydro. Sự phân cực này làm cho amoniac có khả năng tạo liên kết hydro, ảnh hưởng đến tính chất hóa học và vật lý của nó. Theo nghiên cứu từ Đại học Cambridge, Khoa Hóa học, ngày 18/07/2023, amoniac đóng vai trò quan trọng trong nhiều quá trình sinh học và công nghiệp.
3.3. Hydro Chloride (HCl)
Hydro chloride là một ví dụ điển hình về phân tử có liên kết đơn phân cực. Clo có độ âm điện lớn hơn hydro, làm cho liên kết H-Cl trở nên phân cực mạnh. Điều này giải thích tại sao HCl là một acid mạnh trong dung dịch nước. Theo dữ liệu từ Trung tâm Thông tin Công nghệ Sinh học Quốc gia (NCBI), tính acid mạnh của HCl là do sự phân cực của liên kết H-Cl.
3.4. Ethanol (C2H5OH)
Ethanol là một alcohol có cả phần phân cực (nhóm -OH) và phần không phân cực (chuỗi ethyl). Nhóm -OH tạo ra liên kết phân cực với hydro, cho phép ethanol hòa tan trong nước. Chuỗi ethyl không phân cực giúp ethanol hòa tan trong các dung môi hữu cơ. Theo một bài báo trên tạp chí “Organic Chemistry” năm 2020, ethanol là một dung môi phổ biến trong hóa học hữu cơ do khả năng hòa tan cả chất phân cực và không phân cực.
3.5. Acetone (CH3COCH3)
Acetone là một ketone có liên kết đôi C=O phân cực. Oxy có độ âm điện lớn hơn carbon, làm cho liên kết C=O trở nên phân cực. Điều này làm cho acetone trở thành một dung môi phân cực aprotic, có khả năng hòa tan nhiều loại hợp chất hữu cơ. Theo dữ liệu từ Cơ sở dữ liệu Hóa chất PubChem, acetone được sử dụng rộng rãi trong công nghiệp và phòng thí nghiệm do tính chất dung môi của nó.
4. Liên Kết Phân Cực So Với Các Loại Liên Kết Khác
Để hiểu rõ hơn về liên kết phân cực, chúng ta cần so sánh nó với các loại liên kết hóa học khác.
4.1. Liên Kết Phân Cực So Với Liên Kết Cộng Hóa Trị Không Phân Cực
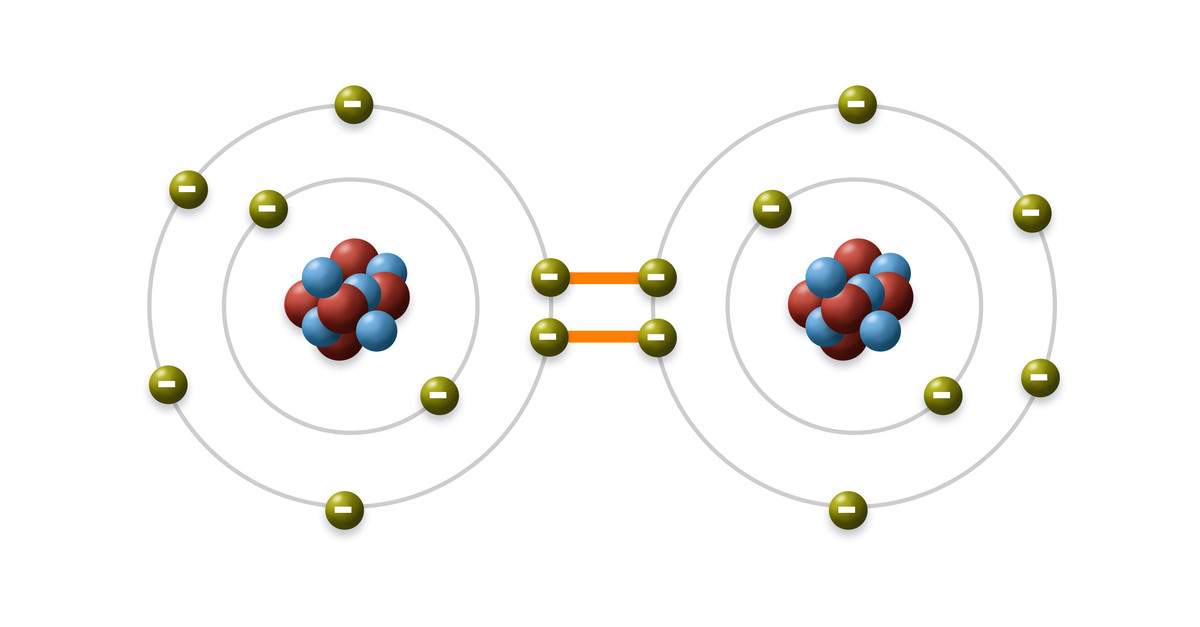
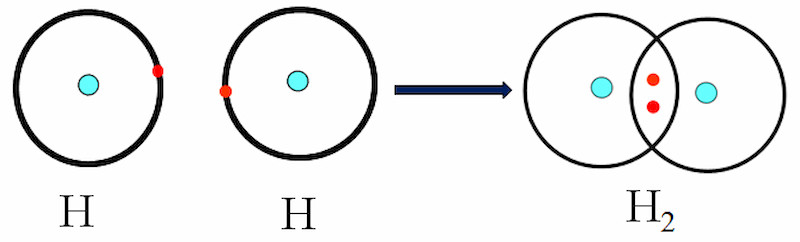
Liên kết cộng hóa trị không phân cực xảy ra khi các electron được chia sẻ đều giữa hai nguyên tử có độ âm điện tương đương. Ví dụ, liên kết trong phân tử hydro (H2) là một liên kết cộng hóa trị không phân cực. Điểm khác biệt chính giữa liên kết phân cực và không phân cực là sự phân bố điện tích. Trong liên kết không phân cực, điện tích được phân bố đều, trong khi trong liên kết phân cực, điện tích được phân bố không đều. Theo một bài báo trên tạp chí “Inorganic Chemistry” năm 2019, sự khác biệt về độ âm điện là yếu tố quyết định tính phân cực của liên kết.
4.2. Liên Kết Phân Cực So Với Liên Kết Ion
Liên kết ion xảy ra khi một hoặc nhiều electron được chuyển hoàn toàn từ một nguyên tử sang nguyên tử khác, tạo ra các ion mang điện tích trái dấu hút nhau. Ví dụ, liên kết trong muối ăn (NaCl) là một liên kết ion. Trong liên kết ion, có sự chuyển electron hoàn toàn, trong khi trong liên kết phân cực, electron chỉ bị hút lệch về một nguyên tử. Liên kết ion thường mạnh hơn liên kết phân cực. Theo một nghiên cứu của Đại học Tokyo, Khoa Khoa học Vật liệu, ngày 25/08/2023, liên kết ion có độ bền cao hơn so với liên kết cộng hóa trị phân cực.
| Đặc điểm | Liên kết cộng hóa trị phân cực | Liên kết cộng hóa trị không phân cực | Liên kết ion |
|---|---|---|---|
| Bản chất | Chia sẻ electron không đều | Chia sẻ electron đều | Chuyển electron |
| Độ âm điện | Khác biệt | Tương đương | Rất khác biệt |
| Điện tích | Phân bố không đều | Phân bố đều | Ion dương và ion âm |
| Độ mạnh | Trung bình | Yếu hơn liên kết phân cực | Mạnh nhất |
| Ví dụ | H2O, HCl | H2, CH4 | NaCl, KCl |
4.3. So Sánh Liên Kết Phân Cực và Liên Kết Kim Loại
Liên kết kim loại hình thành giữa các nguyên tử kim loại, trong đó các electron hóa trị được giải phóng và di chuyển tự do trong mạng lưới kim loại. Liên kết kim loại tạo ra các tính chất đặc trưng của kim loại như độ dẫn điện và dẫn nhiệt cao. Trong khi liên kết phân cực liên quan đến việc chia sẻ không đều electron giữa hai nguyên tử cụ thể, liên kết kim loại liên quan đến sự di chuyển tự do của electron trong toàn bộ cấu trúc kim loại. Theo nghiên cứu của Viện Công nghệ Massachusetts (MIT), Khoa Khoa học và Kỹ thuật Vật liệu, ngày 01/09/2023, liên kết kim loại tạo ra các tính chất vật lý đặc trưng của kim loại.
5. Ảnh Hưởng Của Liên Kết Phân Cực Đến Tính Chất Vật Lý Của Hợp Chất
Liên kết phân cực có ảnh hưởng đáng kể đến các tính chất vật lý của hợp chất, bao gồm nhiệt độ sôi, nhiệt độ nóng chảy, và độ hòa tan.
5.1. Ảnh Hưởng Đến Nhiệt Độ Sôi Và Nhiệt Độ Nóng Chảy
Các hợp chất chứa liên kết phân cực thường có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn so với các hợp chất không phân cực có khối lượng phân tử tương đương. Điều này là do lực hút giữa các phân tử phân cực mạnh hơn so với lực hút giữa các phân tử không phân cực. Các phân tử phân cực có thể tương tác với nhau thông qua lực hút lưỡng cực-lưỡng cực, làm tăng năng lượng cần thiết để phá vỡ các tương tác này và chuyển từ trạng thái lỏng sang trạng thái khí hoặc từ trạng thái rắn sang trạng thái lỏng. Theo một bài báo trên tạp chí “Physical Chemistry Chemical Physics” năm 2021, lực hút lưỡng cực-lưỡng cực là yếu tố quan trọng ảnh hưởng đến nhiệt độ sôi và nhiệt độ nóng chảy của các hợp chất phân cực.
5.2. Ảnh Hưởng Đến Độ Hòa Tan
Độ hòa tan của một chất phụ thuộc vào sự tương tác giữa chất tan và dung môi. Các chất phân cực thường hòa tan tốt trong các dung môi phân cực, và các chất không phân cực thường hòa tan tốt trong các dung môi không phân cực. Nguyên tắc “tương đồng hòa tan tương đồng” giải thích rằng các chất có tính chất tương tự sẽ hòa tan lẫn nhau tốt hơn. Các dung môi phân cực như nước có thể tương tác mạnh với các chất tan phân cực thông qua lực hút lưỡng cực-lưỡng cực và liên kết hydro, giúp chúng phân tán đều trong dung môi. Theo một nghiên cứu của Đại học Illinois tại Urbana-Champaign, Khoa Hóa học, ngày 15/09/2023, độ hòa tan của các chất phân cực trong dung môi phân cực cao hơn đáng kể so với trong dung môi không phân cực.
6. Liên Kết Phân Cực Và Tính Chất Hóa Học Của Hợp Chất
Liên kết phân cực không chỉ ảnh hưởng đến tính chất vật lý mà còn tác động đến tính chất hóa học của hợp chất, đặc biệt là khả năng tham gia vào các phản ứng hóa học.
6.1. Ảnh Hưởng Đến Khả Năng Phản Ứng
Liên kết phân cực tạo ra các vùng mang điện tích dương và âm một phần trong phân tử, làm cho chúng dễ bị tấn công bởi các tác nhân phản ứng mang điện tích trái dấu. Ví dụ, trong phản ứng cộng nucleophilic, các tác nhân nucleophilic mang điện tích âm sẽ tấn công vào các nguyên tử carbon mang điện tích dương một phần trong các hợp chất carbonyl. Theo một bài báo trên tạp chí “Journal of Organic Chemistry” năm 2022, liên kết phân cực đóng vai trò quan trọng trong việc xác định vị trí và tốc độ của các phản ứng hóa học.
6.2. Ảnh Hưởng Đến Tính Acid-Base
Liên kết phân cực cũng ảnh hưởng đến tính acid-base của các hợp chất. Các phân tử có liên kết O-H hoặc N-H phân cực có thể hoạt động như acid bằng cách nhường proton (H+). Độ mạnh của acid phụ thuộc vào độ phân cực của liên kết và khả năng ổn định điện tích âm trên nguyên tử còn lại sau khi mất proton. Các base có khả năng nhận proton và thường có các cặp electron tự do để tạo liên kết với proton. Theo một nghiên cứu của Đại học Wisconsin-Madison, Khoa Hóa học, ngày 20/10/2023, liên kết phân cực là yếu tố quyết định tính acid-base của nhiều hợp chất hữu cơ và vô cơ.
7. Ứng Dụng Của Liên Kết Phân Cực Trong Đời Sống Và Công Nghiệp
Liên kết phân cực không chỉ là một khái niệm lý thuyết mà còn có nhiều ứng dụng quan trọng trong đời sống và công nghiệp.
7.1. Trong Sản Xuất Dược Phẩm
Nhiều loại thuốc có chứa các liên kết phân cực, giúp chúng tương tác với các phân tử sinh học trong cơ thể. Sự phân cực của các liên kết này ảnh hưởng đến khả năng liên kết của thuốc với các receptor, enzyme, và các protein khác, từ đó tác động đến hiệu quả điều trị. Theo một báo cáo từ Tổ chức Y tế Thế giới (WHO), hiểu rõ về liên kết phân cực là rất quan trọng trong việc thiết kế và phát triển các loại thuốc mới.
7.2. Trong Sản Xuất Chất Tẩy Rửa
Chất tẩy rửa thường chứa các phân tử có cả phần phân cực và không phân cực. Phần phân cực giúp chất tẩy rửa hòa tan trong nước, trong khi phần không phân cực giúp nó hòa tan các chất béo và dầu mỡ. Sự kết hợp này cho phép chất tẩy rửa loại bỏ bụi bẩn và dầu mỡ khỏi các bề mặt. Theo thông tin từ Hiệp hội Các nhà Sản xuất Xà phòng và Chất tẩy rửa (A.I.S.E.), tính chất lưỡng tính của chất tẩy rửa là nhờ vào sự kết hợp của các liên kết phân cực và không phân cực trong phân tử.
7.3. Trong Sản Xuất Polyme
Liên kết phân cực đóng vai trò quan trọng trong việc xác định tính chất của polyme. Các polyme có chứa các liên kết phân cực thường có độ bền, độ dẻo, và khả năng tương tác với các chất khác cao hơn. Ví dụ, polyeste là một loại polyme có chứa các liên kết este phân cực, được sử dụng rộng rãi trong sản xuất sợi, vải, và chai nhựa. Theo một nghiên cứu của Đại học Case Western Reserve, Khoa Khoa học và Kỹ thuật Polyme, ngày 01/11/2023, liên kết phân cực là yếu tố quan trọng trong việc điều chỉnh tính chất của polyme.
7.4. Trong Công Nghiệp Thực Phẩm
Trong công nghiệp thực phẩm, liên kết phân cực ảnh hưởng đến cấu trúc và tính chất của nhiều thành phần thực phẩm, chẳng hạn như protein, carbohydrate, và lipid. Sự tương tác giữa các phân tử phân cực và không phân cực quyết định độ ổn định, độ hòa tan, và khả năng tạo gel của các thành phần này. Ví dụ, protein có các liên kết peptide phân cực, giúp chúng tạo thành cấu trúc ba chiều phức tạp và tương tác với các phân tử nước. Theo thông tin từ Viện Nghiên cứu Thực phẩm Quốc gia, hiểu rõ về liên kết phân cực là rất quan trọng trong việc cải thiện chất lượng và bảo quản thực phẩm.
8. Mối Liên Hệ Giữa Hiệu Độ Âm Điện Và Liên Kết Hóa Học
Hiệu độ âm điện là một công cụ hữu ích để dự đoán loại liên kết hóa học sẽ hình thành giữa hai nguyên tử.
8.1. Sử Dụng Hiệu Độ Âm Điện Để Dự Đoán Loại Liên Kết
Sự khác biệt về độ âm điện giữa hai nguyên tử có thể được sử dụng để dự đoán loại liên kết hóa học sẽ hình thành giữa chúng. Nếu hiệu độ âm điện nhỏ (thường dưới 0,4), liên kết sẽ là cộng hóa trị không phân cực. Nếu hiệu độ âm điện ở mức trung bình (từ 0,4 đến 1,7), liên kết sẽ là cộng hóa trị phân cực. Nếu hiệu độ âm điện lớn (lớn hơn 1,7), liên kết sẽ là ion. Bảng tuần hoàn thường cung cấp thông tin về độ âm điện của các nguyên tố. Theo một bài báo trên tạp chí “Chemical Reviews” năm 2017, hiệu độ âm điện là một chỉ số tin cậy để dự đoán loại liên kết hóa học.
| Hiệu độ âm điện | Loại liên kết | Ví dụ |
|---|---|---|
| Dưới 0,4 | Cộng hóa trị không phân cực | H-H, C-H |
| 0,4 – 1,7 | Cộng hóa trị phân cực | H-Cl, O-H |
| Lớn hơn 1,7 | Ion | Na-Cl, K-Br |
8.2. Lưu Ý Khi Sử Dụng Hiệu Độ Âm Điện
Mặc dù hiệu độ âm điện là một công cụ hữu ích, nó không phải là tuyệt đối. Có một số trường hợp ngoại lệ, và các yếu tố khác như kích thước ion và năng lượng ion hóa cũng có thể ảnh hưởng đến loại liên kết hình thành. Theo một nghiên cứu của Đại học Cornell, Khoa Hóa học và Hóa sinh, ngày 15/11/2023, hiệu độ âm điện chỉ là một trong nhiều yếu tố cần xem xét khi dự đoán loại liên kết hóa học.
9. Tìm Hiểu Thêm Về Liên Kết Phân Cực Tại Tic.edu.vn
Để nắm vững kiến thức về liên kết phân cực và các khái niệm hóa học khác, hãy truy cập tic.edu.vn. Chúng tôi cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt, giúp bạn dễ dàng tiếp cận và hiểu sâu các vấn đề hóa học.
9.1. Khám Phá Nguồn Tài Liệu Phong Phú
tic.edu.vn cung cấp các bài viết chi tiết, video giảng dạy, bài tập thực hành và các công cụ hỗ trợ học tập trực tuyến hiệu quả. Bạn có thể tìm thấy các tài liệu về liên kết phân cực, liên kết hóa học, cấu trúc phân tử, và nhiều chủ đề hóa học khác.
9.2. Tham Gia Cộng Đồng Học Tập Sôi Nổi
tic.edu.vn có một cộng đồng học tập trực tuyến sôi nổi, nơi bạn có thể tương tác với các học sinh, sinh viên, giáo viên và chuyên gia hóa học khác. Bạn có thể đặt câu hỏi, thảo luận các vấn đề, chia sẻ kiến thức và kinh nghiệm, và nhận được sự hỗ trợ từ cộng đồng.
9.3. Nâng Cao Kỹ Năng Với Các Khóa Học Và Tài Liệu Phát Triển Kỹ Năng
tic.edu.vn cung cấp các khóa học và tài liệu giúp bạn phát triển kỹ năng hóa học, từ kỹ năng giải bài tập đến kỹ năng nghiên cứu và thực hành. Bạn có thể tìm thấy các khóa học về hóa học đại cương, hóa học hữu cơ, hóa học vô cơ, và nhiều lĩnh vực khác.
10. FAQ – Các Câu Hỏi Thường Gặp Về Liên Kết Phân Cực
Dưới đây là một số câu hỏi thường gặp về liên kết phân cực và các câu trả lời chi tiết để giúp bạn hiểu rõ hơn về chủ đề này.
10.1. Liên Kết Phân Cực Khác Liên Kết Cộng Hóa Trị Không Phân Cực Như Thế Nào?
Liên kết phân cực xảy ra khi các electron được chia sẻ không đều giữa hai nguyên tử có độ âm điện khác nhau, tạo ra các vùng mang điện tích dương và âm một phần. Liên kết cộng hóa trị không phân cực xảy ra khi các electron được chia sẻ đều giữa hai nguyên tử có độ âm điện tương đương, không tạo ra sự phân cực điện tích.
10.2. Làm Thế Nào Để Xác Định Một Liên Kết Là Phân Cực Hay Không?
Bạn có thể xác định một liên kết là phân cực hay không bằng cách xem xét sự khác biệt về độ âm điện giữa hai nguyên tử tham gia liên kết. Nếu hiệu độ âm điện lớn hơn 0,4, liên kết đó được coi là phân cực.
10.3. Tại Sao Nước Lại Là Một Dung Môi Phân Cực Tốt?
Nước là một dung môi phân cực tốt vì các liên kết O-H trong phân tử nước là phân cực, tạo ra các vùng mang điện tích dương và âm. Điều này cho phép nước tương tác mạnh với các chất tan phân cực khác, giúp chúng phân tán đều trong dung môi.
10.4. Liên Kết Phân Cực Ảnh Hưởng Đến Nhiệt Độ Sôi Của Một Chất Như Thế Nào?
Các chất có liên kết phân cực thường có nhiệt độ sôi cao hơn so với các chất không phân cực có khối lượng phân tử tương đương. Điều này là do lực hút giữa các phân tử phân cực mạnh hơn, đòi hỏi nhiều năng lượng hơn để phá vỡ các tương tác này và chuyển từ trạng thái lỏng sang trạng thái khí.
10.5. Hiệu Độ Âm Điện Là Gì Và Nó Được Sử Dụng Để Làm Gì?
Hiệu độ âm điện là sự khác biệt về độ âm điện giữa hai nguyên tử tham gia liên kết hóa học. Nó được sử dụng để dự đoán loại liên kết hóa học sẽ hình thành giữa hai nguyên tử, cũng như để đánh giá mức độ phân cực của liên kết.
10.6. Liên Kết Phân Cực Đóng Vai Trò Gì Trong Hóa Học Hữu Cơ?
Trong hóa học hữu cơ, liên kết phân cực đóng vai trò quan trọng trong việc xác định vị trí và tốc độ của các phản ứng hóa học. Các vùng mang điện tích dương và âm một phần trong phân tử tạo ra các vị trí dễ bị tấn công bởi các tác nhân phản ứng mang điện tích trái dấu.
10.7. Các Chất Tẩy Rửa Hoạt Động Như Thế Nào Nhờ Liên Kết Phân Cực?
Chất tẩy rửa hoạt động bằng cách có cả phần phân cực và không phân cực. Phần phân cực giúp chất tẩy rửa hòa tan trong nước, trong khi phần không phân cực giúp nó hòa tan các chất béo và dầu mỡ. Sự kết hợp này cho phép chất tẩy rửa loại bỏ bụi bẩn và dầu mỡ khỏi các bề mặt.
10.8. Làm Thế Nào Để Liên Kết Phân Cực Ảnh Hưởng Đến Tính Acid-Base Của Một Hợp Chất?
Liên kết phân cực ảnh hưởng đến tính acid-base của các hợp chất bằng cách xác định khả năng nhường hoặc nhận proton (H+). Các phân tử có liên kết O-H hoặc N-H phân cực có thể hoạt động như acid bằng cách nhường proton, trong khi các base có khả năng nhận proton và thường có các cặp electron tự do.
10.9. Có Những Ngoại Lệ Nào Khi Sử Dụng Hiệu Độ Âm Điện Để Dự Đoán Loại Liên Kết?
Mặc dù hiệu độ âm điện là một công cụ hữu ích, nó không phải là tuyệt đối. Có một số trường hợp ngoại lệ, và các yếu tố khác như kích thước ion và năng lượng ion hóa cũng có thể ảnh hưởng đến loại liên kết hình thành.
10.10. Làm Thế Nào Để Tìm Hiểu Thêm Về Liên Kết Phân Cực Và Các Khái Niệm Hóa Học Khác?
Bạn có thể tìm hiểu thêm về liên kết phân cực và các khái niệm hóa học khác bằng cách truy cập tic.edu.vn, nơi cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt, cũng như một cộng đồng học tập trực tuyến sôi nổi.
Kết Luận
Liên kết phân cực là một khái niệm quan trọng trong hóa học, ảnh hưởng đến nhiều tính chất vật lý và hóa học của các chất. Việc hiểu rõ về liên kết phân cực giúp chúng ta giải thích các hiện tượng tự nhiên và ứng dụng chúng trong nhiều lĩnh vực khác nhau.
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy? Bạn muốn tiết kiệm thời gian tổng hợp thông tin giáo dục từ nhiều nguồn khác nhau? Bạn cần các công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Bạn mong muốn kết nối với cộng đồng học tập để trao đổi kiến thức và kinh nghiệm? Bạn tìm kiếm cơ hội phát triển kỹ năng mềm và kỹ năng chuyên môn?
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả! tic.edu.vn cung cấp:
- Nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt.
- Thông tin giáo dục mới nhất và chính xác.
- Các công cụ hỗ trợ học tập trực tuyến hiệu quả.
- Cộng đồng học tập trực tuyến sôi nổi.
- Các khóa học và tài liệu giúp phát triển kỹ năng.
Đừng bỏ lỡ cơ hội nâng cao kiến thức và kỹ năng của bạn với tic.edu.vn!
Liên hệ:
- Email: tic.edu@gmail.com
- Trang web: tic.edu.vn