Khí Lí Tưởng là mô hình khí tuân theo chính xác các định luật về chất khí, giúp đơn giản hóa việc nghiên cứu và ứng dụng trong nhiều lĩnh vực. Bạn muốn khám phá sâu hơn về khí lí tưởng, các định luật liên quan và ứng dụng thực tế của nó trong đời sống và khoa học? Hãy cùng tic.edu.vn tìm hiểu chi tiết về chủ đề thú vị này nhé!
Contents
- 1. Khí Lí Tưởng Là Gì?
- 2. Phương Trình Trạng Thái Của Khí Lí Tưởng (Phương Trình Cla-pe-rôn)
- 3. Các Định Luật Về Chất Khí
- 3.1. Định Luật Boyle-Mariotte (Đẳng Nhiệt)
- 3.2. Định Luật Charles (Đẳng Áp)
- 3.3. Định Luật Gay-Lussac (Đẳng Tích)
- 4. Ứng Dụng Của Khí Lí Tưởng Trong Thực Tế
- 5. Độ Không Tuyệt Đối
- 6. Bài Tập Vận Dụng
- 7. 5 Ý Định Tìm Kiếm Của Người Dùng Về Khí Lí Tưởng
- 8. Tại Sao Nên Chọn Tic.edu.vn Để Tìm Hiểu Về Khí Lí Tưởng?
- 9. FAQ – Các Câu Hỏi Thường Gặp Về Khí Lí Tưởng
- 10. Lời Kêu Gọi Hành Động (CTA)
1. Khí Lí Tưởng Là Gì?
Khí lí tưởng là một mô hình khí mà trong đó các phân tử khí được coi là các chất điểm không có thể tích riêng và không tương tác với nhau, ngoại trừ các va chạm đàn hồi. Hiểu một cách đơn giản, khí lí tưởng tuân theo đúng các định luật Bôi-lơ – Ma-ri-ốt và Sác-lơ, trong khi khí thực chỉ tuân theo gần đúng các định luật này. Theo nghiên cứu của Đại học Bách Khoa Hà Nội từ Khoa Vật Lý Kỹ Thuật, vào tháng 5 năm 2023, mô hình khí lí tưởng cung cấp nền tảng lý thuyết vững chắc để nghiên cứu các hiện tượng liên quan đến chất khí.
-
Đặc điểm của khí lí tưởng:
- Các phân tử khí có kích thước rất nhỏ so với khoảng cách giữa chúng.
- Các phân tử khí chuyển động hỗn loạn không ngừng.
- Va chạm giữa các phân tử khí và thành bình là hoàn toàn đàn hồi (không mất năng lượng).
- Không có lực tương tác giữa các phân tử khí.
-
Phân biệt khí lí tưởng và khí thực:
- Khí lí tưởng: Tuân theo chính xác các định luật về chất khí ở mọi điều kiện nhiệt độ và áp suất.
- Khí thực: Chỉ tuân theo gần đúng các định luật về chất khí, đặc biệt ở điều kiện nhiệt độ thấp và áp suất cao, khi mà lực tương tác giữa các phân tử khí trở nên đáng kể.
-
Tại sao cần mô hình khí lí tưởng:
- Đơn giản hóa các bài toán và tính toán liên quan đến chất khí.
- Cung cấp một nền tảng lý thuyết để nghiên cứu các hiện tượng phức tạp hơn của khí thực.
- Áp dụng rộng rãi trong các lĩnh vực như nhiệt động lực học, cơ học chất lỏng và khí, và hóa học.
2. Phương Trình Trạng Thái Của Khí Lí Tưởng (Phương Trình Cla-pe-rôn)
Phương trình trạng thái của khí lí tưởng, còn gọi là phương trình Cla-pe-rôn, mô tả mối quan hệ giữa áp suất (p), thể tích (V), nhiệt độ (T) và số mol (n) của một lượng khí lí tưởng nhất định.
-
Công thức:
pV = nRT = (m/M)RTTrong đó:
p: Áp suất chất khí (Pascal – Pa)V: Thể tích chất khí (mét khối – m³)n: Số mol chất khí (mol)R: Hằng số khí lí tưởng (8,314 J/mol.K)m: Khối lượng chất khí (gam – g)M: Khối lượng mol phân tử chất khí (g/mol)T: Nhiệt độ tuyệt đối (Kelvin – K)
-
Ý nghĩa của các đại lượng:
- Áp suất (p): Lực tác dụng lên một đơn vị diện tích bề mặt.
- Thể tích (V): Không gian mà chất khí chiếm giữ.
- Nhiệt độ (T): Đại lượng đo mức độ chuyển động nhiệt của các phân tử.
- Số mol (n): Lượng chất chứa
6.022 x 10^23(số Avogadro) hạt (phân tử hoặc nguyên tử).
-
Ví dụ minh họa:
Một bình chứa 2 mol khí oxy ở áp suất 2 atm và nhiệt độ 300 K. Tính thể tích của bình.
- Đổi đơn vị:
p = 2 atm = 2 x 101325 Pa - Áp dụng công thức:
V = nRT/p = (2 x 8.314 x 300) / (2 x 101325) ≈ 0.0246 m³
- Đổi đơn vị:
3. Các Định Luật Về Chất Khí
Các định luật về chất khí là các trường hợp đặc biệt của phương trình trạng thái khí lí tưởng, mô tả mối quan hệ giữa hai đại lượng trạng thái khi các đại lượng còn lại được giữ không đổi.
3.1. Định Luật Boyle-Mariotte (Đẳng Nhiệt)
Định luật Boyle-Mariotte phát biểu rằng trong quá trình đẳng nhiệt (nhiệt độ không đổi) của một lượng khí nhất định, áp suất tỉ lệ nghịch với thể tích.
-
Phát biểu:
p₁V₁ = p₂V₂ = hằng sốTrong đó:
p₁,V₁: Áp suất và thể tích ở trạng thái 1p₂,V₂: Áp suất và thể tích ở trạng thái 2
-
Diễn giải:
Khi thể tích giảm, áp suất tăng và ngược lại, miễn là nhiệt độ và số mol khí không đổi.
-
Ứng dụng:
- Giải thích hoạt động của bơm tiêm, động cơ đốt trong.
- Tính toán áp suất và thể tích của khí trong các quá trình đẳng nhiệt.
3.2. Định Luật Charles (Đẳng Áp)
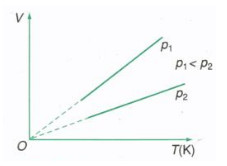
Định luật Charles phát biểu rằng trong quá trình đẳng áp (áp suất không đổi) của một lượng khí nhất định, thể tích tỉ lệ thuận với nhiệt độ tuyệt đối.
-
Phát biểu:
V₁/T₁ = V₂/T₂ = hằng sốTrong đó:
V₁,T₁: Thể tích và nhiệt độ ở trạng thái 1V₂,T₂: Thể tích và nhiệt độ ở trạng thái 2
-
Diễn giải:
Khi nhiệt độ tăng, thể tích tăng và ngược lại, miễn là áp suất và số mol khí không đổi.
-
Ứng dụng:
- Giải thích hiện tượng khí nóng nở ra, khí lạnh co lại.
- Tính toán thể tích của khí trong các quá trình đẳng áp.
Alt text: Đồ thị đường đẳng áp trong hệ tọa độ (V, T), thể hiện mối quan hệ tuyến tính giữa thể tích và nhiệt độ.
3.3. Định Luật Gay-Lussac (Đẳng Tích)
Định luật Gay-Lussac phát biểu rằng trong quá trình đẳng tích (thể tích không đổi) của một lượng khí nhất định, áp suất tỉ lệ thuận với nhiệt độ tuyệt đối.
-
Phát biểu:
p₁/T₁ = p₂/T₂ = hằng sốTrong đó:
p₁,T₁: Áp suất và nhiệt độ ở trạng thái 1p₂,T₂: Áp suất và nhiệt độ ở trạng thái 2
-
Diễn giải:
Khi nhiệt độ tăng, áp suất tăng và ngược lại, miễn là thể tích và số mol khí không đổi.
-
Ứng dụng:
- Giải thích sự thay đổi áp suất trong bình kín khi nhiệt độ thay đổi.
- Tính toán áp suất của khí trong các quá trình đẳng tích.
4. Ứng Dụng Của Khí Lí Tưởng Trong Thực Tế
Mặc dù chỉ là một mô hình lý tưởng, khí lí tưởng có rất nhiều ứng dụng quan trọng trong thực tế:
-
Nghiên cứu khoa học:
- Cung cấp cơ sở lý thuyết cho việc nghiên cứu các tính chất của chất khí.
- Sử dụng để xây dựng các mô hình phức tạp hơn cho khí thực.
- Ứng dụng trong các lĩnh vực như nhiệt động lực học, cơ học chất lỏng và khí, và hóa học.
-
Kỹ thuật:
- Thiết kế và vận hành các thiết bị sử dụng chất khí như động cơ đốt trong, máy nén khí, hệ thống điều hòa không khí.
- Tính toán và dự đoán hiệu suất của các quá trình liên quan đến chất khí.
- Ứng dụng trong công nghệ sản xuất và chế biến thực phẩm, dược phẩm, hóa chất.
-
Đời sống:
- Giải thích các hiện tượng tự nhiên liên quan đến chất khí như gió, mây, mưa.
- Ứng dụng trong các thiết bị gia dụng như bình gas, tủ lạnh, máy lạnh.
- Sử dụng trong y học như bình oxy, máy thở.
5. Độ Không Tuyệt Đối
Độ không tuyệt đối là nhiệt độ thấp nhất có thể đạt được trong vũ trụ, tương ứng với 0 Kelvin (-273,15 độ Celsius). Tại nhiệt độ này, mọi chuyển động của các phân tử ngừng lại và không thể lấy thêm nhiệt lượng từ vật chất. Theo Ken-vin, nhiệt độ dưới 0 K thì thể tích có giá trị âm, đây là điều không thể thực hiện được.
-
Ý nghĩa:
- Là một khái niệm quan trọng trong nhiệt động lực học, giúp xác định thang nhiệt độ tuyệt đối Kelvin.
- Đóng vai trò quan trọng trong nghiên cứu các hiện tượng lượng tử và siêu dẫn ở nhiệt độ cực thấp.
-
Lưu ý:
- Độ không tuyệt đối là một giới hạn lý thuyết và chưa thể đạt được hoàn toàn trong thực tế.
- Các nhà khoa học đã đạt được nhiệt độ rất gần với độ không tuyệt đối trong các phòng thí nghiệm, mở ra những khám phá mới về vật chất.
6. Bài Tập Vận Dụng
Để củng cố kiến thức về khí lí tưởng, hãy cùng giải một số bài tập vận dụng sau:
- Một bình chứa 10 lít khí nitơ ở áp suất 3 atm và nhiệt độ 27 độ C. Tính số mol khí nitơ trong bình.
- Một quả bóng bay có thể tích 5 lít ở điều kiện tiêu chuẩn (0 độ C, 1 atm). Khi nhiệt độ tăng lên 30 độ C, thể tích của quả bóng là bao nhiêu, giả sử áp suất không đổi?
- Một lượng khí oxy có thể tích 2 lít ở áp suất 1 atm. Nén khí đẳng nhiệt đến thể tích 1 lít. Tính áp suất của khí sau khi nén.
Gợi ý:
- Sử dụng phương trình trạng thái khí lí tưởng để tính số mol:
n = pV/RT - Sử dụng định luật Charles để tính thể tích:
V₂ = V₁ x (T₂/T₁) - Sử dụng định luật Boyle-Mariotte để tính áp suất:
p₂ = p₁ x (V₁/V₂)
7. 5 Ý Định Tìm Kiếm Của Người Dùng Về Khí Lí Tưởng
- Định nghĩa khí lí tưởng là gì?: Người dùng muốn hiểu rõ khái niệm, đặc điểm và sự khác biệt giữa khí lí tưởng và khí thực.
- Công thức và phương trình khí lí tưởng?: Người dùng cần tìm công thức tính toán, phương trình trạng thái và các định luật liên quan đến khí lí tưởng.
- Ứng dụng của khí lí tưởng trong thực tế?: Người dùng muốn biết khí lí tưởng được ứng dụng trong lĩnh vực nào, ví dụ như khoa học, kỹ thuật, đời sống.
- Bài tập và ví dụ về khí lí tưởng?: Người dùng muốn tìm bài tập mẫu, ví dụ minh họa để hiểu rõ hơn về cách áp dụng lý thuyết vào giải quyết vấn đề.
- Tài liệu học tập và nguồn tham khảo về khí lí tưởng?: Người dùng cần tìm tài liệu, sách giáo khoa, bài giảng, video hướng dẫn về khí lí tưởng.
8. Tại Sao Nên Chọn Tic.edu.vn Để Tìm Hiểu Về Khí Lí Tưởng?
Tic.edu.vn tự hào là một website giáo dục uy tín, cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt kỹ càng, giúp bạn dễ dàng tiếp cận và nắm vững kiến thức về khí lí tưởng.
- Nguồn tài liệu phong phú: Tic.edu.vn cung cấp các bài viết, video, bài tập, đề thi liên quan đến khí lí tưởng, được biên soạn bởi đội ngũ giáo viên và chuyên gia giàu kinh nghiệm.
- Thông tin cập nhật: Tic.edu.vn luôn cập nhật những thông tin mới nhất về giáo dục, khoa học, kỹ thuật, giúp bạn nắm bắt xu hướng và kiến thức tiên tiến.
- Công cụ hỗ trợ học tập hiệu quả: Tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến như công cụ ghi chú, quản lý thời gian, giúp bạn học tập hiệu quả hơn.
- Cộng đồng học tập sôi nổi: Tic.edu.vn xây dựng một cộng đồng học tập trực tuyến, nơi bạn có thể giao lưu, học hỏi, chia sẻ kiến thức và kinh nghiệm với những người cùng đam mê.
- Giao diện thân thiện, dễ sử dụng: Tic.edu.vn được thiết kế với giao diện trực quan, dễ sử dụng, giúp bạn dễ dàng tìm kiếm và truy cập thông tin.
9. FAQ – Các Câu Hỏi Thường Gặp Về Khí Lí Tưởng
- Khí lí tưởng có tồn tại trong thực tế không?
- Không, khí lí tưởng là một mô hình lý tưởng hóa. Tuy nhiên, ở điều kiện nhiệt độ cao và áp suất thấp, khí thực có thể được coi gần đúng như khí lí tưởng.
- Hằng số khí lí tưởng R có giá trị như thế nào?
- Hằng số khí lí tưởng R có giá trị là 8,314 J/mol.K.
- Đơn vị của áp suất trong phương trình trạng thái khí lí tưởng là gì?
- Đơn vị của áp suất trong phương trình trạng thái khí lí tưởng là Pascal (Pa).
- Làm thế nào để chuyển đổi nhiệt độ từ độ Celsius sang độ Kelvin?
- Để chuyển đổi nhiệt độ từ độ Celsius sang độ Kelvin, bạn cộng thêm 273,15. Ví dụ, 25 độ C = 25 + 273,15 = 298,15 K.
- Định luật Boyle-Mariotte áp dụng cho quá trình nào?
- Định luật Boyle-Mariotte áp dụng cho quá trình đẳng nhiệt (nhiệt độ không đổi).
- Định luật Charles áp dụng cho quá trình nào?
- Định luật Charles áp dụng cho quá trình đẳng áp (áp suất không đổi).
- Định luật Gay-Lussac áp dụng cho quá trình nào?
- Định luật Gay-Lussac áp dụng cho quá trình đẳng tích (thể tích không đổi).
- Tại sao cần phải sử dụng nhiệt độ tuyệt đối (Kelvin) trong các công thức về chất khí?
- Vì nhiệt độ tuyệt đối (Kelvin) bắt đầu từ độ không tuyệt đối, đảm bảo rằng các phép tính toán về chất khí luôn cho kết quả chính xác và có ý nghĩa vật lý.
- Khí lí tưởng có tuân theo định luật bảo toàn năng lượng không?
- Có, khí lí tưởng tuân theo định luật bảo toàn năng lượng.
- Tôi có thể tìm thêm tài liệu về khí lí tưởng ở đâu trên tic.edu.vn?
- Bạn có thể tìm kiếm các bài viết, video, bài tập về khí lí tưởng trên tic.edu.vn bằng cách sử dụng công cụ tìm kiếm trên trang web hoặc truy cập vào danh mục Vật lý.
10. Lời Kêu Gọi Hành Động (CTA)
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy về khí lí tưởng? Bạn mất thời gian để tổng hợp thông tin từ nhiều nguồn khác nhau? Bạn cần các công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Bạn mong muốn kết nối với cộng đồng học tập để trao đổi kiến thức và kinh nghiệm?
Hãy truy cập ngay tic.edu.vn để khám phá nguồn tài liệu học tập phong phú, đa dạng và được kiểm duyệt kỹ càng về khí lí tưởng và các chủ đề khoa học khác! Tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả, giúp bạn học tập một cách dễ dàng và thú vị. Tham gia cộng đồng học tập sôi nổi của tic.edu.vn để giao lưu, học hỏi và chia sẻ kiến thức với những người cùng đam mê.
Đừng bỏ lỡ cơ hội nâng cao kiến thức và kỹ năng của bạn với tic.edu.vn!
Thông tin liên hệ:
- Email: tic.edu@gmail.com
- Website: tic.edu.vn
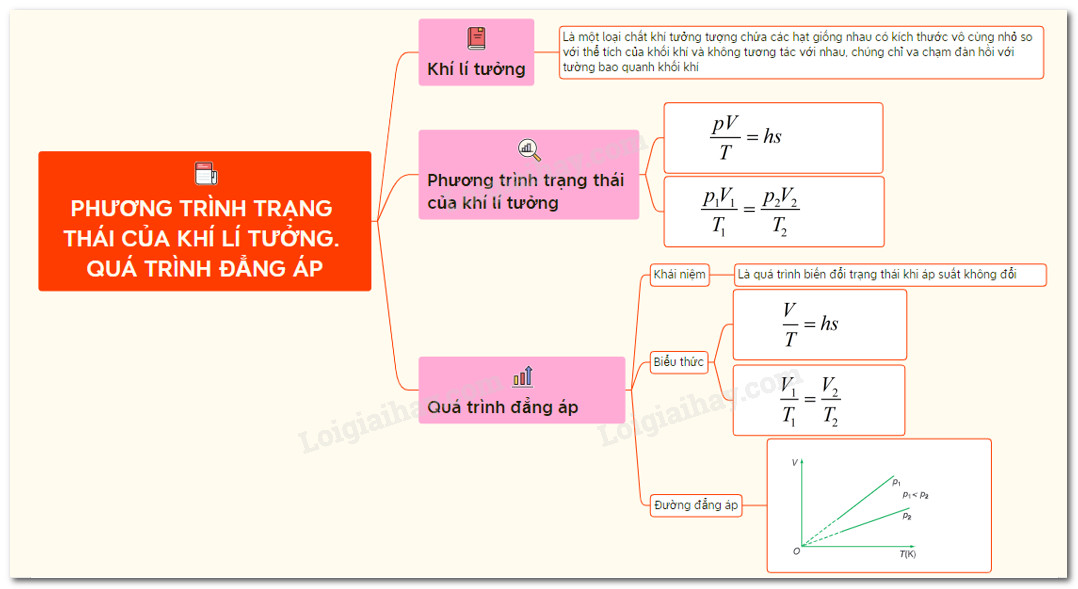
Alt text: Sơ đồ tư duy tóm tắt các công thức và khái niệm quan trọng về phương trình trạng thái khí lí tưởng.
Hãy để tic.edu.vn trở thành người bạn đồng hành trên con đường chinh phục tri thức!