
Hóa Hữu Cơ, lĩnh vực nghiên cứu các hợp chất của cacbon, đóng vai trò then chốt trong nhiều ngành khoa học và công nghiệp. Hãy cùng tic.edu.vn khám phá thế giới hóa học kỳ diệu này, từ những khái niệm cơ bản đến ứng dụng thực tiễn, giúp bạn nắm vững kiến thức và chinh phục mọi bài tập.
Contents
- 1. Hóa Hữu Cơ Là Gì?
- 1.1. Đặc Điểm Cấu Tạo Của Hợp Chất Hữu Cơ?
- 1.2. Tính Chất Vật Lý Của Hợp Chất Hữu Cơ Là Gì?
- 1.3. Tính Chất Hóa Học Của Hợp Chất Hữu Cơ Là Gì?
- 2. Phân Loại Và Gọi Tên Hợp Chất Hữu Cơ
- 2.1. Hợp Chất Hữu Cơ Được Phân Loại Như Thế Nào?
- 2.2. Cách Gọi Tên Hợp Chất Hữu Cơ Theo IUPAC Như Thế Nào?
- 2.3. Tên Thông Thường Của Hợp Chất Hữu Cơ Được Gọi Như Thế Nào?
- 3. Công Thức Phân Tử Của Hợp Chất Hữu Cơ
- 3.1. Công Thức Tổng Quát (CTTQ) Cho Biết Điều Gì?
- 3.2. Công Thức Đơn Giản Nhất (CTĐGN) Là Gì?
- 3.2.1. Cách Thiết Lập CTĐGN Như Thế Nào?
- 3.2.2. Công Thức Thực Nghiệm (CTTN) Được Xác Định Như Thế Nào?
- 3.3. Công Thức Phân Tử (CTPT) Là Gì?
- 3.3.1. Các Phương Pháp Thiết Lập CTPT?
- 4. Phân Tích Nguyên Tố Trong Hợp Chất Hữu Cơ
- 4.1. Phân Tích Định Tính Để Làm Gì?
- 4.2. Phân Tích Định Lượng Để Làm Gì?
- 5. Hiện Tượng Đồng Đẳng Và Đồng Phân
- 5.1. Đồng Đẳng Là Gì?
- 5.2. Đồng Phân Là Gì?
- 6. Liên Kết Hóa Học Và Các Phản Ứng Hóa Hữu Cơ
- 6.1. Các Loại Liên Kết Hóa Học Trong Hợp Chất Hữu Cơ?
- 6.2. Các Loại Phản Ứng Hóa Hữu Cơ Cơ Bản?
- 7. Lý Thuyết Hóa Hữu Cơ: Hiđrocacbon
- 7.1. Ankan Là Gì?
- 7.2. Anken Là Gì?
- 7.3. Ankin Là Gì?
- 7.4. Ankađien Là Gì?
- 7.5. Dãy Đồng Đẳng Benzen Là Gì?
- Bạn Gặp Khó Khăn Trong Học Hóa Hữu Cơ? tic.edu.vn Sẵn Sàng Hỗ Trợ!
- Câu Hỏi Thường Gặp Về Hóa Hữu Cơ
1. Hóa Hữu Cơ Là Gì?
Hóa hữu cơ là ngành hóa học chuyên nghiên cứu về cấu trúc, tính chất, thành phần, phản ứng và điều chế các hợp chất chứa cacbon, ngoại trừ một số hợp chất đơn giản như CO, CO2, HCN, muối cacbonat, xianua và cacbua. Theo nghiên cứu của Đại học Illinois Urbana-Champaign từ Khoa Hóa học, vào ngày 15 tháng 3 năm 2023, hóa hữu cơ cung cấp nền tảng cho sự phát triển của dược phẩm, polyme và nhiều vật liệu khác.
1.1. Đặc Điểm Cấu Tạo Của Hợp Chất Hữu Cơ?
Hợp chất hữu cơ có những đặc điểm cấu tạo riêng biệt, giúp phân biệt chúng với hợp chất vô cơ:
- Cacbon là nguyên tố bắt buộc: Mọi hợp chất hữu cơ đều chứa nguyên tử cacbon (C). Các nguyên tử C này liên kết với nhau tạo thành mạch, đồng thời liên kết với các nguyên tố khác như hydro (H), oxy (O), nitơ (N), đôi khi cả lưu huỳnh (S) và photpho (P).
- Liên kết cộng hóa trị chiếm ưu thế: Liên kết hóa học trong hợp chất hữu cơ chủ yếu là liên kết cộng hóa trị, do đó các phản ứng thường diễn ra chậm, không hoàn toàn và theo nhiều hướng khác nhau.
- Số lượng hợp chất khổng lồ: Số lượng hợp chất hữu cơ rất lớn, ước tính khoảng 10 triệu chất, vượt xa số lượng các hợp chất vô cơ (khoảng 100.000 chất).
1.2. Tính Chất Vật Lý Của Hợp Chất Hữu Cơ Là Gì?
Hợp chất hữu cơ thường có những tính chất vật lý đặc trưng sau:
- Dễ bay hơi: Nhiệt độ nóng chảy và nhiệt độ sôi thường thấp.
- Kém bền nhiệt: Dễ bị phân hủy hoặc cháy ở nhiệt độ cao.
- Khả năng hòa tan: Đa số không tan trong nước nhưng tan tốt trong các dung môi hữu cơ như benzen, ete.
1.3. Tính Chất Hóa Học Của Hợp Chất Hữu Cơ Là Gì?
Tính chất hóa học của hợp chất hữu cơ cũng có những điểm khác biệt so với hợp chất vô cơ:
- Phản ứng chậm: Hầu hết các phản ứng diễn ra chậm, không hoàn toàn và theo nhiều hướng, tạo ra hỗn hợp sản phẩm.
- Phản ứng đa dạng: Tham gia vào nhiều loại phản ứng khác nhau như phản ứng thế, cộng, tách, oxi hóa khử.
2. Phân Loại Và Gọi Tên Hợp Chất Hữu Cơ
Việc phân loại và gọi tên hợp chất hữu cơ một cách chính xác giúp chúng ta dễ dàng nghiên cứu, trao đổi thông tin và ứng dụng chúng trong thực tế.
2.1. Hợp Chất Hữu Cơ Được Phân Loại Như Thế Nào?
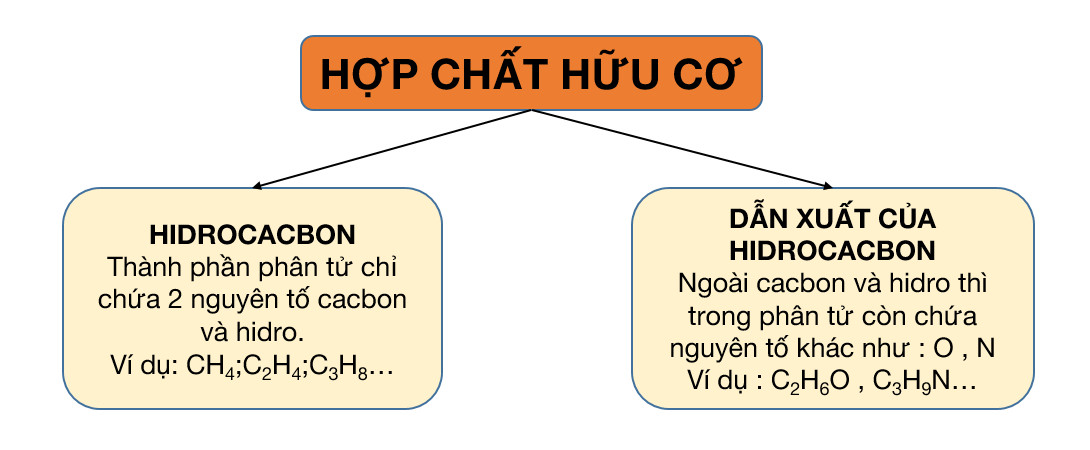
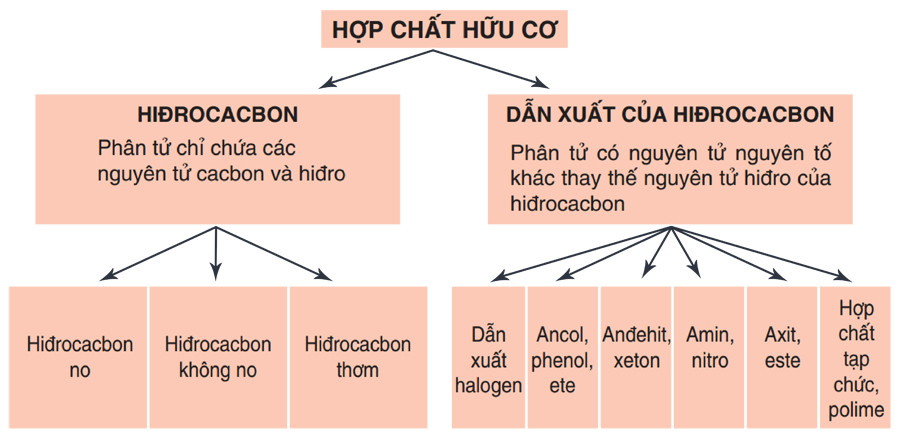
Hợp chất hữu cơ được phân loại theo nhiều cách khác nhau, trong đó phổ biến nhất là dựa vào thành phần nguyên tố và cấu trúc mạch cacbon:
- Theo thành phần nguyên tố:
- Hiđrocacbon: Chỉ chứa hai nguyên tố C và H.
- Hiđrocacbon no (ankan): Chỉ có liên kết đơn (ví dụ: CH4, C2H6).
- Hiđrocacbon không no (anken, ankin, ankađien): Có liên kết đôi, liên kết ba (ví dụ: C2H4, C2H2).
- Hiđrocacbon thơm (aren): Có vòng benzen (ví dụ: C6H6, C7H8).
- Dẫn xuất hiđrocacbon: Chứa thêm các nguyên tố khác như O, N, halogen (Cl, Br), S, P (ví dụ: CH3Cl, C2H5OH, CH3COOH).
- Hiđrocacbon: Chỉ chứa hai nguyên tố C và H.
- Theo cấu trúc mạch cacbon:
- Mạch hở (aliphatic):
- Mạch thẳng: Các nguyên tử C liên kết với nhau thành một đường thẳng.
- Mạch nhánh: Có các nhánh cacbon gắn vào mạch chính.
- Mạch vòng (cyclic):
- Đồng vòng (carbocyclic): Chỉ chứa các nguyên tử C trong vòng.
- Dị vòng (heterocyclic): Chứa các nguyên tử khác (O, N, S…) trong vòng.
- Mạch hở (aliphatic):
2.2. Cách Gọi Tên Hợp Chất Hữu Cơ Theo IUPAC Như Thế Nào?
Danh pháp IUPAC (International Union of Pure and Applied Chemistry) là hệ thống tên gọi quốc tế được sử dụng rộng rãi trong hóa học. Có hai loại tên gọi chính theo IUPAC:
- Tên gốc – chức: Tên phần gốc + tên phần định chức (ví dụ: etyl clorua).
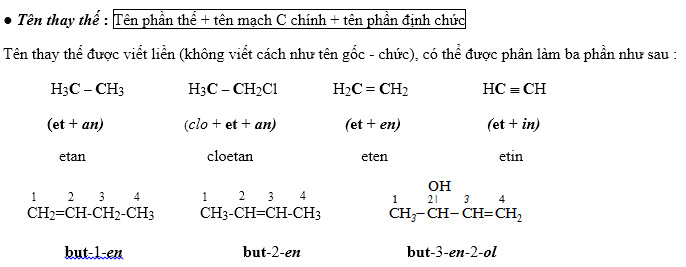
- Tên thay thế: Tên phần thế + tên mạch C chính + tên phần định chức (ví dụ: 2-clorobutan).
Để gọi tên chính xác, bạn cần nắm vững:
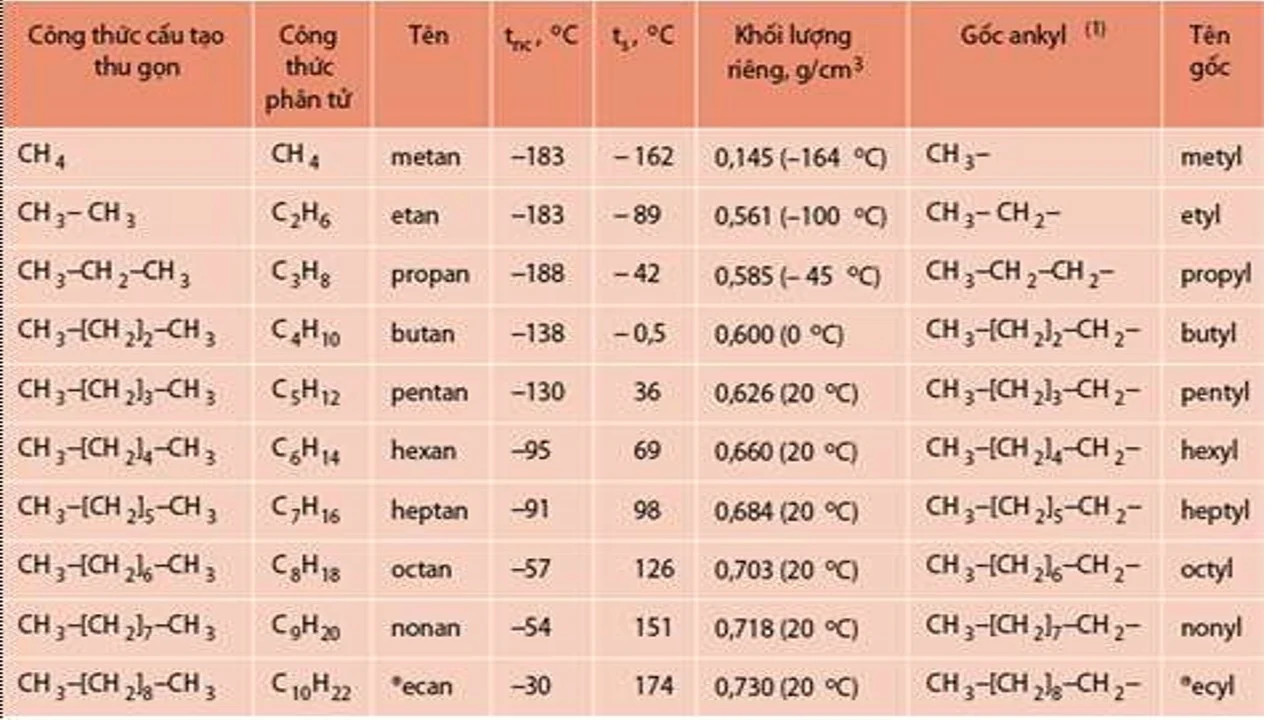
- Tên các số đếm: mono (1), di (2), tri (3), tetra (4), penta (5), hexa (6), hepta (7), octa (8), nona (9), deca (10).
- Tên mạch cacbon chính: met (1C), et (2C), prop (3C), but (4C), pent (5C), hex (6C), hep (7C), oct (8C), non (9C), dec (10C).
- Tên các gốc hiđrocacbon: Tên mạch cacbon + “yl” (ví dụ: CH3- metyl, C2H5- etyl). Một số gốc đặc biệt: vinyl (CH2=CH-), anlyl (CH2=CH-CH2-).
2.3. Tên Thông Thường Của Hợp Chất Hữu Cơ Được Gọi Như Thế Nào?
Tên thông thường (tên thường) thường xuất phát từ nguồn gốc hoặc tính chất của hợp chất. Ví dụ:
- HCOOH: axit fomic (từ formica nghĩa là kiến).
- CH3COOH: axit axetic (từ acetus nghĩa là giấm).
- C10H20O: mentol (từ mentha piperita nghĩa là bạc hà).
3. Công Thức Phân Tử Của Hợp Chất Hữu Cơ
Công thức phân tử cho biết thông tin quan trọng về thành phần và cấu trúc của hợp chất hữu cơ.
3.1. Công Thức Tổng Quát (CTTQ) Cho Biết Điều Gì?
CTTQ cho biết các nguyên tố có trong phân tử hợp chất hữu cơ. Ví dụ, CTTQ CxHyOzNt cho biết hợp chất này được tạo thành từ C, H, O và N.
3.2. Công Thức Đơn Giản Nhất (CTĐGN) Là Gì?
CTĐGN là công thức biểu thị tỉ lệ tối giản về số nguyên tử của các nguyên tố trong phân tử.
3.2.1. Cách Thiết Lập CTĐGN Như Thế Nào?
Để thiết lập CTĐGN của CxHyOzNt, ta thiết lập tỉ lệ:
x : y : z : t = (mC/12) : (mH/1) : (mO/16) : (mN/14)
hoặc
x : y : z : t = (%mC/12) : (%mH/1) : (%mO/16) : (%mN/14)
3.2.2. Công Thức Thực Nghiệm (CTTN) Được Xác Định Như Thế Nào?
CTTN = (CTĐGN)n, trong đó n là số nguyên dương. Xác định n để tìm CTTN.
3.3. Công Thức Phân Tử (CTPT) Là Gì?
CTPT cho biết số lượng nguyên tử của mỗi nguyên tố trong phân tử.
3.3.1. Các Phương Pháp Thiết Lập CTPT?
Có ba cách chính để thiết lập CTPT:
- Cách 1: Dựa vào thành phần % khối lượng các nguyên tố.
Cho CTPT CxHyOz, ta có tỉ lệ:
M/100 = 12x/%mC = y/%mH = 16z/%mO
Từ đó:
x = M.%mC/(12.100); y = M.%mH/(1.100); z = M.%mO/(16.100);
- Cách 2: Dựa vào CTĐGN.
Bước 1: Đặt CTPT là (CTĐGN)n (n ∈ N).
Bước 2: Tính độ bất bão hòa (k) của phân tử (chỉ áp dụng cho hợp chất hữu cơ có liên kết cộng hóa trị).
Bước 3: Dựa vào biểu thức k để chọn giá trị n, từ đó tìm ra CTPT.
Độ bất bão hòa (k) là tổng số liên kết π và vòng trong phân tử.
Công thức tính: k = (2x + 2 + t – y)/2 (với CxHyOzNt)
- Cách 3: Tính trực tiếp theo khối lượng sản phẩm cháy.
Phương trình phản ứng cháy:
CxHyOzNt + (x + y/4 – z/2) O2 → xCO2 + (y/2)H2O + (t/2)N2
Áp dụng định luật bảo toàn nguyên tố: nC = nCO2; nH = 2nH2O; nN = 2nN2
Áp dụng định luật bảo toàn khối lượng: mHCHC = mC + mH + mO + mN + …
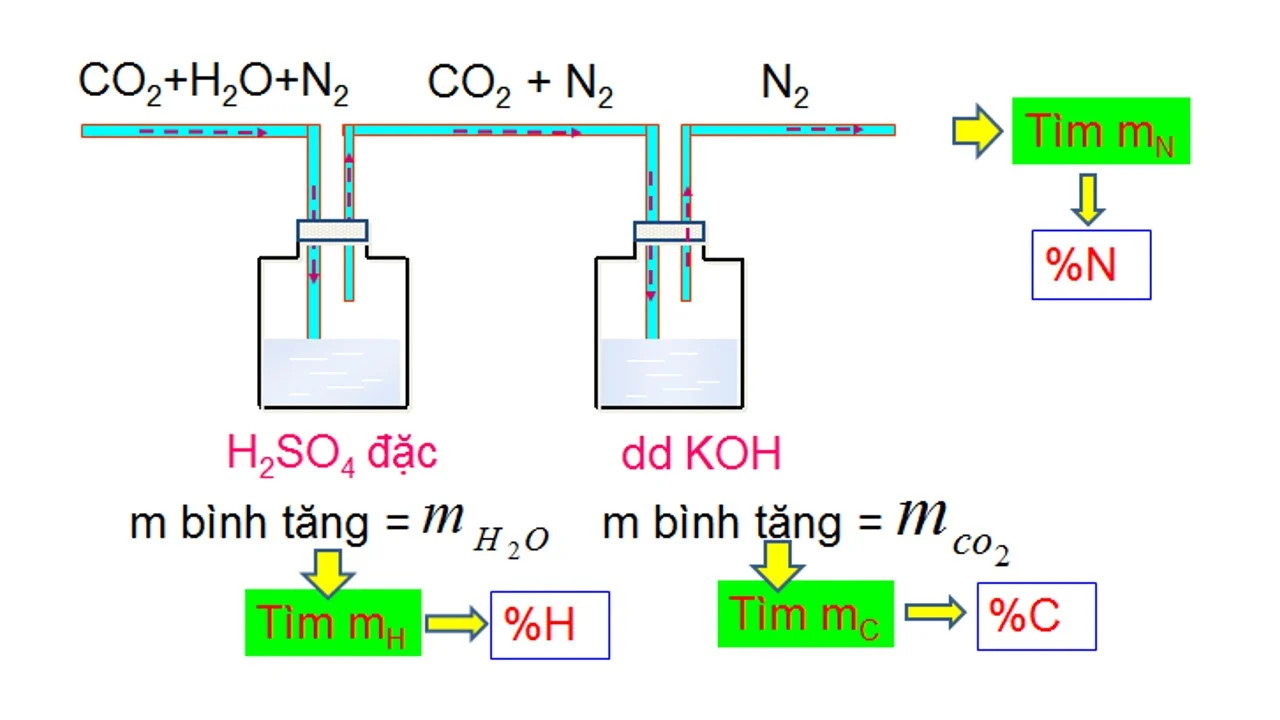
Sản phẩm cháy CO2, H2O,… được hấp thụ vào các bình:
- Bình đựng chất hút nước (H2SO4 đặc, P2O5, muối khan): khối lượng bình tăng = khối lượng nước.
- Bình đựng dung dịch bazơ: khối lượng bình tăng = khối lượng CO2.
Trường hợp cho hỗn hợp CO2 và H2O vào bình đựng nước vôi trong hoặc Ba(OH)2:
- Khối lượng bình tăng: m↑ = mCO2 + mH2O
- Khối lượng dung dịch tăng: mdd↑ = (mCO2 + mH2O) – mkết tủa
- Khối lượng dung dịch giảm: mdd↓ = mkết tủa – (mCO2 + mH2O)
4. Phân Tích Nguyên Tố Trong Hợp Chất Hữu Cơ
Phân tích nguyên tố giúp xác định thành phần và hàm lượng các nguyên tố trong hợp chất hữu cơ.
4.1. Phân Tích Định Tính Để Làm Gì?
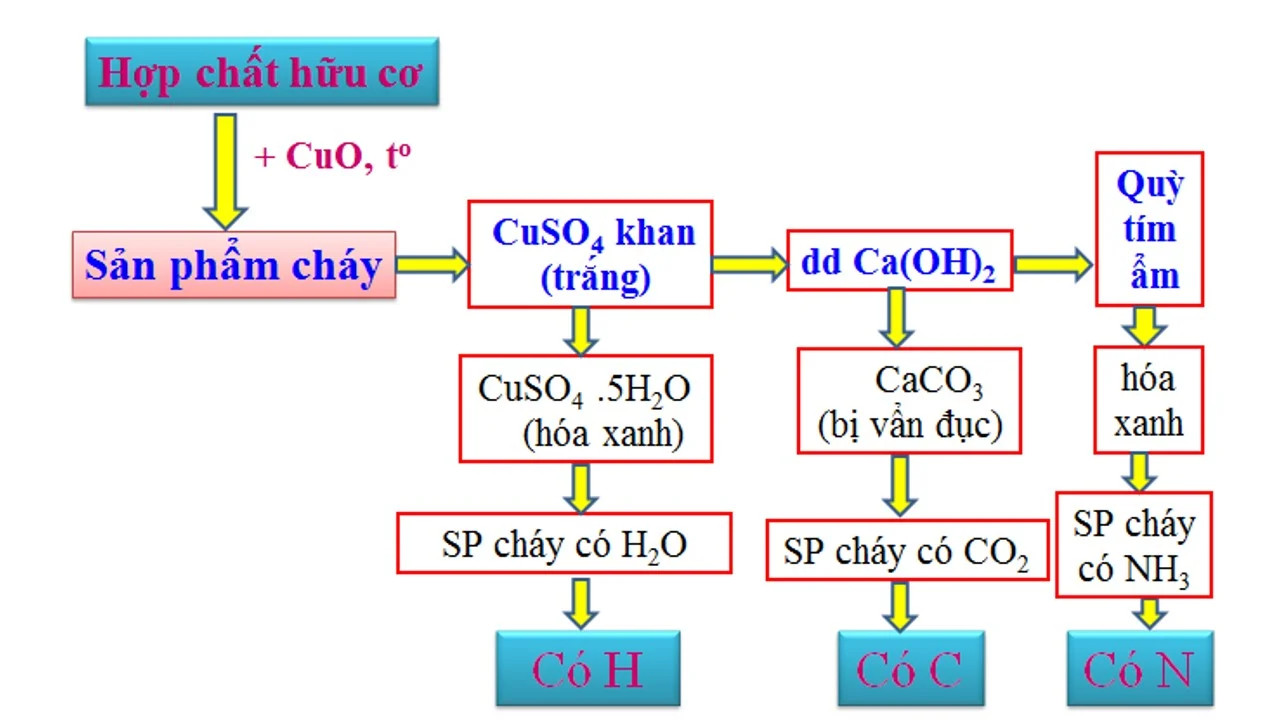
Mục đích của phân tích định tính là xác định các nguyên tố có mặt trong hợp chất hữu cơ. Nguyên tắc là chuyển các nguyên tố thành các chất vô cơ đơn giản, sau đó nhận biết chúng bằng các phản ứng đặc trưng.
4.2. Phân Tích Định Lượng Để Làm Gì?
Mục đích của phân tích định lượng là xác định thành phần % về khối lượng của các nguyên tố trong hợp chất hữu cơ.
Nguyên tắc: Cân chính xác khối lượng hợp chất hữu cơ, chuyển C thành CO2, H thành H2O, N thành N2, rồi xác định chính xác khối lượng hoặc thể tích của các chất tạo thành. Từ đó tính được % khối lượng các nguyên tố.
Xác định khối lượng mol phân tử:
- Dựa vào tỉ khối của chất hữu cơ so với không khí hoặc so với H2: MA = 29.dA/KK hoặc MA = 2.dA/H2
- Các chất khó bay hơi hoặc không bay hơi được xác định bằng phương pháp nghiệm lạnh hoặc nghiệm sôi.
5. Hiện Tượng Đồng Đẳng Và Đồng Phân
Đồng đẳng và đồng phân là hai khái niệm quan trọng trong hóa hữu cơ, giúp giải thích sự đa dạng của các hợp chất.
5.1. Đồng Đẳng Là Gì?
Những hợp chất hữu cơ có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hóa học tương tự nhau được gọi là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
Ví dụ: Dãy ankan CH4, C2H6, C3H8, C4H10, C5H12,… (CnH2n+2), mỗi chất hơn chất liền trước 1 nhóm CH2 và có tính chất hóa học tương tự nhau.
5.2. Đồng Phân Là Gì?
Những hợp chất có cấu tạo khác nhau nhưng có chung công thức phân tử gọi là những chất đồng phân.
Ví dụ: Etanol (C2H5OH) và đimetyl ete (CH3OCH3) có cùng công thức phân tử C2H6O nhưng cấu tạo và tính chất khác nhau.
6. Liên Kết Hóa Học Và Các Phản Ứng Hóa Hữu Cơ
Liên kết hóa học và các phản ứng hóa hữu cơ là nền tảng để hiểu và dự đoán tính chất của các hợp chất.
6.1. Các Loại Liên Kết Hóa Học Trong Hợp Chất Hữu Cơ?
- Liên kết σ (sigma): Liên kết đơn, được tạo bởi 1 cặp electron dùng chung.
- Liên kết π (pi): Liên kết bội (đôi, ba). Liên kết đôi gồm 1 liên kết σ và 1 liên kết π, liên kết ba gồm 1 liên kết σ và 2 liên kết π.
6.2. Các Loại Phản Ứng Hóa Hữu Cơ Cơ Bản?
- Phản ứng thế: Nguyên tử hoặc nhóm nguyên tử trong phân tử bị thay thế bởi nguyên tử hoặc nhóm nguyên tử khác.
- Bẻ gãy liên kết C-H: Ưu tiên C bậc cao.
- Bẻ gãy liên kết C-C (cracking): CnH2n+2 → CaH2a+2 + CbH2b (n = a + b).
- Phản ứng cộng: Cộng các nguyên tử hoặc nhóm nguyên tử vào liên kết π.
- Tuân theo quy tắc Markovnikov: Khi cộng HX vào anken bất đối xứng, H ưu tiên cộng vào C bậc thấp, X ưu tiên cộng vào C bậc cao.
- Phản ứng trùng hợp: Các phân tử nhỏ (monome) kết hợp với nhau tạo thành phân tử lớn (polime).
- Phản ứng thế của H linh động: H trong R-C≡CH có thể phản ứng với kim loại mạnh (Na) hoặc AgNO3/NH3 tạo kết tủa.
7. Lý Thuyết Hóa Hữu Cơ: Hiđrocacbon
Hiđrocacbon là nhóm hợp chất hữu cơ quan trọng, làm nền tảng cho nhiều hợp chất khác.
7.1. Ankan Là Gì?
Ankan (parafin) là hiđrocacbon no, mạch hở, chỉ chứa liên kết đơn.
- CTTQ: CnH2n+2 (n ≥ 1).
- Đồng phân: Đồng phân mạch C (mạch thẳng, mạch nhánh).
- Danh pháp: Số chỉ vị trí nhánh – Tên nhánh + Tên mạch chính + an.
- Tính chất hóa học:
- Phản ứng thế: Thế H bằng halogen (ưu tiên H ở C bậc cao).
- Phản ứng tách (cracking): CnH2n+2 → Ankan + Anken.
7.2. Anken Là Gì?
Anken (olefin) là hiđrocacbon không no, mạch hở, chứa một liên kết đôi.
- CTTQ: CnH2n (n ≥ 2).
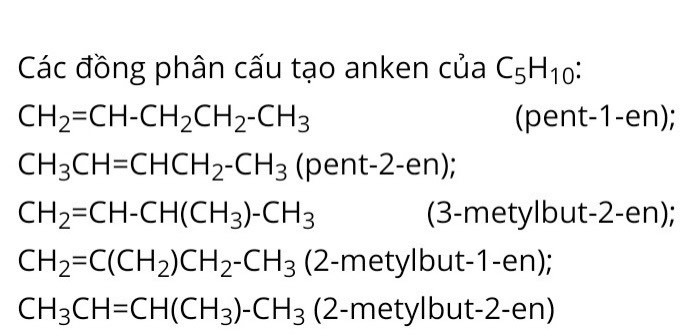
- Đồng phân: Đồng phân cấu tạo (mạch C, vị trí nối đôi), đồng phân hình học (cis, trans).
- Danh pháp: Số chỉ vị trí nhánh – Tên nhánh + Tên mạch chính – số chỉ vị trí nối đôi – en.
- Tính chất hóa học:
- Phản ứng cộng: Cộng H2 (tạo ankan), halogen (tạo dẫn xuất halogen), HX (tuân theo quy tắc Markovnikov), H2O (tạo ancol).
- Phản ứng trùng hợp: nCH2=CH2 → (-CH2-CH2-)n.
- Phản ứng oxi hóa: Làm mất màu dung dịch KMnO4, dung dịch brom.
7.3. Ankin Là Gì?
Ankin là hiđrocacbon không no, mạch hở, chứa một liên kết ba.
- CTTQ: CnH2n-2 (n ≥ 2).
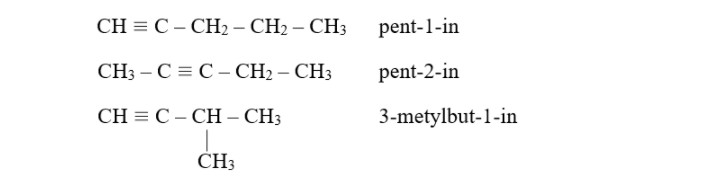
- Đồng phân: Đồng phân mạch C, vị trí nối ba.
- Danh pháp: Số chỉ vị trí nhánh – Tên nhánh + Tên mạch chính – số chỉ vị trí nối ba – in. Tên thường: axetilen, metylaxetilen,…
- Tính chất hóa học:
- Phản ứng cộng: Tương tự anken, cộng H2, halogen, HX.
- Phản ứng nhị hợp, tam hợp của axetilen.
- Phản ứng thế H linh động ở ankin-1 (R-C≡CH) với kim loại mạnh (Na) hoặc AgNO3/NH3.
- Phản ứng oxi hóa.
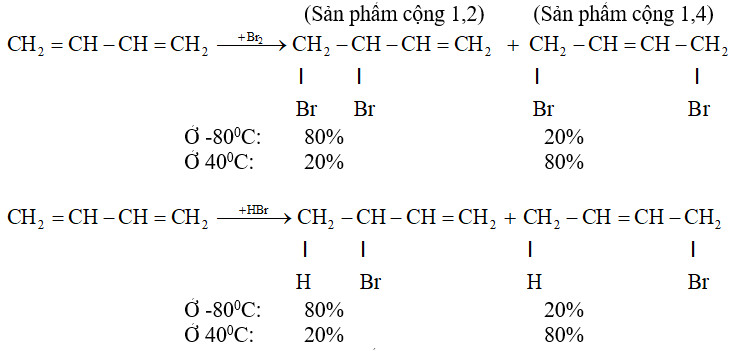
7.4. Ankađien Là Gì?
Ankađien là hiđrocacbon mạch hở chứa hai liên kết đôi.
- CTTQ: CnH2n-2 (n ≥ 3).
- Phân loại: Ankađien có hai nối đôi liên tiếp, ankađien liên hợp (hai nối đôi cách một nối đơn), ankađien có hai nối đôi cách nhau nhiều nối đơn.
- Tính chất hóa học: Tương tự anken.
- Ứng dụng: Điều chế polime (cao su).
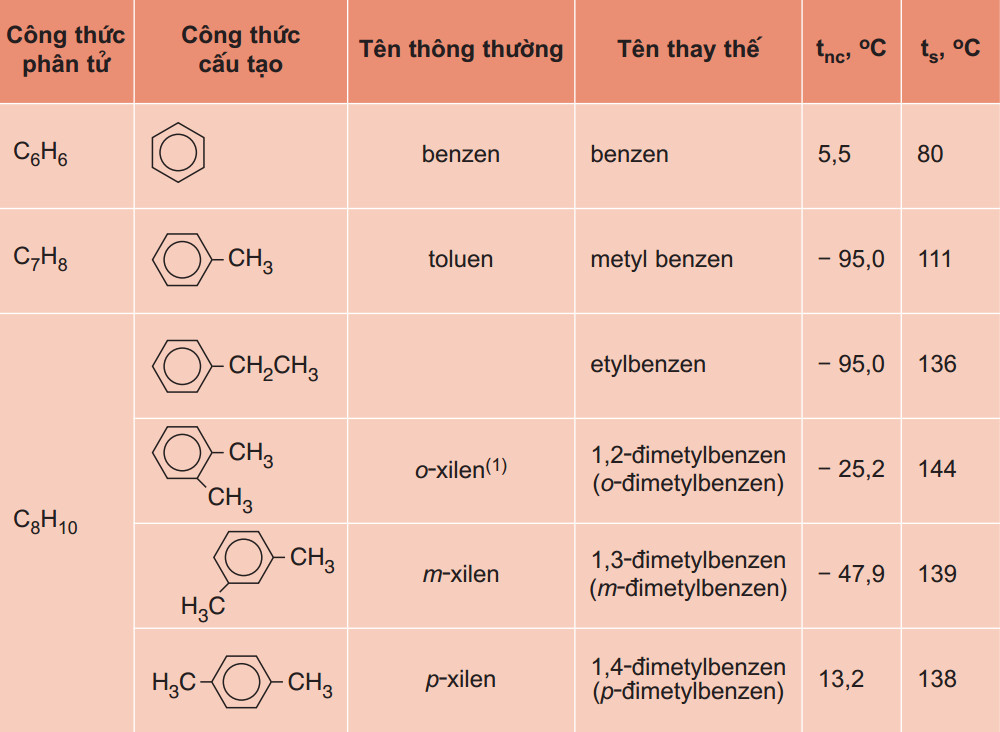
7.5. Dãy Đồng Đẳng Benzen Là Gì?
Đồng đẳng benzen là hiđrocacbon thơm chứa một vòng benzen.
- CTTQ: CnH2n-6 (n ≥ 6).
- Đồng phân: Vị trí nhóm ankyl trên vòng benzen, cấu tạo mạch C của nhánh.
- Tên gọi: Tên nhóm ankyl + benzen. Vị trí tương đối: ortho (o-), meta (m-), para (p-).
- Tính chất hóa học:
- Phản ứng thế: Thế H trên vòng benzen (xúc tác Fe) hoặc thế H ở nhánh (ánh sáng).
- Phản ứng cộng: Cộng H2 (tạo xiclohexan), Cl2 (tạo hexacloran).
- Phản ứng oxi hóa: Benzen không làm mất màu KMnO4 ở điều kiện thường, toluen làm mất màu khi đun nóng.
Bạn Gặp Khó Khăn Trong Học Hóa Hữu Cơ? tic.edu.vn Sẵn Sàng Hỗ Trợ!
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng, mất thời gian tổng hợp thông tin, cần công cụ hỗ trợ học tập hiệu quả, mong muốn kết nối với cộng đồng học tập và tìm kiếm cơ hội phát triển kỹ năng?
tic.edu.vn cung cấp nguồn tài liệu học tập đa dạng, đầy đủ, được kiểm duyệt, cập nhật thông tin giáo dục mới nhất và chính xác, cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả (ví dụ: công cụ ghi chú, quản lý thời gian), xây dựng cộng đồng học tập trực tuyến sôi nổi để người dùng có thể tương tác và học hỏi lẫn nhau, giới thiệu các khóa học và tài liệu giúp phát triển kỹ năng.
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả!
- Email: [email protected]
- Trang web: tic.edu.vn
Câu Hỏi Thường Gặp Về Hóa Hữu Cơ
-
Hóa hữu cơ khác hóa vô cơ như thế nào?
Hóa hữu cơ nghiên cứu các hợp chất chứa cacbon, trong khi hóa vô cơ nghiên cứu các hợp chất không chứa cacbon (ngoại trừ một số ít). Hợp chất hữu cơ thường có liên kết cộng hóa trị, dễ cháy, và có nhiều đồng phân hơn hợp chất vô cơ. -
Tại sao cacbon lại tạo ra nhiều hợp chất hữu cơ đến vậy?
Cacbon có khả năng tạo thành mạch dài, mạch vòng, và liên kết với nhiều nguyên tố khác nhau, tạo nên sự đa dạng về cấu trúc và tính chất. -
Đồng đẳng và đồng phân khác nhau như thế nào?
Đồng đẳng là các chất có cấu trúc tương tự, hơn kém nhau một hay nhiều nhóm CH2. Đồng phân là các chất có cùng công thức phân tử nhưng cấu trúc khác nhau. -
Quy tắc Markovnikov áp dụng cho loại phản ứng nào?
Quy tắc Markovnikov áp dụng cho phản ứng cộng HX (HCl, HBr, H2O…) vào anken bất đối xứng. Nguyên tử H ưu tiên cộng vào C bậc thấp, nguyên tử X ưu tiên cộng vào C bậc cao. -
Phản ứng nào dùng để nhận biết anken?
Phản ứng làm mất màu dung dịch brom và dung dịch KMnO4 là hai phản ứng đặc trưng để nhận biết anken. -
Ankin-1 là gì và có tính chất đặc biệt nào?
Ankin-1 là ankin có liên kết ba ở đầu mạch (R-C≡CH). H ở vị trí này có tính linh động, có thể phản ứng với kim loại mạnh hoặc dung dịch AgNO3/NH3. -
Vòng benzen có cấu trúc như thế nào?
Vòng benzen có cấu trúc phẳng, hình lục giác đều, với 6 nguyên tử cacbon liên kết xen kẽ giữa 3 liên kết đơn và 3 liên kết đôi. -
Ứng dụng của benzen trong công nghiệp là gì?
Benzen là nguyên liệu quan trọng để sản xuất nhiều hóa chất, polyme, dược phẩm, thuốc nhuộm, và dung môi. -
Làm thế nào để viết đồng phân của một hợp chất hữu cơ?
Bắt đầu bằng cách viết mạch chính dài nhất, sau đó giảm dần số nguyên tử cacbon trên mạch chính và thêm nhánh. Chú ý đến vị trí của các nhóm chức và liên kết bội. -
Tại sao cần phải học hóa hữu cơ?
Hóa hữu cơ là nền tảng của nhiều ngành khoa học và công nghiệp như y học, dược phẩm, hóa học vật liệu, nông nghiệp, và công nghệ sinh học. Hiểu biết về hóa hữu cơ giúp chúng ta giải quyết nhiều vấn đề thực tiễn và phát triển các công nghệ mới.