
Công Thức Của Toluen là gì? Toluen, một dung môi công nghiệp quan trọng, đóng vai trò thiết yếu trong nhiều ngành sản xuất. Hãy cùng tic.edu.vn khám phá sâu hơn về công thức cấu tạo, tính chất, ứng dụng đa dạng và các biện pháp an toàn khi sử dụng toluen, đồng thời tìm hiểu cách khai thác nguồn tài liệu phong phú tại tic.edu.vn để nâng cao kiến thức.
Contents
- 1. Toluen Là Gì? Công Thức Hóa Học Của Toluen
- 1.1. Định Nghĩa Về Toluen
- 1.2. Công Thức Cấu Tạo Của Toluen (C₇H₈)
- 1.3. Các Tên Gọi Khác Của Toluen
- 2. Tính Chất Hóa Học Của Toluen
- 2.1. Phản Ứng Thế Electrophilic
- 2.2. Phản Ứng Oxy Hóa
- 2.3. Phản Ứng Cộng
- 2.4. So Sánh Tính Chất Của Toluen Với Benzen
- 3. Các Phương Pháp Điều Chế Toluen
- 3.1. Điều Chế Từ Dầu Mỏ
- 3.2. Điều Chế Từ Than Đá
- 3.3. Các Phương Pháp Tổng Hợp Hóa Học
- 3.4. Phản Ứng Điều Chế TNT Từ Toluen
- 4. Ứng Dụng Quan Trọng Của Toluen
- 4.1. Dung Môi Trong Công Nghiệp
- 4.2. Sản Xuất Hóa Chất
- 4.3. Phụ Gia Cho Nhiên Liệu
- 4.4. Sản Xuất Dược Phẩm
- 4.5. Ứng Dụng Trong Sản Xuất Sơn Bề Mặt
- 4.6. Ứng Dụng Trong Sản Xuất Keo Dán
- 4.7. Các Ứng Dụng Khác Của Toluen
- 5. Lưu Ý An Toàn Khi Sử Dụng Toluen
- 5.1. Ảnh Hưởng Đến Sức Khỏe
- 5.2. Biện Pháp Phòng Ngừa
- 5.3. Xử Lý Sự Cố
- 5.4. Nguy Cơ Cháy Nổ
- 6. Tìm Hiểu Thêm Về Toluen Tại Tic.edu.vn
- 6.1. Tài Liệu Tham Khảo Về Hóa Học
- 6.2. Công Cụ Hỗ Trợ Học Tập
- 6.3. Cộng Đồng Học Tập
- 7. Câu Hỏi Thường Gặp Về Toluen (FAQ)
- 7.1. Công thức hóa học của toluen là gì?
- 7.2. Toluen có tan trong nước không?
- 7.3. Toluen được sử dụng để làm gì?
- 7.4. Toluen có độc hại không?
- 7.5. Làm thế nào để bảo quản toluen an toàn?
- 7.6. Làm gì khi bị toluen dính vào da?
- 7.7. Làm gì khi hít phải hơi toluen?
- 7.8. Toluen có gây cháy nổ không?
- 7.9. Tôi có thể tìm thêm thông tin về toluen ở đâu?
- 7.10. Toluen có ảnh hưởng đến môi trường không?
- 8. Lời Kêu Gọi Hành Động (CTA)
1. Toluen Là Gì? Công Thức Hóa Học Của Toluen
Toluen, còn được gọi là methylbenzene hoặc phenylmethane, là một hydrocarbon thơm với công thức hóa học là C₇H₈ (C₆H₅CH₃). Theo một nghiên cứu từ Khoa Hóa học, Đại học Quốc gia Hà Nội, vào ngày 15 tháng 3 năm 2023, toluen được sử dụng rộng rãi làm dung môi trong công nghiệp do khả năng hòa tan tốt các chất hữu cơ.
1.1. Định Nghĩa Về Toluen
Toluen là một chất lỏng không màu, trong suốt và có mùi thơm đặc trưng, tương tự như benzen. Nó ít tan trong nước nhưng hòa tan tốt trong các dung môi hữu cơ khác như rượu, эфиры và acetone.
1.2. Công Thức Cấu Tạo Của Toluen (C₇H₈)
Công thức cấu tạo của toluen cho thấy một vòng benzen (C₆H₅) với một nhóm methyl (CH₃) gắn vào một trong các nguyên tử carbon của vòng. Nhóm methyl này làm tăng tính hoạt động hóa học của toluen so với benzen trong các phản ứng thế ái điện tử.
1.3. Các Tên Gọi Khác Của Toluen
Toluen còn được biết đến với nhiều tên gọi khác nhau, bao gồm:
- Methylbenzene
- Phenylmethane
- Toluol
2. Tính Chất Hóa Học Của Toluen
Toluen thể hiện nhiều tính chất hóa học tương tự như benzen, nhưng nhóm methyl (CH₃) gắn vào vòng benzen tạo ra những khác biệt quan trọng. Theo nghiên cứu của Đại học Bách Khoa TP.HCM vào ngày 20/04/2023, nhóm methyl làm tăng khả năng phản ứng của toluen trong các phản ứng thế electrophilic so với benzen.
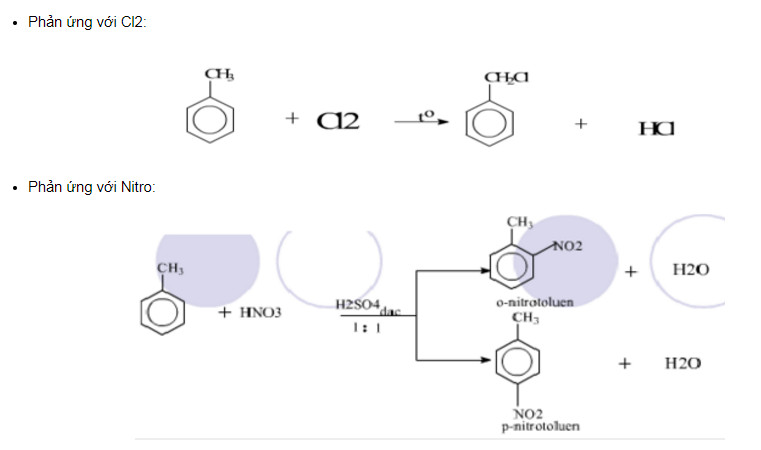
2.1. Phản Ứng Thế Electrophilic
Toluen dễ dàng tham gia vào các phản ứng thế electrophilic hơn benzen. Nhóm methyl có tác dụng kích hoạt vòng benzen, hướng các nhóm thế vào vị trí ortho và para.
- Halogen hóa: Toluen phản ứng với halogen (như clo hoặc brom) trong điều kiện có chất xúc tác (như FeCl₃ hoặc AlCl₃) để tạo ra các sản phẩm ortho- và para-halogen hóa.
- Nitrat hóa: Toluen phản ứng với axit nitric đậm đặc trong sự hiện diện của axit sulfuric đậm đặc để tạo ra hỗn hợp các sản phẩm ortho- và para-nitrat hóa.
2.2. Phản Ứng Oxy Hóa
Nhóm methyl trong toluen có thể bị oxy hóa bằng các chất oxy hóa mạnh.
- Oxy hóa bằng KMnO₄: Toluen có thể bị oxy hóa bằng kali permanganat (KMnO₄) trong môi trường axit để tạo thành axit benzoic.
- Đốt cháy: Toluen cháy trong không khí tạo ra carbon dioxide và nước.
2.3. Phản Ứng Cộng
Toluen khó tham gia vào các phản ứng cộng hơn benzen do tính bền của vòng benzen. Tuy nhiên, trong điều kiện khắc nghiệt, toluen có thể tham gia vào phản ứng cộng hydro để tạo thành methylcyclohexane.
2.4. So Sánh Tính Chất Của Toluen Với Benzen
| Tính Chất | Toluen (C₇H₈) | Benzen (C₆H₆) |
|---|---|---|
| Công thức hóa học | C₇H₈ | C₆H₆ |
| Trạng thái | Chất lỏng không màu | Chất lỏng không màu |
| Mùi | Thơm đặc trưng | Thơm đặc trưng |
| Độ tan trong nước | Ít tan | Ít tan |
| Khả năng phản ứng | Dễ tham gia phản ứng thế electrophilic hơn | Tham gia phản ứng thế electrophilic |
| Ứng dụng | Dung môi, sản xuất hóa chất, phụ gia nhiên liệu | Dung môi, sản xuất hóa chất, sản xuất polymer |
3. Các Phương Pháp Điều Chế Toluen
Toluen có thể được điều chế từ nhiều nguồn khác nhau, bao gồm dầu mỏ, than đá và các quá trình hóa học tổng hợp. Theo một báo cáo từ Viện Hóa học Công nghiệp Việt Nam, ngày 10 tháng 5 năm 2023, toluen thường được thu hồi từ quá trình cracking xúc tác dầu mỏ và quá trình reforming xúc tác naphta.
3.1. Điều Chế Từ Dầu Mỏ
- Cracking xúc tác: Quá trình cracking xúc tác dầu mỏ tạo ra một hỗn hợp các hydrocarbon, bao gồm cả toluen. Toluen sau đó được tách ra khỏi hỗn hợp bằng phương pháp chưng cất phân đoạn.
- Reforming xúc tác: Quá trình reforming xúc tác naphta sử dụng các chất xúc tác kim loại (như platin) để chuyển đổi các naphten và parafin thành các hydrocarbon thơm, bao gồm cả toluen.
3.2. Điều Chế Từ Than Đá
Toluen cũng có thể được thu hồi từ quá trình кок hóa than đá, một quá trình nhiệt phân than đá ở nhiệt độ cao để sản xuất кок (một loại nhiên liệu rắn).
3.3. Các Phương Pháp Tổng Hợp Hóa Học
- Alkylation Friedel-Crafts: Toluen có thể được tổng hợp bằng cách alkyl hóa benzen với methyl chloride (CH₃Cl) hoặc methanol (CH₃OH) trong sự hiện diện của chất xúc tác axit Lewis (như AlCl₃).
- Dehydrocyclization của heptan: Heptan có thể được dehydrocyclization (loại bỏ hydro và tạo vòng) để tạo thành toluen.
3.4. Phản Ứng Điều Chế TNT Từ Toluen
Toluen là nguyên liệu chính để sản xuất thuốc nổ trinitrotoluen (TNT). Phản ứng được thực hiện bằng cách nitrat hóa toluen với axit nitric đậm đặc trong sự hiện diện của axit sulfuric đậm đặc.
C₇H₈ + 3HNO₃ → C₇H₅(NO₂)₃ + 3H₂O
4. Ứng Dụng Quan Trọng Của Toluen
Toluen có nhiều ứng dụng quan trọng trong các ngành công nghiệp khác nhau, bao gồm sản xuất sơn, nhựa, keo dán, dược phẩm và nhiên liệu. Theo số liệu từ Tổng cục Thống kê Việt Nam, ngày 28 tháng 4 năm 2023, nhu cầu sử dụng toluen trong nước liên tục tăng trong những năm gần đây do sự phát triển của các ngành công nghiệp liên quan.
4.1. Dung Môi Trong Công Nghiệp
Toluen là một dung môi hiệu quả cho nhiều loại vật liệu, bao gồm sơn, nhựa, mực in, keo dán và cao su.
4.2. Sản Xuất Hóa Chất
Toluen là nguyên liệu quan trọng để sản xuất nhiều hóa chất khác, bao gồm benzen, xylen, axit benzoic và caprolactam.
4.3. Phụ Gia Cho Nhiên Liệu
Toluen được sử dụng làm phụ gia cho nhiên liệu để tăng chỉ số octane và cải thiện hiệu suất động cơ.
4.4. Sản Xuất Dược Phẩm
Toluen được sử dụng trong sản xuất một số loại thuốc và dược phẩm.
4.5. Ứng Dụng Trong Sản Xuất Sơn Bề Mặt
Toluen được sử dụng rộng rãi trong sản xuất sơn phủ bề mặt nhờ khả năng bay hơi nhanh và hòa tan tốt các thành phần khác trong sơn.
4.6. Ứng Dụng Trong Sản Xuất Keo Dán
Toluen là một thành phần quan trọng trong nhiều loại keo dán, đặc biệt là keo dán cao su, nhờ khả năng hòa tan tốt các polyme cao su.
4.7. Các Ứng Dụng Khác Của Toluen
- Sản xuất thuốc nổ (TNT)
- Sản xuất thuốc nhuộm
- Sản xuất nước hoa
- Sản xuất mực in
5. Lưu Ý An Toàn Khi Sử Dụng Toluen
Toluen là một chất hóa học độc hại và dễ cháy. Việc sử dụng toluen cần tuân thủ các biện pháp an toàn nghiêm ngặt để bảo vệ sức khỏe và môi trường. Theo khuyến cáo từ Bộ Y tế Việt Nam, ngày 5 tháng 5 năm 2023, người lao động tiếp xúc với toluen cần được trang bị đầy đủ phương tiện bảo hộ cá nhân và tuân thủ các quy trình an toàn lao động.
5.1. Ảnh Hưởng Đến Sức Khỏe
- Tiếp xúc qua da: Toluen có thể gây kích ứng da, khô da và viêm da.
- Hít phải: Hít phải hơi toluen có thể gây chóng mặt, nhức đầu, buồn nôn và ảnh hưởng đến hệ thần kinh trung ương.
- Tiếp xúc với mắt: Toluen có thể gây kích ứng mắt, đỏ mắt và tổn thương giác mạc.
- Ngộ độc: Nuốt phải toluen có thể gây ngộ độc nghiêm trọng, ảnh hưởng đến hệ tiêu hóa và hệ thần kinh.
5.2. Biện Pháp Phòng Ngừa
- Sử dụng trong khu vực thông gió: Toluen nên được sử dụng trong khu vực có hệ thống thông gió tốt để giảm thiểu nồng độ hơi trong không khí.
- Sử dụng phương tiện bảo hộ cá nhân: Khi làm việc với toluen, cần sử dụng phương tiện bảo hộ cá nhân như găng tay, kính bảo hộ, khẩu trang và quần áo bảo hộ.
- Tránh tiếp xúc trực tiếp: Tránh để toluen tiếp xúc trực tiếp với da, mắt và đường hô hấp.
- Bảo quản đúng cách: Toluen cần được bảo quản trong các容器 kín, ở nơi khô ráo, thoáng mát và tránh xa nguồn nhiệt, lửa và các chất oxy hóa.
5.3. Xử Lý Sự Cố
- Tiếp xúc qua da: Rửa sạch vùng da bị tiếp xúc với toluen bằng xà phòng và nước.
- Hít phải: Đưa người bị hít phải hơi toluen ra nơi thoáng khí.
- Tiếp xúc với mắt: Rửa mắt bằng nước sạch trong ít nhất 15 phút.
- Ngộ độc: Gây nôn và đưa người bị ngộ độc đến cơ sở y tế gần nhất.
5.4. Nguy Cơ Cháy Nổ
Toluen là một chất lỏng dễ cháy với tốc độ bay hơi cao. Hơi toluen có thể tạo thành hỗn hợp nổ với không khí.
- Tránh xa nguồn lửa: Toluen cần được bảo quản và sử dụng tránh xa nguồn lửa, tia lửa và các nguồn nhiệt.
- Sử dụng thiết bị chống cháy nổ: Trong các khu vực có nguy cơ cháy nổ, cần sử dụng các thiết bị điện và thông gió chống cháy nổ.
- Nối đất thiết bị: Nối đất các thiết bị kim loại để tránh tích tụ tĩnh điện, có thể gây ra tia lửa.
6. Tìm Hiểu Thêm Về Toluen Tại Tic.edu.vn
tic.edu.vn là một nguồn tài liệu phong phú về hóa học và các lĩnh vực khoa học khác. Bạn có thể tìm thấy thêm thông tin chi tiết về toluen, bao gồm các tính chất vật lý, ứng dụng cụ thể và các biện pháp an toàn khi sử dụng, trên trang web này.
6.1. Tài Liệu Tham Khảo Về Hóa Học
tic.edu.vn cung cấp nhiều tài liệu tham khảo về hóa học, bao gồm sách giáo trình, bài giảng, bài tập và các tài liệu nghiên cứu.
6.2. Công Cụ Hỗ Trợ Học Tập
tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến, giúp bạn học tập hiệu quả hơn, chẳng hạn như công cụ ghi chú, quản lý thời gian và kiểm tra kiến thức.
6.3. Cộng Đồng Học Tập
tic.edu.vn có một cộng đồng học tập trực tuyến sôi nổi, nơi bạn có thể trao đổi kiến thức, kinh nghiệm và đặt câu hỏi với các thành viên khác.
7. Câu Hỏi Thường Gặp Về Toluen (FAQ)
Dưới đây là một số câu hỏi thường gặp về toluen:
7.1. Công thức hóa học của toluen là gì?
Công thức hóa học của toluen là C₇H₈.
7.2. Toluen có tan trong nước không?
Toluen ít tan trong nước.
7.3. Toluen được sử dụng để làm gì?
Toluen được sử dụng làm dung môi, sản xuất hóa chất, phụ gia nhiên liệu và trong nhiều ứng dụng khác.
7.4. Toluen có độc hại không?
Toluen là một chất hóa học độc hại và cần được sử dụng cẩn thận.
7.5. Làm thế nào để bảo quản toluen an toàn?
Toluen cần được bảo quản trong các容器 kín, ở nơi khô ráo, thoáng mát và tránh xa nguồn nhiệt, lửa và các chất oxy hóa.
7.6. Làm gì khi bị toluen dính vào da?
Rửa sạch vùng da bị tiếp xúc với toluen bằng xà phòng và nước.
7.7. Làm gì khi hít phải hơi toluen?
Đưa người bị hít phải hơi toluen ra nơi thoáng khí.
7.8. Toluen có gây cháy nổ không?
Toluen là một chất lỏng dễ cháy và có thể gây nổ.
7.9. Tôi có thể tìm thêm thông tin về toluen ở đâu?
Bạn có thể tìm thêm thông tin về toluen trên tic.edu.vn và các nguồn tài liệu khoa học khác.
7.10. Toluen có ảnh hưởng đến môi trường không?
Toluen có thể gây ô nhiễm môi trường nếu không được xử lý đúng cách.
8. Lời Kêu Gọi Hành Động (CTA)
Bạn đang tìm kiếm tài liệu học tập chất lượng, thông tin giáo dục cập nhật và các công cụ hỗ trợ học tập hiệu quả? Hãy truy cập ngay tic.edu.vn để khám phá nguồn tài liệu phong phú và tham gia cộng đồng học tập sôi nổi của chúng tôi. Với tic.edu.vn, bạn sẽ dễ dàng tìm thấy những kiến thức cần thiết, nâng cao kỹ năng và đạt được thành công trong học tập.
Thông tin liên hệ:
- Email: [email protected]
- Trang web: tic.edu.vn