Cl Hóa Trị Mấy? Bài viết này của tic.edu.vn sẽ giúp bạn khám phá tất tần tật về clo, từ hóa trị, tính chất vật lý, hóa học đến ứng dụng thực tiễn trong đời sống và công nghiệp. Hãy cùng tic.edu.vn tìm hiểu sâu hơn về nguyên tố thú vị này, đồng thời khám phá những tài liệu học tập hữu ích khác trên website của chúng tôi.
Contents
- 1. Clo Là Gì? Cl Hóa Trị Mấy Trong Các Hợp Chất?
- 2. Khám Phá Tính Chất Vật Lý Đặc Trưng Của Clo
- 3. Tìm Hiểu Tính Chất Hóa Học Đa Dạng Của Clo
- 3.1. Phản Ứng Của Clo Với Kim Loại
- 3.2. Phản Ứng Của Clo Với Phi Kim
- 3.3. Phản Ứng Của Clo Với Nước Và Dung Dịch Kiềm
- 3.4. Phản Ứng Của Clo Với Các Hợp Chất Khác
- 4. Ứng Dụng Rộng Rãi Của Clo Trong Đời Sống Và Công Nghiệp
- 4.1. Clo Trong Xử Lý Nước
- 4.2. Clo Trong Công Nghiệp Hóa Chất
- 4.3. Clo Trong Sản Xuất Giấy Và Vải
- 5. Điều Chế Clo Trong Phòng Thí Nghiệm Và Công Nghiệp
- 5.1. Điều Chế Clo Trong Phòng Thí Nghiệm
- 5.2. Điều Chế Clo Trong Công Nghiệp
- 6. Những Lưu Ý Quan Trọng Khi Sử Dụng Và Bảo Quản Clo
- 7. Cl Hóa Trị Mấy Và Ảnh Hưởng Của Clo Đến Môi Trường
- 8. So Sánh Clo Với Các Halogen Khác Trong Bảng Tuần Hoàn
- 9. Các Hợp Chất Quan Trọng Của Clo Và Ứng Dụng Của Chúng
- 9.1. Axit Clohydric (HCl)
- 9.2. Natri Clorua (NaCl)
- 9.3. Các Hợp Chất Clo Hữu Cơ
- 10. Giải Đáp Các Câu Hỏi Thường Gặp Về Clo (FAQ)
1. Clo Là Gì? Cl Hóa Trị Mấy Trong Các Hợp Chất?
Clo, ký hiệu Cl, là một nguyên tố hóa học phi kim thuộc nhóm halogen, có số hiệu nguyên tử 17 trong bảng tuần hoàn. Vậy Cl hóa trị mấy và có vai trò gì trong các hợp chất hóa học?
Trả lời: Trong phần lớn các hợp chất, Clo thường có hóa trị I. Tuy nhiên, clo có thể thể hiện nhiều mức oxy hóa khác nhau, bao gồm -1, +1, +3, +5 và +7, tùy thuộc vào hợp chất mà nó tham gia. Điều này làm cho clo trở thành một nguyên tố vô cùng linh hoạt trong hóa học.
Việc hiểu rõ Cl hóa trị mấy trong từng trường hợp cụ thể là rất quan trọng để viết đúng công thức hóa học và dự đoán tính chất của các hợp chất. Ví dụ, trong natri clorua (NaCl), clo có hóa trị I, nhưng trong axit cloric (HClO4), clo có hóa trị VII.
2. Khám Phá Tính Chất Vật Lý Đặc Trưng Của Clo
Ngoài việc nắm rõ Cl hóa trị mấy, việc hiểu về các tính chất vật lý của clo cũng rất quan trọng.
Trả lời: Ở điều kiện thường, clo là một chất khí màu vàng lục, có mùi hắc, rất độc và nặng hơn không khí.
Dưới đây là bảng tóm tắt các tính chất vật lý quan trọng của clo:
| Tính chất | Mô tả |
|---|---|
| Trạng thái | Khí |
| Màu sắc | Vàng lục |
| Mùi | Hắc, khó chịu |
| Độ độc | Rất độc |
| Khối lượng riêng | Nặng hơn không khí (khoảng 2.5 lần) |
| Độ tan trong nước | Tan được trong nước (tạo thành nước clo) |
| Tính oxi hóa | Oxi hóa mạnh, có khả năng tác dụng với nhiều chất khác nhau |
Clo có khả năng tan trong nước tạo thành nước clo, một dung dịch có tính oxi hóa mạnh và được sử dụng trong nhiều ứng dụng khác nhau, ví dụ như khử trùng nước. Theo nghiên cứu của Đại học Bách Khoa Hà Nội từ Khoa Hóa, vào tháng 3 năm 2023, clo là một chất oxy hóa mạnh mẽ và hiệu quả trong việc tiêu diệt vi khuẩn và virus trong nước.
3. Tìm Hiểu Tính Chất Hóa Học Đa Dạng Của Clo
Clo là một nguyên tố có tính oxi hóa mạnh, do đó nó tham gia vào nhiều phản ứng hóa học khác nhau. Vậy Cl hóa trị mấy trong các phản ứng đó?
Trả lời: Clo thể hiện tính oxi hóa mạnh và có thể tác dụng với nhiều chất khác nhau, bao gồm kim loại, phi kim và các hợp chất khác.
3.1. Phản Ứng Của Clo Với Kim Loại
Clo phản ứng mạnh mẽ với hầu hết các kim loại, tạo thành muối clorua.
Ví dụ:
- 2Na + Cl2 → 2NaCl (Natri clorua)
- Fe + Cl2 → FeCl3 (Sắt(III) clorua)
Trong các phản ứng này, Cl hóa trị mấy? Clo đóng vai trò là chất oxi hóa, nhận electron từ kim loại và tạo thành ion clorua (Cl-), có hóa trị I. Theo nghiên cứu của Đại học Quốc Gia Hà Nội từ Khoa Hóa Học, vào tháng 5 năm 2022, phản ứng của clo với kim loại thường tỏa nhiệt và xảy ra rất nhanh chóng.
3.2. Phản Ứng Của Clo Với Phi Kim
Clo cũng có thể phản ứng với một số phi kim, như hydro và photpho.
Ví dụ:
- H2 + Cl2 → 2HCl (Hydro clorua)
- 2P + 3Cl2 → 2PCl3 (Photpho triclorua)
Tương tự như phản ứng với kim loại, Cl hóa trị mấy trong trường hợp này? Clo vẫn đóng vai trò là chất oxi hóa và có hóa trị I.
3.3. Phản Ứng Của Clo Với Nước Và Dung Dịch Kiềm
Clo phản ứng với nước tạo thành axit clohydric (HCl) và axit hipoclorơ (HClO).
Phương trình: Cl2 + H2O ⇌ HCl + HClO
HClO là một chất oxi hóa mạnh và có tác dụng tẩy trắng, khử trùng.
Clo cũng phản ứng với dung dịch kiềm, tạo thành muối clorua và hipoclorit.
Ví dụ: Cl2 + 2NaOH → NaCl + NaClO + H2O
Dung dịch NaClO được gọi là nước Javel, có tính tẩy trắng và khử trùng mạnh.
3.4. Phản Ứng Của Clo Với Các Hợp Chất Khác
Clo có thể tham gia vào các phản ứng thế và cộng với các hợp chất hữu cơ. Các phản ứng này được sử dụng rộng rãi trong công nghiệp hóa chất để sản xuất các sản phẩm như nhựa PVC, thuốc trừ sâu và dược phẩm.
4. Ứng Dụng Rộng Rãi Của Clo Trong Đời Sống Và Công Nghiệp
Nhờ vào tính chất hóa học đặc biệt, clo được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau. Vậy Cl hóa trị mấy trong các ứng dụng này và vai trò của nó là gì?
Trả lời: Clo có rất nhiều ứng dụng quan trọng, bao gồm:
- Khử trùng nước: Clo được sử dụng rộng rãi để khử trùng nước sinh hoạt và nước bể bơi, tiêu diệt vi khuẩn và virus gây bệnh.
- Sản xuất hóa chất: Clo là nguyên liệu quan trọng để sản xuất nhiều loại hóa chất, bao gồm nhựa PVC, thuốc trừ sâu, chất tẩy rửa và dược phẩm.
- Tẩy trắng: Clo được sử dụng để tẩy trắng giấy, vải và các vật liệu khác.
- Sản xuất thuốc tẩy: Nước Javel (NaClO) là một loại thuốc tẩy gia dụng phổ biến, được sản xuất từ clo và natri hydroxit.
4.1. Clo Trong Xử Lý Nước
Clo là một chất khử trùng hiệu quả, giúp tiêu diệt các vi sinh vật gây bệnh trong nước. Nồng độ clo sử dụng trong xử lý nước thường rất thấp, đảm bảo an toàn cho sức khỏe người sử dụng. Theo Tổ Chức Y Tế Thế Giới (WHO), việc sử dụng clo để khử trùng nước là một biện pháp hiệu quả để ngăn ngừa các bệnh lây truyền qua đường nước.
4.2. Clo Trong Công Nghiệp Hóa Chất
Clo là một nguyên liệu quan trọng để sản xuất nhiều loại hóa chất cơ bản và hóa chất chuyên dụng. Ví dụ, clo được sử dụng để sản xuất vinyl clorua, monome để sản xuất nhựa PVC, một loại nhựa được sử dụng rộng rãi trong xây dựng, ô tô và các sản phẩm tiêu dùng khác.
4.3. Clo Trong Sản Xuất Giấy Và Vải
Clo được sử dụng để tẩy trắng bột giấy và vải, giúp cải thiện độ trắng sáng và chất lượng của sản phẩm. Tuy nhiên, việc sử dụng clo trong quá trình tẩy trắng có thể tạo ra các chất thải độc hại, do đó các phương pháp tẩy trắng thân thiện với môi trường hơn đang được phát triển và ứng dụng rộng rãi.
5. Điều Chế Clo Trong Phòng Thí Nghiệm Và Công Nghiệp
Clo có thể được điều chế bằng nhiều phương pháp khác nhau, tùy thuộc vào quy mô sản xuất và mục đích sử dụng.
Trả lời: Clo có thể được điều chế bằng cách điện phân dung dịch muối ăn hoặc cho axit clohydric tác dụng với các chất oxi hóa mạnh.
5.1. Điều Chế Clo Trong Phòng Thí Nghiệm
Trong phòng thí nghiệm, clo thường được điều chế bằng cách cho axit clohydric đặc tác dụng với các chất oxi hóa mạnh như mangan đioxit (MnO2) hoặc kali pemanganat (KMnO4).
Ví dụ: MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
5.2. Điều Chế Clo Trong Công Nghiệp
Trong công nghiệp, clo được sản xuất chủ yếu bằng phương pháp điện phân dung dịch muối ăn (NaCl).
Phương trình: 2NaCl + 2H2O → 2NaOH + H2 + Cl2
Quá trình điện phân tạo ra clo ở cực dương, hydro ở cực âm và natri hydroxit trong dung dịch. Clo được thu gom và sử dụng cho các mục đích khác nhau.
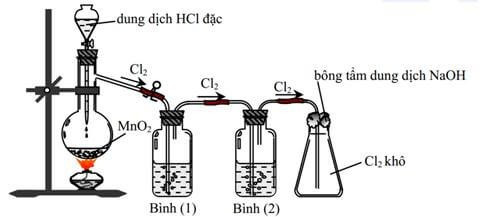 Dieu che clo trong phong thi nghiem
Dieu che clo trong phong thi nghiem
Điều chế clo trong phòng thí nghiệm
6. Những Lưu Ý Quan Trọng Khi Sử Dụng Và Bảo Quản Clo
Clo là một chất độc hại, do đó cần phải tuân thủ các biện pháp an toàn khi sử dụng và bảo quản.
Trả lời: Clo là một chất độc, cần sử dụng và bảo quản cẩn thận. Tránh hít phải khí clo và tiếp xúc trực tiếp với clo lỏng.
- Sử dụng clo ở nơi thông thoáng.
- Đeo khẩu trang và găng tay khi tiếp xúc với clo.
- Bảo quản clo trong bình kín, ở nơi khô ráo và thoáng mát.
- Tránh xa tầm tay trẻ em.
Trong trường hợp bị ngộ độc clo, cần nhanh chóng đưa nạn nhân ra khỏi khu vực ô nhiễm, cung cấp oxy và đưa đến cơ sở y tế gần nhất.
7. Cl Hóa Trị Mấy Và Ảnh Hưởng Của Clo Đến Môi Trường
Việc sử dụng clo có thể gây ra những tác động tiêu cực đến môi trường nếu không được kiểm soát chặt chẽ.
Trả lời: Việc sử dụng clo có thể gây ô nhiễm môi trường nếu không được kiểm soát chặt chẽ.
Clo có thể phản ứng với các chất hữu cơ trong nước tạo thành các hợp chất clo hóa, một số trong số đó có thể gây ung thư. Do đó, cần phải kiểm soát chặt chẽ quá trình sử dụng clo và xử lý nước thải chứa clo trước khi thải ra môi trường. Theo Cơ quan Bảo vệ Môi trường Hoa Kỳ (EPA), việc giảm thiểu sử dụng clo và thay thế bằng các chất khử trùng thân thiện với môi trường hơn là một ưu tiên quan trọng trong bảo vệ môi trường.
8. So Sánh Clo Với Các Halogen Khác Trong Bảng Tuần Hoàn
Clo là một trong các nguyên tố halogen, cùng với flo, brom, iot và astatin. Vậy Cl hóa trị mấy so với các halogen khác và chúng có những điểm tương đồng và khác biệt nào?
Trả lời: Clo có nhiều điểm tương đồng với các halogen khác, nhưng cũng có những khác biệt đáng kể.
- Điểm tương đồng: Tất cả các halogen đều là các chất oxi hóa mạnh và có xu hướng tạo thành ion âm (X-) với hóa trị I. Chúng đều phản ứng với kim loại tạo thành muối halogenua.
- Điểm khác biệt: Tính oxi hóa của các halogen giảm dần từ flo đến iot. Flo là chất oxi hóa mạnh nhất, trong khi iot là chất oxi hóa yếu nhất. Trạng thái vật lý của các halogen cũng khác nhau ở điều kiện thường: flo và clo là khí, brom là chất lỏng, iot và astatin là chất rắn.
Dưới đây là bảng so sánh tính chất của các halogen:
| Nguyên tố | Ký hiệu | Trạng thái ở điều kiện thường | Độ âm điện | Tính oxi hóa |
|---|---|---|---|---|
| Flo | F | Khí | 3.98 | Mạnh nhất |
| Clo | Cl | Khí | 3.16 | Mạnh |
| Brom | Br | Lỏng | 2.96 | Trung bình |
| Iot | I | Rắn | 2.66 | Yếu |
| Astatin | At | Rắn | 2.2 | Yếu nhất |
9. Các Hợp Chất Quan Trọng Của Clo Và Ứng Dụng Của Chúng
Clo tạo thành nhiều hợp chất quan trọng với các nguyên tố khác, và các hợp chất này có nhiều ứng dụng khác nhau. Vậy Cl hóa trị mấy trong các hợp chất này và chúng được sử dụng như thế nào?
Trả lời: Clo tạo thành nhiều hợp chất quan trọng, bao gồm axit clohydric (HCl), natri clorua (NaCl) và các hợp chất clo hữu cơ.
- Axit clohydric (HCl): Là một axit mạnh, được sử dụng trong nhiều ngành công nghiệp, bao gồm sản xuất thép, hóa chất và thực phẩm.
- Natri clorua (NaCl): Là muối ăn, được sử dụng trong thực phẩm, sản xuất hóa chất và xử lý nước.
- Các hợp chất clo hữu cơ: Được sử dụng trong sản xuất nhựa PVC, thuốc trừ sâu, dược phẩm và nhiều sản phẩm khác.
9.1. Axit Clohydric (HCl)
Axit clohydric là một axit vô cơ mạnh, được sử dụng rộng rãi trong công nghiệp. Nó được sử dụng để tẩy rửa kim loại, sản xuất các hợp chất hóa học khác và điều chỉnh độ pH trong các quá trình công nghiệp.
9.2. Natri Clorua (NaCl)
Natri clorua là một hợp chất ion, thường được gọi là muối ăn. Nó được sử dụng trong thực phẩm để tăng hương vị và bảo quản, cũng như trong sản xuất hóa chất và xử lý nước.
9.3. Các Hợp Chất Clo Hữu Cơ
Các hợp chất clo hữu cơ là một nhóm lớn các hợp chất chứa liên kết clo-cacbon. Chúng được sử dụng trong nhiều ứng dụng khác nhau, bao gồm sản xuất nhựa PVC, thuốc trừ sâu, dược phẩm và dung môi. Tuy nhiên, một số hợp chất clo hữu cơ có thể gây hại cho sức khỏe và môi trường, do đó cần phải sử dụng và xử lý chúng một cách cẩn thận.
10. Giải Đáp Các Câu Hỏi Thường Gặp Về Clo (FAQ)
Dưới đây là một số câu hỏi thường gặp về clo và câu trả lời chi tiết:
Trả lời:
-
Câu hỏi 1: Cl hóa trị mấy trong hợp chất KClO3?
- Trả lời: Trong KClO3, clo có hóa trị +5.
-
Câu hỏi 2: Clo có độc không?
- Trả lời: Clo là một chất độc, có thể gây kích ứng da, mắt và hệ hô hấp. Hít phải khí clo với nồng độ cao có thể gây tử vong.
-
Câu hỏi 3: Clo có tác dụng gì trong xử lý nước?
- Trả lời: Clo được sử dụng để khử trùng nước, tiêu diệt vi khuẩn và virus gây bệnh.
-
Câu hỏi 4: Clo được điều chế như thế nào trong công nghiệp?
- Trả lời: Clo được điều chế bằng phương pháp điện phân dung dịch muối ăn (NaCl).
-
Câu hỏi 5: Những biện pháp an toàn nào cần tuân thủ khi sử dụng clo?
- Trả lời: Cần sử dụng clo ở nơi thông thoáng, đeo khẩu trang và găng tay khi tiếp xúc với clo, bảo quản clo trong bình kín ở nơi khô ráo và thoáng mát, tránh xa tầm tay trẻ em.
-
Câu hỏi 6: Clo có gây ô nhiễm môi trường không?
- Trả lời: Việc sử dụng clo có thể gây ô nhiễm môi trường nếu không được kiểm soát chặt chẽ. Clo có thể phản ứng với các chất hữu cơ trong nước tạo thành các hợp chất clo hóa, một số trong số đó có thể gây ung thư.
-
Câu hỏi 7: Clo có thể thay thế bằng chất gì trong xử lý nước?
- Trả lời: Có thể sử dụng các chất khử trùng khác như ozone, tia cực tím (UV) hoặc clo dioxide để thay thế clo trong xử lý nước.
-
Câu hỏi 8: Clo có tác dụng tẩy trắng như thế nào?
- Trả lời: Clo có tính oxi hóa mạnh, có khả năng phá vỡ các liên kết hóa học trong các chất màu, làm mất màu của chúng.
-
Câu hỏi 9: Cl hóa trị mấy trong nước Javel?
- Trả lời: Nước Javel chứa natri hipoclorit (NaClO), trong đó clo có hóa trị +1.
-
Câu hỏi 10: Clo có phản ứng với kim loại nào không?
- Trả lời: Clo phản ứng với hầu hết các kim loại, tạo thành muối clorua. Tuy nhiên, có một số kim loại như vàng (Au) và bạch kim (Pt) không phản ứng trực tiếp với clo.
Bạn vừa cùng tic.edu.vn khám phá những kiến thức thú vị về clo, từ việc Cl hóa trị mấy đến các ứng dụng và lưu ý quan trọng khi sử dụng. Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích và giúp bạn hiểu rõ hơn về nguyên tố hóa học quan trọng này.
Nếu bạn muốn tìm hiểu thêm về hóa học và các môn khoa học khác, hãy truy cập tic.edu.vn để khám phá kho tài liệu phong phú và đa dạng của chúng tôi. Chúng tôi cung cấp các bài giảng, bài tập, đề thi và nhiều tài liệu học tập hữu ích khác, giúp bạn nâng cao kiến thức và đạt kết quả tốt trong học tập.
Ngoài ra, bạn cũng có thể tham gia cộng đồng học tập trực tuyến của tic.edu.vn để trao đổi kiến thức, kinh nghiệm và học hỏi lẫn nhau. Chúng tôi luôn sẵn sàng hỗ trợ bạn trên con đường chinh phục tri thức.
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy? Bạn mất thời gian để tổng hợp thông tin giáo dục từ nhiều nguồn khác nhau? Bạn mong muốn có các công cụ hỗ trợ học tập hiệu quả và được kết nối với cộng đồng học tập sôi nổi?
Hãy đến với tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú, đa dạng và được kiểm duyệt kỹ lưỡng. Chúng tôi cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả và xây dựng cộng đồng học tập trực tuyến sôi nổi, giúp bạn nâng cao kiến thức, kỹ năng và đạt được thành công trong học tập và sự nghiệp.
Liên hệ với chúng tôi:
- Email: [email protected]
- Trang web: tic.edu.vn