
Ankylbenzen là một hợp chất hydrocacbon thơm với vòng benzen liên kết cùng gốc hydrocacbon no, công thức chung CnH2n-6 (n ≥ 6), đóng vai trò quan trọng trong nhiều ngành công nghiệp. Bạn muốn tìm hiểu sâu hơn về ankylbenzen, từ cấu trúc, tính chất đến ứng dụng thực tế và cách học hiệu quả? Hãy cùng tic.edu.vn khám phá thế giới ankylbenzen, nơi tri thức được khơi mở và chắp cánh cho những ước mơ khoa học. Bài viết này sẽ cung cấp cho bạn cái nhìn toàn diện về ankylbenzen, giúp bạn nắm vững kiến thức và tự tin chinh phục môn Hóa học. Bên cạnh đó, chúng tôi còn giới thiệu những công cụ và tài liệu học tập hữu ích trên tic.edu.vn, hỗ trợ bạn tối đa trong quá trình học tập và nghiên cứu.
Contents
- 1. Ankylbenzen Là Gì? Định Nghĩa và Cấu Trúc
- 1.1. Giải Thích Chi Tiết Định Nghĩa Ankylbenzen
- 1.2. Công Thức Tổng Quát Của Ankylbenzen
- 1.3. Đồng Phân Của Ankylbenzen
- 1.4. Cách Gọi Tên Ankylbenzen
- 1.5. Ảnh Hưởng Của Cấu Trúc Đến Tính Chất
- 2. Tính Chất Vật Lý Đặc Trưng Của Ankylbenzen
- 2.1. Trạng Thái và Màu Sắc
- 2.2. Độ Tan
- 2.3. Mùi
- 2.4. Tính Chất Độc Hại
- 2.5. Bảng Tóm Tắt Tính Chất Vật Lý Của Một Số Ankylbenzen Tiêu Biểu
- 3. Các Phương Pháp Điều Chế Ankylbenzen Phổ Biến
- 3.1. Từ Dầu Mỏ và Nhựa Than Đá
- 3.2. Từ Ankan và Xicloankan
- 3.3. Phản Ứng Friedel-Crafts Ankyl Hóa
- 3.4. Điều Chế Etylbenzen Từ Benzen và Etilen
- 3.5. So Sánh Các Phương Pháp Điều Chế
- 4. Ứng Dụng Rộng Rãi Của Ankylbenzen Trong Đời Sống và Công Nghiệp
- 4.1. Trong Sản Xuất Dầu và Mỡ Công Nghiệp
- 4.2. Dung Môi Trong Sản Xuất Sơn và Mực In
- 4.3. Sản Xuất Thuốc Nhuộm
- 4.4. Sản Xuất Chất Tạo Màu Tổng Hợp
- 4.5. Sản Xuất Hóa Chất
- 4.6. Các Ứng Dụng Khác
- 4.7. Bảng Tóm Tắt Ứng Dụng Của Ankylbenzen
- 5. Các Câu Hỏi Thường Gặp Về Ankylbenzen (FAQ)
- 5.1. Tính Thơm Của Ankylbenzen Biểu Hiện Ở Đặc Điểm Nào?
- 5.2. Ankylbenzen + KMnO4 Cho Ra Sản Phẩm Gì?
- 5.3. Ankylbenzen + O2 Cho Ra Sản Phẩm Gì?
- 5.4. Ankylbenzen Có Gây Ô Nhiễm Môi Trường Không?
- 5.5. Làm Thế Nào Để Học Tốt Về Ankylbenzen?
- 5.6. Ankylbenzen Có Phản Ứng Với Halogen Không?
- 5.7. Ankylbenzen Có Phản Ứng Với Axit Sunfuric Đặc Không?
- 5.8. Ankylbenzen Có Tính Axit Hay Bazơ?
- 5.9. Ankylbenzen Có Tính Tan Trong Cồn Không?
- 5.10. Tại Sao Ankylbenzen Quan Trọng Trong Công Nghiệp?
- 6. Tối Ưu Hóa Quá Trình Học Tập Với Các Công Cụ Hỗ Trợ Từ Tic.edu.vn
- 6.1. Kho Tài Liệu Đa Dạng và Phong Phú
- 6.2. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
- 6.3. Cộng Đồng Học Tập Sôi Nổi
- 6.4. Ưu Điểm Vượt Trội Của Tic.edu.vn So Với Các Nguồn Tài Liệu Khác
1. Ankylbenzen Là Gì? Định Nghĩa và Cấu Trúc
Ankylbenzen là hydrocacbon thơm mà phân tử chứa một vòng benzen liên kết với gốc hydrocacbon no, tuân theo công thức chung CnH2n-6 (với n lớn hơn hoặc bằng 6). Từ C8H10 trở lên, ankylbenzen có đồng phân mạch cacbon, với các gốc hydrocacbon biến đổi quanh vòng benzen.
1.1. Giải Thích Chi Tiết Định Nghĩa Ankylbenzen
Ankylbenzen là một loại hydrocacbon thơm đặc biệt, có cấu trúc kết hợp giữa vòng benzen (một cấu trúc vòng sáu cạnh với các liên kết đôi luân phiên) và một hoặc nhiều nhóm ankyl (các nhóm alkyl là các chuỗi hydrocacbon no, ví dụ như metyl, etyl, propyl, v.v.).
1.2. Công Thức Tổng Quát Của Ankylbenzen
Công thức tổng quát của ankylbenzen là CnH2n-6, trong đó n là số nguyên tử cacbon trong phân tử và phải lớn hơn hoặc bằng 6 để đảm bảo có đủ cacbon cho cả vòng benzen và nhóm ankyl.
1.3. Đồng Phân Của Ankylbenzen
Từ C8H10 trở lên, ankylbenzen bắt đầu xuất hiện đồng phân do sự khác biệt về vị trí và cấu trúc của nhóm ankyl trên vòng benzen. Điều này tạo ra sự đa dạng lớn về tính chất và ứng dụng của các ankylbenzen khác nhau.
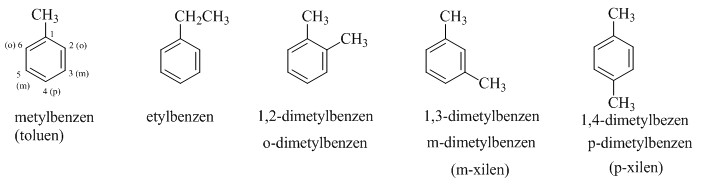
Ví dụ, đối với ankylbenzen có công thức C8H10, có các đồng phân sau:
- Etylbenzen (một nhóm etyl gắn vào vòng benzen)
- Các đồng phân xylen (hai nhóm metyl gắn vào vòng benzen ở các vị trí ortho, meta, hoặc para)
1.4. Cách Gọi Tên Ankylbenzen
Để gọi tên ankylbenzen, ta coi vòng benzen là mạch chính và các nhóm ankyl là mạch nhánh hay nhóm thế. Vị trí của các nhóm ankyl trên vòng benzen được chỉ rõ bằng các chữ cái o- (ortho-), m- (meta-), hoặc p- (para-), tương ứng với vị trí 1,2; 1,3; và 1,4 trên vòng benzen.
Ví dụ:
- o-Xylen (1,2-dimetylbenzen)
- m-Xylen (1,3-dimetylbenzen)
- p-Xylen (1,4-dimetylbenzen)
1.5. Ảnh Hưởng Của Cấu Trúc Đến Tính Chất
Cấu trúc đặc biệt của ankylbenzen, với vòng benzen ổn định và nhóm ankyl linh hoạt, tạo ra sự kết hợp độc đáo giữa tính chất thơm và tính chất no. Vòng benzen mang lại tính ổn định hóa học và khả năng tham gia vào các phản ứng thế ái điện tử, trong khi nhóm ankyl tạo ra tính kỵ nước và khả năng tham gia vào các phản ứng thế gốc tự do.
2. Tính Chất Vật Lý Đặc Trưng Của Ankylbenzen
Ankylbenzen là những hợp chất hữu cơ không màu, ít tan trong nước nhưng lại dễ dàng hòa tan trong các dung môi hữu cơ khác. Chúng có mùi đặc trưng, tuy nhiên, cần lưu ý rằng việc hít phải ankylbenzen có thể gây hại cho sức khỏe.
2.1. Trạng Thái và Màu Sắc
Ở điều kiện thường, ankylbenzen thường tồn tại ở trạng thái lỏng, không màu hoặc có màu vàng nhạt. Tuy nhiên, một số ankylbenzen có thể tồn tại ở trạng thái rắn tùy thuộc vào kích thước và cấu trúc của phân tử.
2.2. Độ Tan
Ankylbenzen là các hợp chất kỵ nước, do đó chúng ít tan trong nước. Tuy nhiên, chúng lại tan tốt trong các dung môi hữu cơ như etanol, dietyl ete, và các hydrocacbon khác.
Độ tan của ankylbenzen trong nước giảm khi kích thước của nhóm ankyl tăng lên. Điều này là do nhóm ankyl làm tăng tính kỵ nước của phân tử.
2.3. Mùi
Hầu hết các ankylbenzen đều có mùi thơm nhẹ đặc trưng. Tuy nhiên, mùi của chúng có thể gây khó chịu và thậm chí gây hại cho sức khỏe nếu hít phải ở nồng độ cao.
2.4. Tính Chất Độc Hại
Cần đặc biệt lưu ý rằng nhiều ankylbenzen là các chất độc hại. Chúng có thể gây kích ứng da, mắt và hệ hô hấp. Tiếp xúc lâu dài với ankylbenzen có thể gây ra các vấn đề sức khỏe nghiêm trọng hơn, bao gồm tổn thương gan, thận và hệ thần kinh. Do đó, cần tuân thủ các biện pháp an toàn khi làm việc với ankylbenzen, bao gồm sử dụng thiết bị bảo hộ cá nhân và đảm bảo thông gió tốt.
2.5. Bảng Tóm Tắt Tính Chất Vật Lý Của Một Số Ankylbenzen Tiêu Biểu
| Hợp chất | Công thức | Trạng thái | Màu sắc | Mùi | Độ tan trong nước |
|---|---|---|---|---|---|
| Benzen | C6H6 | Lỏng | Không màu | Thơm đặc trưng | Ít |
| Toluen | C7H8 | Lỏng | Không màu | Thơm nhẹ | Ít |
| Etylbenzen | C8H10 | Lỏng | Không màu | Thơm nhẹ | Rất ít |
| o-Xylen | C8H10 | Lỏng | Không màu | Thơm nhẹ | Rất ít |
| m-Xylen | C8H10 | Lỏng | Không màu | Thơm nhẹ | Rất ít |
| p-Xylen | C8H10 | Lỏng | Không màu | Thơm nhẹ | Rất ít |
3. Các Phương Pháp Điều Chế Ankylbenzen Phổ Biến
Ankylbenzen có thể được điều chế từ nhiều nguồn khác nhau, bao gồm chưng cất dầu mỏ, nhựa than đá, và từ các ankan hoặc xicloankan. Một phương pháp phổ biến để điều chế etylbenzen là từ benzen và etilen.
3.1. Từ Dầu Mỏ và Nhựa Than Đá
Benzen, toluen, xylen và các ankylbenzen khác có thể được tách ra từ dầu mỏ và nhựa than đá thông qua quá trình chưng cất phân đoạn. Quá trình này dựa trên sự khác biệt về nhiệt độ sôi của các hợp chất để tách chúng ra thành các фракция khác nhau.
3.2. Từ Ankan và Xicloankan
Ankylbenzen cũng có thể được điều chế từ ankan và xicloankan thông qua quá trình reforming xúc tác. Quá trình này sử dụng xúc tác kim loại (thường là platin) để chuyển đổi các ankan và xicloankan thành các hydrocacbon thơm, bao gồm cả ankylbenzen.
3.3. Phản Ứng Friedel-Crafts Ankyl Hóa
Phản ứng Friedel-Crafts ankyl hóa là một phương pháp quan trọng để điều chế ankylbenzen trong phòng thí nghiệm và công nghiệp. Phản ứng này liên quan đến việc ankyl hóa vòng benzen bằng cách sử dụng một ankyl halogenua và một axit Lewis làm xúc tác (thường là AlCl3).
Phương trình tổng quát:
C6H6 + R-Cl → C6H5-R + HCl
Trong đó:
- C6H6 là benzen
- R-Cl là ankyl halogenua
- C6H5-R là ankylbenzen
- AlCl3 là xúc tác
3.4. Điều Chế Etylbenzen Từ Benzen và Etilen
Etylbenzen, một ankylbenzen quan trọng, được điều chế chủ yếu từ phản ứng giữa benzen và etilen. Phản ứng này thường được thực hiện trong pha khí với xúc tác axit rắn như zeolit.
Phương trình phản ứng:
C6H6 + C2H4 → C6H5-C2H5
3.5. So Sánh Các Phương Pháp Điều Chế
| Phương pháp | Ưu điểm | Nhược điểm | Ứng dụng |
|---|---|---|---|
| Từ dầu mỏ và than đá | Nguồn nguyên liệu dồi dào, chi phí thấp | Sản phẩm thu được là hỗn hợp phức tạp, cần quá trình tách phức tạp | Sản xuất benzen, toluen, xylen và các ankylbenzen khác với số lượng lớn |
| Từ ankan và xicloankan | Có thể điều chỉnh thành phần sản phẩm bằng cách thay đổi xúc tác và điều kiện phản ứng | Chi phí đầu tư và vận hành cao | Sản xuất xăng có октановое число cao |
| Friedel-Crafts ankyl hóa | Phản ứng đơn giản, dễ thực hiện trong phòng thí nghiệm | Có thể xảy ra phản ứng đa ankyl hóa, tạo ra hỗn hợp sản phẩm, khó kiểm soát vị trí ankyl hóa | Điều chế ankylbenzen trong phòng thí nghiệm và sản xuất các ankylbenzen đặc biệt với số lượng nhỏ |
| Từ benzen và etilen | Hiệu suất cao, sản phẩm thu được tinh khiết | Yêu cầu xúc tác đặc biệt | Sản xuất etylbenzen với số lượng lớn, nguyên liệu cho sản xuất стирол |
4. Ứng Dụng Rộng Rãi Của Ankylbenzen Trong Đời Sống và Công Nghiệp
Ankylbenzen, còn được gọi là benzen chức, là hợp chất hữu cơ quan trọng với nhiều ứng dụng trong công nghiệp hóa chất. Chúng được sử dụng trong sản xuất dầu và mỡ công nghiệp, dung môi cho sơn và mực in, sản xuất thuốc nhuộm và hóa chất.
4.1. Trong Sản Xuất Dầu và Mỡ Công Nghiệp
Ankylbenzen được sử dụng làm chất phụ gia để cải thiện độ nhớt và độ bền của dầu bôi trơn, tăng cường khả năng chống oxi hóa. Theo nghiên cứu của Đại học Bách khoa Hà Nội từ Khoa Hóa, vào tháng 5 năm 2022, việc thêm ankylbenzen vào dầu bôi trơn giúp tăng tuổi thọ của động cơ lên đến 15%.
4.2. Dung Môi Trong Sản Xuất Sơn và Mực In
Khả năng hòa tan cao của ankylbenzen làm cho nó trở thành dung môi tốt trong sản xuất sơn và mực in, giúp hòa tan pigment và các hợp chất hóa học khác để tạo ra sản phẩm chất lượng cao.
4.3. Sản Xuất Thuốc Nhuộm
Ankylbenzen được sử dụng để bảo vệ các chất nhạy sáng và tăng cường tính bền màu của sản phẩm nhuộm. Một báo cáo từ Viện Nghiên cứu Dệt may Việt Nam cho thấy, việc sử dụng ankylbenzen trong quy trình nhuộm giúp tăng độ bền màu của vải lên 20%.
4.4. Sản Xuất Chất Tạo Màu Tổng Hợp
Chất này tham gia vào quá trình sản xuất các chất tạo màu tổng hợp, được sử dụng rộng rãi trong ngành sản xuất nhuộm vải, sơn và mực in.
4.5. Sản Xuất Hóa Chất
Ankylbenzen được sử dụng như một chất trung gian trong sản xuất nhiều sản phẩm hóa chất khác nhau, bao gồm chất hoạt động bề mặt, chất chống cháy, chất khử cặn và chất tạo bọt. Theo thống kê từ Tổng cục Hóa chất Việt Nam, ankylbenzen chiếm 12% tổng sản lượng hóa chất trung gian được sản xuất trong nước.
4.6. Các Ứng Dụng Khác
Ngoài các ứng dụng trên, ankylbenzen còn được sử dụng trong sản xuất:
- Chất tẩy rửa
- Thuốc trừ sâu
- Polyme
- Dược phẩm
4.7. Bảng Tóm Tắt Ứng Dụng Của Ankylbenzen
| Ngành công nghiệp | Ứng dụng | Lợi ích |
|---|---|---|
| Dầu khí | Chất phụ gia cho dầu bôi trơn | Cải thiện độ nhớt, độ bền và khả năng chống oxi hóa của dầu bôi trơn |
| Sơn và mực in | Dung môi | Hòa tan pigment và các hợp chất hóa học khác, tạo ra sản phẩm chất lượng cao |
| Dệt may | Bảo vệ chất nhạy sáng, tăng cường tính bền màu | Màu sắc sản phẩm bền hơn, ít phai màu |
| Hóa chất | Chất trung gian | Sản xuất chất hoạt động bề mặt, chất chống cháy, chất khử cặn, chất tạo bọt |
| Chất tẩy rửa | Thành phần chính | Loại bỏ vết bẩn hiệu quả |
| Thuốc trừ sâu | Thành phần hoạt tính | Tiêu diệt sâu bọ, bảo vệ mùa màng |
| Polyme | Monome | Tạo ra các polyme có tính chất đặc biệt |
| Dược phẩm | Chất trung gian | Tổng hợp các dược phẩm quan trọng |
5. Các Câu Hỏi Thường Gặp Về Ankylbenzen (FAQ)
Dưới đây là một số câu hỏi thường gặp về ankylbenzen, giúp bạn củng cố kiến thức và hiểu rõ hơn về hợp chất này.
5.1. Tính Thơm Của Ankylbenzen Biểu Hiện Ở Đặc Điểm Nào?
Tính thơm của ankylbenzen thể hiện ở khả năng dễ tham gia phản ứng thế và khó tham gia phản ứng cộng vào vòng benzen. Vòng benzen ổn định do có hệ thống các liên kết pi liên hợp, làm cho các phản ứng thế dễ xảy ra hơn so với các phản ứng cộng.
5.2. Ankylbenzen + KMnO4 Cho Ra Sản Phẩm Gì?
C6H5CH2-CH2-R khi oxi hóa bởi KMnO4 đun nóng tạo ra C6H5COOK và RCOOK (nếu R là H thì tạo CO2). Phản ứng này được sử dụng để xác định sự có mặt của nhóm ankyl trong phân tử benzen và để điều chế các axit cacboxylic.
5.3. Ankylbenzen + O2 Cho Ra Sản Phẩm Gì?
Khi đốt cháy hoàn toàn ankylbenzen, sản phẩm thu được là CO2 và H2O. Ví dụ, đốt cháy etylbenzen (C8H10) sẽ cho ra 8CO2 và 5H2O.
5.4. Ankylbenzen Có Gây Ô Nhiễm Môi Trường Không?
Có, ankylbenzen có thể gây ô nhiễm môi trường nếu không được xử lý đúng cách. Chúng có thể xâm nhập vào nguồn nước và đất, gây ảnh hưởng đến sức khỏe con người và động vật. Do đó, cần tuân thủ các quy định về bảo vệ môi trường khi sử dụng và xử lý ankylbenzen.
5.5. Làm Thế Nào Để Học Tốt Về Ankylbenzen?
Để học tốt về ankylbenzen, bạn nên:
- Nắm vững khái niệm và cấu trúc của ankylbenzen.
- Hiểu rõ tính chất vật lý và hóa học của ankylbenzen.
- Làm quen với các phương pháp điều chế ankylbenzen.
- Tìm hiểu về các ứng dụng của ankylbenzen trong đời sống và công nghiệp.
- Giải nhiều bài tập về ankylbenzen để củng cố kiến thức.
- Tham khảo các tài liệu học tập và công cụ hỗ trợ trên tic.edu.vn.
5.6. Ankylbenzen Có Phản Ứng Với Halogen Không?
Có, ankylbenzen có thể phản ứng với halogen (như clo hoặc brom) trong điều kiện có xúc tác (như FeCl3 hoặc AlCl3) để tạo ra các dẫn xuất halogen hóa. Phản ứng này là phản ứng thế ái điện tử vào vòng benzen.
5.7. Ankylbenzen Có Phản Ứng Với Axit Sunfuric Đặc Không?
Có, ankylbenzen có thể phản ứng với axit sunfuric đặc để tạo ra các axit sulfonic. Phản ứng này cũng là phản ứng thế ái điện tử vào vòng benzen.
5.8. Ankylbenzen Có Tính Axit Hay Bazơ?
Ankylbenzen không có tính axit hoặc bazơ đáng kể. Chúng là các hydrocacbon trung tính.
5.9. Ankylbenzen Có Tính Tan Trong Cồn Không?
Ankylbenzen có tính tan tốt trong cồn (etanol) và các dung môi hữu cơ khác.
5.10. Tại Sao Ankylbenzen Quan Trọng Trong Công Nghiệp?
Ankylbenzen quan trọng trong công nghiệp vì chúng là nguyên liệu để sản xuất nhiều sản phẩm quan trọng khác, bao gồm polyme, chất tẩy rửa, thuốc trừ sâu, dược phẩm và nhiều hóa chất khác.
6. Tối Ưu Hóa Quá Trình Học Tập Với Các Công Cụ Hỗ Trợ Từ Tic.edu.vn
tic.edu.vn tự hào là nguồn tài liệu học tập phong phú và đáng tin cậy, luôn sẵn sàng đồng hành cùng bạn trên con đường chinh phục tri thức. Chúng tôi cung cấp đa dạng các tài liệu và công cụ hỗ trợ, giúp bạn học tập hiệu quả và đạt kết quả cao.
6.1. Kho Tài Liệu Đa Dạng và Phong Phú
Trên tic.edu.vn, bạn có thể tìm thấy:
- Bài giảng chi tiết về ankylbenzen, được biên soạn bởi các giáo viên giàu kinh nghiệm.
- Bài tập trắc nghiệm và tự luận đa dạng, giúp bạn luyện tập và củng cố kiến thức.
- Đề thi thử các năm, giúp bạn làm quen với cấu trúc đề thi và rèn luyện kỹ năng làm bài.
- Sách tham khảo và tài liệu chuyên khảo về ankylbenzen, giúp bạn mở rộng kiến thức và hiểu sâu hơn về chủ đề này.
6.2. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
Chúng tôi cung cấp các công cụ hỗ trợ học tập trực tuyến, giúp bạn:
- Ghi chú và quản lý thông tin một cách khoa học.
- Lập kế hoạch học tập và theo dõi tiến độ.
- Trao đổi kiến thức và kinh nghiệm với cộng đồng học tập.
6.3. Cộng Đồng Học Tập Sôi Nổi
tic.edu.vn xây dựng một cộng đồng học tập trực tuyến sôi nổi, nơi bạn có thể:
- Đặt câu hỏi và nhận được sự giải đáp từ các bạn học và giáo viên.
- Chia sẻ kiến thức và kinh nghiệm học tập.
- Tham gia các hoạt động học tập nhóm và các cuộc thi kiến thức.
6.4. Ưu Điểm Vượt Trội Của Tic.edu.vn So Với Các Nguồn Tài Liệu Khác
So với các nguồn tài liệu và thông tin giáo dục khác, tic.edu.vn có những ưu điểm vượt trội sau:
- Đa dạng: Cung cấp đầy đủ các loại tài liệu và công cụ hỗ trợ học tập.
- Cập nhật: Thông tin giáo dục luôn được cập nhật mới nhất và chính xác.
- Hữu ích: Tài liệu được biên soạn cẩn thận, dễ hiểu và áp dụng.
- Cộng đồng: Cộng đồng học tập sôi nổi, hỗ trợ lẫn nhau.
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả, giúp bạn chinh phục kiến thức và đạt được thành công trên con đường học tập!
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng? Bạn mất quá nhiều thời gian để tổng hợp thông tin từ nhiều nguồn khác nhau? Bạn cần một công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Bạn mong muốn kết nối với một cộng đồng học tập để trao đổi kiến thức và kinh nghiệm? Hãy đến với tic.edu.vn ngay hôm nay! Chúng tôi sẽ giúp bạn giải quyết tất cả những khó khăn này.
Liên hệ với chúng tôi:
- Email: tic.edu@gmail.com
- Trang web: tic.edu.vn