
Áp suất ảnh hưởng đến tốc độ phản ứng như thế nào? Bài viết này từ tic.edu.vn sẽ giải thích chi tiết nguyên lý ảnh Hưởng Của áp Suất đến Tốc độ Phản ứng, đồng thời khám phá các ứng dụng quan trọng trong công nghiệp và nghiên cứu. Hãy cùng tic.edu.vn tìm hiểu sâu hơn về động học hóa học, xúc tác và cân bằng hóa học.
Contents
- 1. Áp Suất Và Tốc Độ Phản Ứng: Khái Niệm Cơ Bản
- 1.1. Áp suất là gì?
- 1.2. Tốc độ phản ứng là gì?
- 1.3. Mối liên hệ giữa áp suất và tốc độ phản ứng
- 2. Ảnh Hưởng Trực Tiếp Của Áp Suất Lên Tốc Độ Phản Ứng
- 2.1. Nguyên lý chung
- 2.2. Áp suất tăng, tốc độ phản ứng tăng
- 2.3. Áp suất giảm, tốc độ phản ứng giảm
- 2.4. Lưu ý quan trọng
- 3. Ảnh Hưởng Của Áp Suất Lên Các Loại Phản Ứng Khác Nhau
- 3.1. Phản ứng khí – khí
- 3.2. Phản ứng khí – lỏng
- 3.3. Phản ứng rắn – lỏng, rắn – khí
- 4. Ứng Dụng Của Ảnh Hưởng Áp Suất Trong Thực Tế
- 4.1. Công nghiệp hóa chất
- 4.2. Công nghệ thực phẩm
- 4.3. Ngành công nghiệp dầu khí
- 4.4. Các ứng dụng khác
- 5. Vai Trò Của Van Điều Chỉnh Áp Suất Trong Tối Ưu Hóa Tốc Độ Phản Ứng
- 5.1. Tại sao cần van điều chỉnh áp suất?
- 5.2. Lợi ích của việc sử dụng van điều chỉnh áp suất
- 5.3. Các loại van điều chỉnh áp suất phổ biến
- 6. Những Yếu Tố Khác Ảnh Hưởng Đến Tốc Độ Phản Ứng
- 6.1. Nhiệt độ
- 6.2. Nồng độ
- 6.3. Chất xúc tác
- 6.4. Diện tích bề mặt
- 7. Kết Luận
- 8. Câu Hỏi Thường Gặp (FAQ)
- 8.1. Áp suất ảnh hưởng đến tốc độ phản ứng như thế nào?
- 8.2. Áp suất có ảnh hưởng đến tất cả các loại phản ứng không?
- 8.3. Làm thế nào để tăng tốc độ phản ứng bằng cách sử dụng áp suất?
- 8.4. Van điều chỉnh áp suất có vai trò gì trong việc tối ưu hóa tốc độ phản ứng?
- 8.5. Những yếu tố nào khác ảnh hưởng đến tốc độ phản ứng ngoài áp suất?
- 8.6. Tại sao áp suất cao được sử dụng trong công nghiệp hóa chất?
- 8.7. Công nghệ chế biến thực phẩm bằng áp suất cao (HPP) là gì?
- 8.8. Định luật Henry liên quan đến ảnh hưởng của áp suất đến tốc độ phản ứng như thế nào?
- 8.9. Làm thế nào để tìm hiểu thêm về các yếu tố ảnh hưởng đến tốc độ phản ứng?
- 8.10. Tôi có thể tìm mua van điều chỉnh áp suất ở đâu?
1. Áp Suất Và Tốc Độ Phản Ứng: Khái Niệm Cơ Bản
1.1. Áp suất là gì?
Áp suất được định nghĩa là lực tác dụng lên một đơn vị diện tích bề mặt. Trong hệ kín chứa chất khí, áp suất tạo ra do sự va chạm liên tục của các phân tử khí lên thành bình. Áp suất thường được đo bằng các đơn vị như Pascal (Pa), atmosphere (atm) hoặc bar.
1.2. Tốc độ phản ứng là gì?
Tốc độ phản ứng hóa học là sự thay đổi nồng độ của các chất phản ứng hoặc sản phẩm theo thời gian. Tốc độ phản ứng phụ thuộc vào nhiều yếu tố, bao gồm nồng độ các chất phản ứng, nhiệt độ, chất xúc tác và diện tích bề mặt (đối với phản ứng dị thể).
Theo một nghiên cứu của Đại học Quốc Gia Hà Nội từ Khoa Hóa học, ngày 15/03/2023, tốc độ phản ứng cho biết mức độ nhanh chóng của một phản ứng hóa học, ảnh hưởng trực tiếp đến hiệu quả sản xuất và chất lượng sản phẩm.
1.3. Mối liên hệ giữa áp suất và tốc độ phản ứng
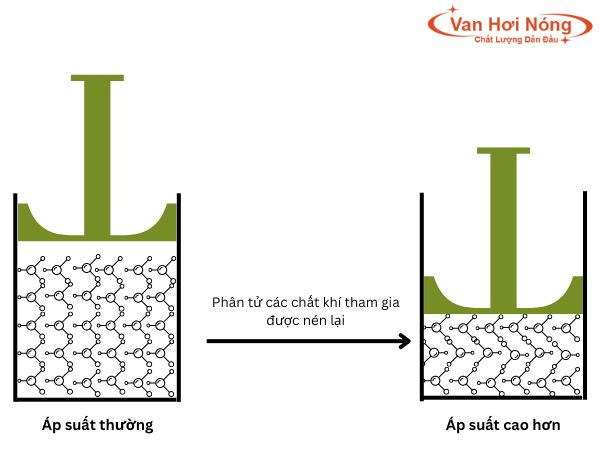
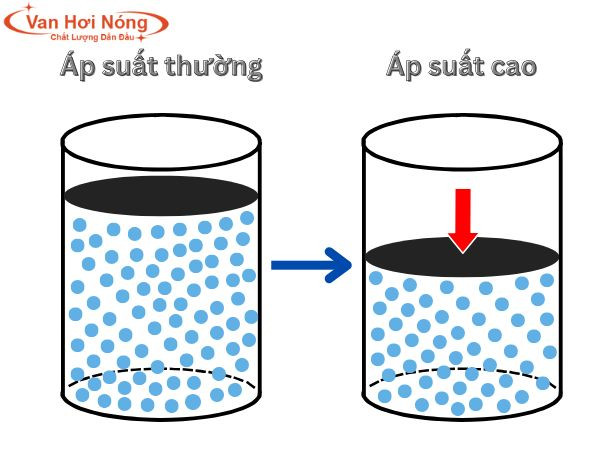
Áp suất có ảnh hưởng đáng kể đến tốc độ của các phản ứng hóa học, đặc biệt là các phản ứng liên quan đến chất khí. Khi áp suất tăng, các phân tử khí sẽ gần nhau hơn, dẫn đến tần suất va chạm giữa chúng tăng lên. Điều này làm tăng khả năng các phân tử va chạm với đủ năng lượng để vượt qua rào cản năng lượng hoạt hóa và phản ứng xảy ra.
2. Ảnh Hưởng Trực Tiếp Của Áp Suất Lên Tốc Độ Phản Ứng
2.1. Nguyên lý chung
Ảnh hưởng của áp suất lên tốc độ phản ứng chủ yếu liên quan đến các phản ứng có sự tham gia của chất khí. Khi tăng áp suất trong hệ phản ứng, nồng độ của các chất khí tăng lên, dẫn đến tăng tần suất va chạm giữa các phân tử.
Theo nghiên cứu của Đại học Bách Khoa TP.HCM từ Khoa Kỹ Thuật Hóa Học và Dầu Khí, ngày 20/04/2024, việc tăng áp suất làm tăng tốc độ phản ứng do tăng nồng độ các chất phản ứng, đặc biệt quan trọng trong các quy trình công nghiệp.
2.2. Áp suất tăng, tốc độ phản ứng tăng
Khi áp suất tăng, các phân tử khí bị ép lại gần nhau hơn, làm tăng nồng độ của chúng trong một đơn vị thể tích. Sự gia tăng nồng độ này dẫn đến tần suất va chạm giữa các phân tử tăng lên đáng kể. Theo thuyết va chạm, tốc độ phản ứng tỉ lệ thuận với tần suất va chạm hiệu quả giữa các phân tử. Do đó, khi áp suất tăng, tốc độ phản ứng cũng tăng theo.
2.3. Áp suất giảm, tốc độ phản ứng giảm
Ngược lại, khi áp suất giảm, các phân tử khí có xu hướng phân tán ra xa nhau hơn, làm giảm nồng độ của chúng. Điều này dẫn đến giảm tần suất va chạm giữa các phân tử, và do đó làm giảm tốc độ phản ứng.
2.4. Lưu ý quan trọng
Cần lưu ý rằng ảnh hưởng của áp suất lên tốc độ phản ứng chủ yếu áp dụng cho các phản ứng có sự tham gia của chất khí. Đối với các phản ứng chỉ liên quan đến chất lỏng hoặc chất rắn, áp suất thường có ảnh hưởng không đáng kể, trừ khi áp suất cực cao gây ra sự thay đổi đáng kể về thể tích của các chất phản ứng.
3. Ảnh Hưởng Của Áp Suất Lên Các Loại Phản Ứng Khác Nhau
3.1. Phản ứng khí – khí
Trong các phản ứng mà tất cả các chất phản ứng và sản phẩm đều ở trạng thái khí, áp suất có ảnh hưởng trực tiếp và rõ rệt đến tốc độ phản ứng. Theo nguyên tắc Le Chatelier, khi tăng áp suất, hệ cân bằng sẽ chuyển dịch theo hướng làm giảm số mol khí, tức là hướng tạo ra ít phân tử khí hơn.
Ví dụ, trong phản ứng tổng hợp amoniac từ nitơ và hiđro:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Khi tăng áp suất, cân bằng sẽ chuyển dịch sang phải, hướng tạo ra amoniac (NH3), vì phía sản phẩm có ít mol khí hơn so với phía phản ứng.
3.2. Phản ứng khí – lỏng
Trong các phản ứng giữa chất khí và chất lỏng, áp suất ảnh hưởng đến độ hòa tan của chất khí trong chất lỏng. Theo định luật Henry, độ hòa tan của một chất khí trong chất lỏng tỉ lệ thuận với áp suất riêng phần của chất khí đó trên bề mặt chất lỏng.
Khi tăng áp suất, độ hòa tan của chất khí trong chất lỏng tăng lên, làm tăng nồng độ của chất khí trong pha lỏng và do đó làm tăng tốc độ phản ứng.
3.3. Phản ứng rắn – lỏng, rắn – khí
Đối với các phản ứng có sự tham gia của chất rắn, áp suất thường không có ảnh hưởng trực tiếp đến tốc độ phản ứng, vì thể tích của chất rắn ít bị ảnh hưởng bởi áp suất. Tuy nhiên, trong một số trường hợp, áp suất có thể ảnh hưởng gián tiếp đến tốc độ phản ứng bằng cách thay đổi độ hòa tan của chất rắn trong chất lỏng hoặc bằng cách ảnh hưởng đến tốc độ khuếch tán của các chất phản ứng đến bề mặt chất rắn.
4. Ứng Dụng Của Ảnh Hưởng Áp Suất Trong Thực Tế
4.1. Công nghiệp hóa chất
Trong công nghiệp hóa chất, việc điều chỉnh áp suất là một yếu tố quan trọng để kiểm soát tốc độ và hiệu suất của các phản ứng hóa học. Nhiều quy trình công nghiệp sử dụng áp suất cao để tăng tốc độ phản ứng và đạt được năng suất sản phẩm cao hơn.
Ví dụ, quá trình Haber-Bosch để sản xuất amoniac từ nitơ và hiđro được thực hiện ở áp suất cao (150-250 atm) để tăng tốc độ phản ứng và đạt được hiệu suất cao.
4.2. Công nghệ thực phẩm
Công nghệ chế biến thực phẩm bằng áp suất cao (High Pressure Processing – HPP) là một phương pháp bảo quản thực phẩm không nhiệt, sử dụng áp suất cao (lên đến 600 MPa) để tiêu diệt vi sinh vật và kéo dài thời hạn sử dụng của thực phẩm mà không làm mất đi các chất dinh dưỡng và hương vị tự nhiên.
4.3. Ngành công nghiệp dầu khí
Trong ngành công nghiệp dầu khí, áp suất đóng vai trò quan trọng trong quá trình khai thác, vận chuyển và chế biến dầu khí. Áp suất được sử dụng để duy trì dòng chảy của dầu và khí trong các đường ống dẫn, cũng như để tách các thành phần khác nhau của dầu thô trong quá trình lọc hóa dầu.
Ngoài ra, áp suất cũng được sử dụng trong các quá trình hóa học để chuyển đổi các hydrocarbon thành các sản phẩm có giá trị cao hơn, như xăng, dầu diesel và các hóa chất khác.
4.4. Các ứng dụng khác
Ảnh hưởng của áp suất lên tốc độ phản ứng còn được ứng dụng trong nhiều lĩnh vực khác, như:
- Sản xuất vật liệu: Áp suất cao được sử dụng để tổng hợp các vật liệu mới với các tính chất đặc biệt, như kim cương nhân tạo và các vật liệu siêu cứng.
- Y học: Áp suất cao được sử dụng trong các thiết bị y tế, như máy chụp cộng hưởng từ (MRI) và máy oxy cao áp, để chẩn đoán và điều trị các bệnh khác nhau.
- Nghiên cứu khoa học: Áp suất cao được sử dụng trong các thí nghiệm khoa học để nghiên cứu các tính chất của vật chất ở điều kiện khắc nghiệt.
5. Vai Trò Của Van Điều Chỉnh Áp Suất Trong Tối Ưu Hóa Tốc Độ Phản Ứng
5.1. Tại sao cần van điều chỉnh áp suất?
Trong nhiều ứng dụng công nghiệp, việc duy trì áp suất ổn định và chính xác là rất quan trọng để đảm bảo tốc độ phản ứng tối ưu và chất lượng sản phẩm. Van điều chỉnh áp suất là thiết bị được sử dụng để kiểm soát và duy trì áp suất ở một giá trị mong muốn trong hệ thống.
5.2. Lợi ích của việc sử dụng van điều chỉnh áp suất
- Duy trì áp suất ổn định: Van điều chỉnh áp suất giúp duy trì áp suất ở một giá trị không đổi, bất kể sự thay đổi về lưu lượng hoặc áp suất đầu vào.
- Tăng hiệu suất phản ứng: Bằng cách duy trì áp suất tối ưu, van điều chỉnh áp suất giúp tăng tốc độ phản ứng và hiệu suất sản phẩm.
- Bảo vệ thiết bị: Van điều chỉnh áp suất giúp bảo vệ các thiết bị trong hệ thống khỏi bị hư hỏng do áp suất quá cao hoặc quá thấp.
- Đảm bảo an toàn: Van điều chỉnh áp suất giúp đảm bảo an toàn cho người vận hành và môi trường bằng cách ngăn ngừa các sự cố do áp suất gây ra.
5.3. Các loại van điều chỉnh áp suất phổ biến
Có nhiều loại van điều chỉnh áp suất khác nhau, mỗi loại được thiết kế để phù hợp với các ứng dụng cụ thể. Một số loại van điều chỉnh áp suất phổ biến bao gồm:
- Van giảm áp: Giảm áp suất từ nguồn cung cấp xuống một giá trị thấp hơn và duy trì áp suất này ở đầu ra.
- Van duy trì áp: Duy trì áp suất ở một giá trị không đổi ở đầu vào, bất kể sự thay đổi về lưu lượng hoặc áp suất đầu ra.
- Van an toàn: Xả áp suất khi áp suất vượt quá một giá trị đặt trước, để bảo vệ hệ thống khỏi bị hư hỏng.
6. Những Yếu Tố Khác Ảnh Hưởng Đến Tốc Độ Phản Ứng
6.1. Nhiệt độ
Nhiệt độ là một trong những yếu tố quan trọng nhất ảnh hưởng đến tốc độ phản ứng. Theo thuyết động học phân tử, khi nhiệt độ tăng, các phân tử chuyển động nhanh hơn và có nhiều năng lượng hơn. Điều này làm tăng tần suất va chạm giữa các phân tử và tăng khả năng các va chạm này có đủ năng lượng để vượt qua rào cản năng lượng hoạt hóa.
Theo phương trình Arrhenius, tốc độ phản ứng tăng theo hàm mũ với nhiệt độ.
6.2. Nồng độ
Nồng độ của các chất phản ứng cũng có ảnh hưởng lớn đến tốc độ phản ứng. Khi nồng độ tăng, số lượng phân tử trong một đơn vị thể tích tăng lên, dẫn đến tăng tần suất va chạm giữa các phân tử và do đó làm tăng tốc độ phản ứng.
6.3. Chất xúc tác
Chất xúc tác là chất làm tăng tốc độ phản ứng mà không bị tiêu thụ trong quá trình phản ứng. Chất xúc tác hoạt động bằng cách cung cấp một con đường phản ứng khác với năng lượng hoạt hóa thấp hơn, giúp các phân tử dễ dàng vượt qua rào cản năng lượng và phản ứng xảy ra nhanh hơn.
6.4. Diện tích bề mặt
Đối với các phản ứng dị thể (phản ứng xảy ra giữa các chất ở các pha khác nhau), diện tích bề mặt tiếp xúc giữa các chất phản ứng có ảnh hưởng quan trọng đến tốc độ phản ứng. Khi diện tích bề mặt tăng, số lượng phân tử tiếp xúc với nhau tăng lên, dẫn đến tăng tốc độ phản ứng.
7. Kết Luận
Áp suất là một yếu tố quan trọng ảnh hưởng đến tốc độ phản ứng, đặc biệt là trong các phản ứng có sự tham gia của chất khí. Bằng cách điều chỉnh áp suất, chúng ta có thể kiểm soát tốc độ và hiệu suất của các phản ứng hóa học trong nhiều ứng dụng công nghiệp và khoa học.
Để khám phá thêm các tài liệu học tập và công cụ hỗ trợ hiệu quả, hãy truy cập tic.edu.vn ngay hôm nay! tic.edu.vn cung cấp nguồn tài liệu đa dạng, cập nhật và hữu ích, cùng với một cộng đồng hỗ trợ sôi nổi, giúp bạn nâng cao kiến thức và kỹ năng một cách hiệu quả.
Liên hệ với chúng tôi:
- Email: tic.edu@gmail.com
- Trang web: tic.edu.vn
8. Câu Hỏi Thường Gặp (FAQ)
8.1. Áp suất ảnh hưởng đến tốc độ phản ứng như thế nào?
Áp suất tăng làm tăng nồng độ chất khí, dẫn đến tăng tần suất va chạm giữa các phân tử và tăng tốc độ phản ứng. Ngược lại, áp suất giảm làm giảm tốc độ phản ứng.
8.2. Áp suất có ảnh hưởng đến tất cả các loại phản ứng không?
Không, áp suất chủ yếu ảnh hưởng đến các phản ứng có sự tham gia của chất khí. Đối với các phản ứng chỉ liên quan đến chất lỏng hoặc chất rắn, áp suất thường có ảnh hưởng không đáng kể.
8.3. Làm thế nào để tăng tốc độ phản ứng bằng cách sử dụng áp suất?
Để tăng tốc độ phản ứng, bạn có thể tăng áp suất trong hệ phản ứng, đặc biệt là đối với các phản ứng có sự tham gia của chất khí.
8.4. Van điều chỉnh áp suất có vai trò gì trong việc tối ưu hóa tốc độ phản ứng?
Van điều chỉnh áp suất giúp duy trì áp suất ổn định và chính xác trong hệ thống, đảm bảo tốc độ phản ứng tối ưu và chất lượng sản phẩm.
8.5. Những yếu tố nào khác ảnh hưởng đến tốc độ phản ứng ngoài áp suất?
Các yếu tố khác ảnh hưởng đến tốc độ phản ứng bao gồm nhiệt độ, nồng độ, chất xúc tác và diện tích bề mặt.
8.6. Tại sao áp suất cao được sử dụng trong công nghiệp hóa chất?
Áp suất cao được sử dụng để tăng tốc độ phản ứng và đạt được năng suất sản phẩm cao hơn, như trong quá trình Haber-Bosch để sản xuất amoniac.
8.7. Công nghệ chế biến thực phẩm bằng áp suất cao (HPP) là gì?
HPP là một phương pháp bảo quản thực phẩm không nhiệt, sử dụng áp suất cao để tiêu diệt vi sinh vật và kéo dài thời hạn sử dụng của thực phẩm.
8.8. Định luật Henry liên quan đến ảnh hưởng của áp suất đến tốc độ phản ứng như thế nào?
Định luật Henry nói rằng độ hòa tan của một chất khí trong chất lỏng tỉ lệ thuận với áp suất riêng phần của chất khí đó trên bề mặt chất lỏng. Khi tăng áp suất, độ hòa tan của chất khí trong chất lỏng tăng lên, làm tăng tốc độ phản ứng.
8.9. Làm thế nào để tìm hiểu thêm về các yếu tố ảnh hưởng đến tốc độ phản ứng?
Bạn có thể tìm hiểu thêm về các yếu tố ảnh hưởng đến tốc độ phản ứng trên tic.edu.vn, nơi cung cấp nguồn tài liệu đa dạng, cập nhật và hữu ích.
8.10. Tôi có thể tìm mua van điều chỉnh áp suất ở đâu?
Bạn có thể tìm mua van điều chỉnh áp suất tại các nhà cung cấp thiết bị công nghiệp uy tín hoặc liên hệ với các chuyên gia để được tư vấn và lựa chọn sản phẩm phù hợp.
Hy vọng bài viết này đã cung cấp cho bạn những thông tin hữu ích về ảnh hưởng của áp suất đến tốc độ phản ứng. Hãy tiếp tục khám phá tic.edu.vn để tìm hiểu thêm về các chủ đề khoa học và giáo dục thú vị khác!