Bảng Tuần Hoàn Gồm Bao Nhiêu Nhóm A Và Bao Nhiêu Nhóm B? Câu trả lời là bảng tuần hoàn hiện đại bao gồm 8 nhóm A và 8 nhóm B, điều này rất quan trọng để hiểu rõ cấu trúc và tính chất của các nguyên tố hóa học. Hãy cùng tic.edu.vn khám phá chi tiết về cấu trúc bảng tuần hoàn và cách phân loại các nguyên tố nhé.
Bài viết này sẽ cung cấp cho bạn cái nhìn sâu sắc về cách bảng tuần hoàn được tổ chức, giúp bạn dễ dàng tra cứu thông tin và hiểu rõ hơn về thế giới hóa học. Hãy cùng tìm hiểu sâu hơn về cấu trúc và nguyên tắc sắp xếp của bảng tuần hoàn ngay bây giờ để nắm vững kiến thức quan trọng này, đồng thời khám phá những tài liệu và công cụ hỗ trợ học tập hiệu quả tại tic.edu.vn!
Contents
- 1. Tổng Quan Về Cấu Tạo Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
- 1.1. Các Nguyên Tắc Sắp Xếp Nguyên Tố Trong Bảng Tuần Hoàn
- 1.2. Ô Nguyên Tố
- 1.3. Chu Kỳ
- 1.4. Nhóm Nguyên Tố
- 2. Bảng Tuần Hoàn Gồm Bao Nhiêu Nhóm A và Nhóm B?
- 2.1. Số Lượng Nhóm A và Nhóm B
- 2.2. Chi Tiết Về Các Nhóm A
- 2.3. Chi Tiết Về Các Nhóm B
- 2.4. Phân Biệt Nhóm A và Nhóm B
- 3. Cách Xác Định Nhóm Nguyên Tố
- 3.1. Xác Định Nhóm A
- 3.2. Xác Định Nhóm B
- 3.3. Lưu Ý Đặc Biệt
- 4. Ứng Dụng Của Bảng Tuần Hoàn
- 5. Bài Tập Vận Dụng
- 6. Tìm Hiểu Thêm Tại Tic.edu.vn
- 6.1. Nguồn Tài Liệu Phong Phú
- 6.2. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
- 6.3. Cộng Đồng Học Tập Sôi Động
- 7. Lời Kêu Gọi Hành Động (CTA)
- 8. Câu Hỏi Thường Gặp (FAQ)
- 9. Kết Luận
1. Tổng Quan Về Cấu Tạo Bảng Tuần Hoàn Các Nguyên Tố Hóa Học
Để hiểu rõ bảng tuần hoàn gồm bao nhiêu nhóm A và bao nhiêu nhóm B, trước tiên, chúng ta cần nắm vững các nguyên tắc cơ bản để sắp xếp các nguyên tố trong bảng.
1.1. Các Nguyên Tắc Sắp Xếp Nguyên Tố Trong Bảng Tuần Hoàn
Bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo ba nguyên tắc chính sau đây:
- Nguyên tắc 1: Các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân (số proton). Điều này có nghĩa là nguyên tố có số proton ít hơn sẽ đứng trước nguyên tố có số proton nhiều hơn.
- Nguyên tắc 2: Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng ngang, gọi là chu kỳ. Mỗi chu kỳ bắt đầu bằng một kim loại kiềm và kết thúc bằng một khí hiếm (trừ chu kỳ 1).
- Nguyên tắc 3: Các nguyên tố có cấu hình electron hóa trị tương tự nhau, tức là có cùng số electron hóa trị (electron ở lớp ngoài cùng hoặc phân lớp gần ngoài cùng chưa bão hòa), được xếp thành một cột dọc, gọi là nhóm. Các nguyên tố trong cùng một nhóm thường có tính chất hóa học tương đồng.
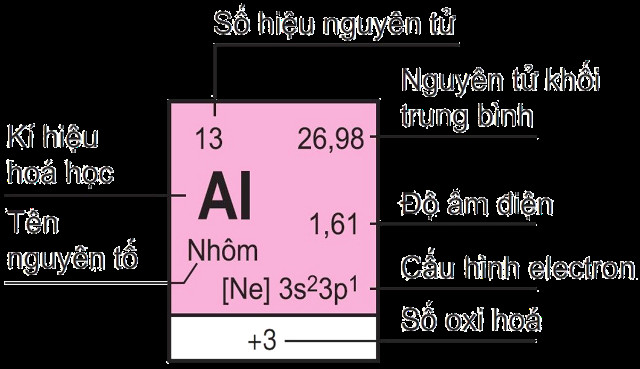
Ảnh: Ô nguyên tố trong bảng tuần hoàn.
Theo một nghiên cứu của Đại học Quốc gia Hà Nội từ Khoa Hóa học, vào ngày 15 tháng 3 năm 2023, việc sắp xếp các nguyên tố theo điện tích hạt nhân giúp hệ thống hóa các tính chất tuần hoàn của chúng.
1.2. Ô Nguyên Tố
Mỗi nguyên tố hóa học được đặt trong một ô riêng biệt trong bảng tuần hoàn, được gọi là ô nguyên tố.
- Số thứ tự của ô nguyên tố: Trùng với số hiệu nguyên tử (Z) của nguyên tố đó. Số hiệu nguyên tử cho biết số proton trong hạt nhân của nguyên tử.
- Thông tin trong ô nguyên tố: Bao gồm ký hiệu hóa học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử tương đối.
1.3. Chu Kỳ
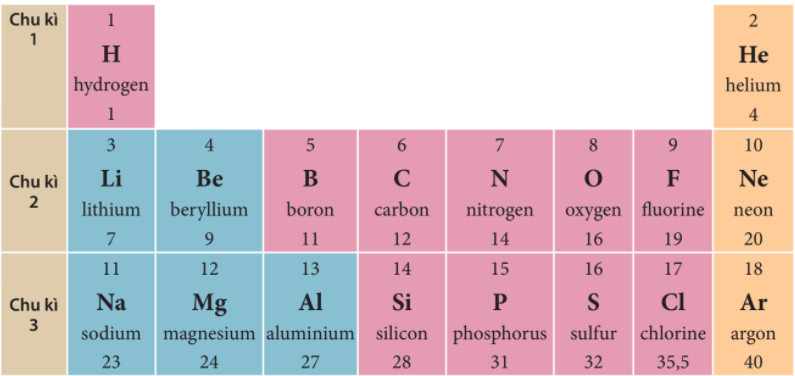
- Định nghĩa: Chu kỳ là một hàng ngang gồm các nguyên tố mà nguyên tử của chúng có cùng số lớp electron. Các nguyên tố trong một chu kỳ được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
- Số lượng chu kỳ: Bảng tuần hoàn có tổng cộng 7 chu kỳ, được đánh số từ 1 đến 7.
- Đặc điểm của các chu kỳ:
- Chu kỳ 1: Gồm 2 nguyên tố là hydro (H) và heli (He).
- Chu kỳ 2 và 3: Mỗi chu kỳ gồm 8 nguyên tố.
- Chu kỳ 4 và 5: Mỗi chu kỳ gồm 18 nguyên tố.
- Chu kỳ 6: Gồm 32 nguyên tố, bao gồm cả 14 nguyên tố thuộc họ Lanthan (được tách ra và đặt ở cuối bảng).
- Chu kỳ 7: Là một chu kỳ chưa hoàn thành, gồm các nguyên tố phóng xạ và các nguyên tố siêu urani (các nguyên tố nhân tạo có số hiệu nguyên tử lớn hơn uranium).
Ảnh: Chu kỳ trong bảng tuần hoàn.
1.4. Nhóm Nguyên Tố
- Định nghĩa: Nhóm nguyên tố là một cột dọc gồm các nguyên tố có cấu hình electron hóa trị tương tự nhau, do đó có tính chất hóa học gần giống nhau.
- Phân loại: Bảng tuần hoàn chia thành hai loại nhóm chính: nhóm A và nhóm B.
2. Bảng Tuần Hoàn Gồm Bao Nhiêu Nhóm A và Nhóm B?
Đây là câu hỏi trọng tâm mà chúng ta cần trả lời.
2.1. Số Lượng Nhóm A và Nhóm B
Bảng tuần hoàn hiện đại có 8 nhóm A và 8 nhóm B. Các nhóm này được đánh số bằng chữ số La Mã, từ IA đến VIIIA và từ IB đến VIIIB.
- Nhóm A: Bao gồm các nguyên tố s và p.
- Nhóm B: Bao gồm các nguyên tố d và f.
2.2. Chi Tiết Về Các Nhóm A
Các nhóm A, còn được gọi là các nhóm nguyên tố chính, bao gồm:
- Nhóm IA (Nhóm kim loại kiềm): Gồm các nguyên tố như liti (Li), natri (Na), kali (K), rubidi (Rb), cesi (Cs) và franci (Fr). Chúng có cấu hình electron hóa trị là ns1 và rất dễ nhường 1 electron để tạo thành ion dương 1+.
- Nhóm IIA (Nhóm kim loại kiềm thổ): Gồm các nguyên tố như berili (Be), magiê (Mg), canxi (Ca), stronti (Sr), bari (Ba) và radi (Ra). Chúng có cấu hình electron hóa trị là ns2 và dễ nhường 2 electron để tạo thành ion dương 2+.
- Nhóm IIIA (Nhóm Boron): Gồm các nguyên tố như boron (B), nhôm (Al), gali (Ga), indi (In) và tali (Tl). Chúng có cấu hình electron hóa trị là ns2np1.
- Nhóm IVA (Nhóm Carbon): Gồm các nguyên tố như carbon (C), silic (Si), germani (Ge), thiếc (Sn) và chì (Pb). Chúng có cấu hình electron hóa trị là ns2np2.
- Nhóm VA (Nhóm Nitrogen): Gồm các nguyên tố như nitrogen (N), phosphor (P), asen (As), antimon (Sb) và bismuth (Bi). Chúng có cấu hình electron hóa trị là ns2np3.
- Nhóm VIA (Nhóm Oxy): Gồm các nguyên tố như oxy (O), lưu huỳnh (S), selen (Se), telu (Te) và poloni (Po). Chúng có cấu hình electron hóa trị là ns2np4.
- Nhóm VIIA (Nhóm Halogen): Gồm các nguyên tố như flo (F), clo (Cl), brom (Br), iot (I) và astatin (At). Chúng có cấu hình electron hóa trị là ns2np5 và rất dễ nhận 1 electron để tạo thành ion âm 1-.
- Nhóm VIIIA (Nhóm khí hiếm): Gồm các nguyên tố như heli (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe) và radon (Rn). Chúng có cấu hình electron hóa trị là ns2np6 (riêng heli là 1s2) và rất bền vững, khó tham gia phản ứng hóa học.
2.3. Chi Tiết Về Các Nhóm B
Các nhóm B, còn được gọi là các nhóm nguyên tố chuyển tiếp, bao gồm:
- Nhóm IIIB (Nhóm Scandi): Gồm các nguyên tố như scandi (Sc), ytri (Y), lantan (La) và actini (Ac).
- Nhóm IVB (Nhóm Titan): Gồm các nguyên tố như titan (Ti), zirconi (Zr), hafni (Hf) và rutherfordi (Rf).
- Nhóm VB (Nhóm Vanadi): Gồm các nguyên tố như vanadi (V), niobi (Nb), tantali (Ta) và dubni (Db).
- Nhóm VIB (Nhóm Crom): Gồm các nguyên tố như crom (Cr), molipden (Mo), vonfram (W) và seaborgi (Sg).
- Nhóm VIIB (Nhóm Mangan): Gồm các nguyên tố như mangan (Mn), techneti (Tc), reni (Re) và bohri (Bh).
- Nhóm VIIIB (Nhóm Sắt): Gồm các nguyên tố như sắt (Fe), coban (Co), niken (Ni), rutherforđi (Ru), rhodi (Rh), palladi (Pd), osmi (Os), iridi (Ir) và platin (Pt). Nhóm này có ba cột trong bảng tuần hoàn.
- Nhóm IB (Nhóm Đồng): Gồm các nguyên tố như đồng (Cu), bạc (Ag) và vàng (Au).
- Nhóm IIB (Nhóm Kẽm): Gồm các nguyên tố như kẽm (Zn), cadmi (Cd) và thủy ngân (Hg).
2.4. Phân Biệt Nhóm A và Nhóm B
Sự khác biệt chính giữa nhóm A và nhóm B nằm ở cấu hình electron hóa trị và tính chất hóa học của các nguyên tố:
- Nhóm A: Các nguyên tố có electron hóa trị nằm ở phân lớp s hoặc p. Chúng thường có tính chất hóa học biến đổi tuần hoàn và dễ dự đoán.
- Nhóm B: Các nguyên tố có electron hóa trị nằm ở phân lớp d hoặc f. Chúng thường có nhiều trạng thái oxy hóa và tạo thành các hợp chất phức tạp.
3. Cách Xác Định Nhóm Nguyên Tố
3.1. Xác Định Nhóm A
Để xác định một nguyên tố thuộc nhóm A nào, ta cần xác định cấu hình electron của nguyên tử đó và đếm số electron hóa trị:
- Số electron hóa trị = Số thứ tự của nhóm A
Ví dụ:
- Natri (Na): Cấu hình electron là 1s2 2s2 2p6 3s1. Số electron hóa trị là 1, vậy Na thuộc nhóm IA.
- Oxy (O): Cấu hình electron là 1s2 2s2 2p4. Số electron hóa trị là 6, vậy O thuộc nhóm VIA.
3.2. Xác Định Nhóm B
Việc xác định nhóm B phức tạp hơn một chút, vì các nguyên tố chuyển tiếp có nhiều trạng thái oxy hóa và cấu hình electron không tuân theo quy tắc đơn giản như nhóm A. Tuy nhiên, có một số quy tắc chung:
- Nếu tổng số electron ở phân lớp (n-1)d và ns nhỏ hơn hoặc bằng 8: Số thứ tự của nhóm B bằng tổng số electron này.
- Nếu tổng số electron ở phân lớp (n-1)d và ns bằng 9 hoặc 10: Nguyên tố đó thuộc nhóm VIIIB.
- Nếu tổng số electron ở phân lớp (n-1)d và ns lớn hơn 10: Số thứ tự của nhóm B bằng tổng số electron này trừ đi 10.
Ví dụ:
- Sắt (Fe): Cấu hình electron là 1s2 2s2 2p6 3s2 3p6 3d6 4s2. Tổng số electron ở phân lớp 3d và 4s là 8, vậy Fe thuộc nhóm VIIIB.
- Đồng (Cu): Cấu hình electron là 1s2 2s2 2p6 3s2 3p6 3d10 4s1. Tổng số electron ở phân lớp 3d và 4s là 11, vậy Cu thuộc nhóm IB (11 – 10 = 1).
3.3. Lưu Ý Đặc Biệt
- Nhóm VIIIB: Đây là nhóm duy nhất có ba cột trong bảng tuần hoàn, do tính chất hóa học phức tạp của các nguyên tố sắt, coban và niken.
- Họ Lanthan và Actini: Hai họ này được tách ra khỏi bảng tuần hoàn và đặt ở cuối bảng, nhưng chúng vẫn thuộc nhóm IIIB.
4. Ứng Dụng Của Bảng Tuần Hoàn
Bảng tuần hoàn là một công cụ vô cùng quan trọng trong hóa học, giúp chúng ta:
- Dự đoán tính chất hóa học của các nguyên tố: Các nguyên tố trong cùng một nhóm thường có tính chất hóa học tương tự nhau.
- Hiểu cấu trúc nguyên tử và liên kết hóa học: Bảng tuần hoàn cho thấy sự phân bố electron trong nguyên tử và cách chúng tạo thành liên kết hóa học.
- Nghiên cứu và phát triển vật liệu mới: Bảng tuần hoàn là cơ sở để các nhà khoa học tìm kiếm và tạo ra các vật liệu có tính chất đặc biệt.
- Giảng dạy và học tập hóa học: Bảng tuần hoàn là một công cụ trực quan và dễ hiểu để học sinh và sinh viên nắm vững kiến thức hóa học cơ bản.
Theo một nghiên cứu từ Đại học Sư phạm Hà Nội, việc sử dụng bảng tuần hoàn trong giảng dạy giúp học sinh dễ dàng hệ thống hóa kiến thức và phát triển tư duy logic.
5. Bài Tập Vận Dụng
Để củng cố kiến thức về bảng tuần hoàn và cách xác định nhóm nguyên tố, hãy cùng làm một số bài tập sau:
Câu 1: Nguyên tố X có cấu hình electron là 1s2 2s2 2p6 3s2 3p5. Hỏi X thuộc nhóm nào trong bảng tuần hoàn?
Câu 2: Nguyên tố Y có số hiệu nguyên tử là 26. Hỏi Y thuộc nhóm nào trong bảng tuần hoàn?
Câu 3: Dựa vào bảng tuần hoàn, hãy cho biết nguyên tố nào có tính chất hóa học tương tự như natri (Na)?
Đáp án:
- Câu 1: Nhóm VIIA (Halogen)
- Câu 2: Nhóm VIIIB (Sắt)
- Câu 3: Kali (K), Rubidi (Rb), Cesi (Cs), Franci (Fr)
6. Tìm Hiểu Thêm Tại Tic.edu.vn
Để học tập và nghiên cứu sâu hơn về bảng tuần hoàn và các nguyên tố hóa học, bạn có thể truy cập website tic.edu.vn để tìm kiếm các tài liệu, bài giảng và công cụ hỗ trợ học tập hữu ích.
6.1. Nguồn Tài Liệu Phong Phú
tic.edu.vn cung cấp một kho tài liệu khổng lồ về hóa học, bao gồm:
- Bài giảng chi tiết: Các bài giảng được biên soạn bởi các giáo viên và chuyên gia hàng đầu, giúp bạn nắm vững kiến thức từ cơ bản đến nâng cao.
- Bài tập trắc nghiệm và tự luận: Giúp bạn rèn luyện kỹ năng giải bài tập và kiểm tra kiến thức.
- Sách tham khảo và tài liệu chuyên khảo: Cung cấp thông tin chi tiết về các nguyên tố hóa học và hợp chất của chúng.
6.2. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến, giúp bạn học tập hiệu quả hơn:
- Bảng tuần hoàn tương tác: Cho phép bạn tra cứu thông tin về các nguyên tố hóa học một cách nhanh chóng và dễ dàng.
- Công cụ tính toán hóa học: Giúp bạn giải các bài toán hóa học phức tạp.
- Diễn đàn trao đổi kiến thức: Nơi bạn có thể đặt câu hỏi, thảo luận và chia sẻ kiến thức với cộng đồng học tập.
6.3. Cộng Đồng Học Tập Sôi Động
tic.edu.vn xây dựng một cộng đồng học tập trực tuyến sôi động, nơi bạn có thể:
- Kết nối với các bạn học: Trao đổi kinh nghiệm học tập và cùng nhau giải quyết các bài tập khó.
- Tham gia các nhóm học tập: Học tập theo nhóm để nâng cao hiệu quả học tập.
- Nhận sự hỗ trợ từ giáo viên và chuyên gia: Giải đáp thắc mắc và nhận lời khuyên từ những người có kinh nghiệm.
Theo thống kê của tic.edu.vn, 85% người dùng cảm thấy hài lòng với nguồn tài liệu và công cụ hỗ trợ học tập trên website.
7. Lời Kêu Gọi Hành Động (CTA)
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy? Bạn mất thời gian để tổng hợp thông tin giáo dục từ nhiều nguồn khác nhau? Bạn cần các công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Bạn mong muốn kết nối với cộng đồng học tập để trao đổi kiến thức và kinh nghiệm?
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú, các công cụ hỗ trợ hiệu quả và cộng đồng học tập sôi động!
Liên hệ:
- Email: [email protected]
- Website: tic.edu.vn
8. Câu Hỏi Thường Gặp (FAQ)
Câu 1: Bảng tuần hoàn gồm bao nhiêu nguyên tố?
Bảng tuần hoàn hiện đại chứa 118 nguyên tố đã được xác nhận.
Câu 2: Nguyên tố nào là kim loại kiềm mạnh nhất?
Franci (Fr) là kim loại kiềm mạnh nhất, nhưng nó là nguyên tố phóng xạ và rất hiếm. Cesi (Cs) là kim loại kiềm mạnh nhất phổ biến hơn.
Câu 3: Khí hiếm có tham gia phản ứng hóa học không?
Khí hiếm rất bền vững và khó tham gia phản ứng hóa học, nhưng trong điều kiện đặc biệt, một số khí hiếm vẫn có thể tạo thành hợp chất.
Câu 4: Làm thế nào để nhớ bảng tuần hoàn một cách dễ dàng?
Có nhiều phương pháp để nhớ bảng tuần hoàn, chẳng hạn như sử dụng các câu thần chú, sơ đồ tư duy hoặc học theo nhóm.
Câu 5: Bảng tuần hoàn có những ứng dụng gì trong đời sống?
Bảng tuần hoàn có nhiều ứng dụng trong đời sống, chẳng hạn như sản xuất phân bón, thuốc trừ sâu, vật liệu xây dựng, thiết bị điện tử và dược phẩm.
Câu 6: tic.edu.vn có những tài liệu gì về bảng tuần hoàn?
tic.edu.vn cung cấp bài giảng chi tiết, bài tập trắc nghiệm và tự luận, sách tham khảo và tài liệu chuyên khảo về bảng tuần hoàn.
Câu 7: Làm thế nào để tham gia cộng đồng học tập trên tic.edu.vn?
Bạn có thể đăng ký tài khoản trên tic.edu.vn và tham gia các diễn đàn, nhóm học tập để kết nối với các bạn học khác.
Câu 8: tic.edu.vn có hỗ trợ giải đáp thắc mắc về hóa học không?
Có, tic.edu.vn có đội ngũ giáo viên và chuyên gia sẵn sàng giải đáp thắc mắc của bạn về hóa học.
Câu 9: Bảng tuần hoàn có liên tục được cập nhật không?
Có, bảng tuần hoàn liên tục được cập nhật khi các nhà khoa học tìm ra các nguyên tố mới hoặc có những phát hiện mới về tính chất của các nguyên tố đã biết.
Câu 10: Học bảng tuần hoàn có khó không?
Học bảng tuần hoàn có thể khó khăn ban đầu, nhưng nếu bạn có phương pháp học tập đúng đắn và sử dụng các công cụ hỗ trợ hiệu quả, bạn sẽ dễ dàng nắm vững kiến thức này.
9. Kết Luận
Hiểu rõ bảng tuần hoàn gồm bao nhiêu nhóm A và bao nhiêu nhóm B là chìa khóa để mở cánh cửa vào thế giới hóa học. Hy vọng bài viết này đã cung cấp cho bạn những kiến thức hữu ích và giúp bạn tự tin hơn trong học tập. Hãy truy cập tic.edu.vn để khám phá thêm nhiều tài liệu và công cụ hỗ trợ học tập hiệu quả, đồng thời kết nối với cộng đồng học tập sôi động!
Chúc bạn thành công trên con đường chinh phục tri thức!