Kim loại Fe không phản ứng với dung dịch nào là câu hỏi thường gặp trong hóa học. Bài viết này từ tic.edu.vn sẽ cung cấp câu trả lời chi tiết, giải thích rõ ràng về tính chất hóa học của sắt và các phản ứng liên quan, giúp bạn nắm vững kiến thức và tự tin chinh phục các bài tập. Đồng thời, khám phá nguồn tài liệu phong phú và công cụ hỗ trợ học tập hiệu quả trên tic.edu.vn.
Contents
- 1. Câu Trả Lời Ngắn Gọn: Kim Loại Fe Không Phản Ứng Với Dung Dịch Nào?
- 2. Giải Thích Chi Tiết: Tại Sao Fe Không Phản Ứng Với ZnCl2?
- 2.1. Quy Tắc α (Alpha) Là Gì?
- 2.2. Áp Dụng Quy Tắc α Cho Fe và ZnCl2
- 2.3. Dãy Điện Hóa Của Kim Loại
- 3. Tính Chất Hóa Học Của Sắt (Fe)
- 3.1. Tác Dụng Với Phi Kim
- 3.1.1. Phản Ứng Với Oxi (O2)
- 3.1.2. Phản Ứng Với Clo (Cl2)
- 3.1.3. Phản Ứng Với Các Phi Kim Khác
- 3.2. Tác Dụng Với Axit
- 3.2.1. Phản Ứng Với Axit Clohidric (HCl) và Axit Sunfuric Loãng (H2SO4)
- 3.2.2. Lưu Ý Quan Trọng Về Axit Đặc Nguội
- 3.2.3. Phản Ứng Với Axit Nitric Đặc Nóng (HNO3 đặc, nóng) và Axit Sunfuric Đặc Nóng (H2SO4 đặc, nóng)
- 3.3. Tác Dụng Với Dung Dịch Muối
- 4. Các Trường Hợp Fe Không Phản Ứng Với Dung Dịch
- 4.1. Dung Dịch HNO3 Đặc Nguội và H2SO4 Đặc Nguội
- 4.2. Dung Dịch Muối Của Kim Loại Mạnh Hơn
- 5. Câu Hỏi Trắc Nghiệm Vận Dụng
- 6. Ứng Dụng Kiến Thức Về Phản Ứng Của Sắt
- 6.1. Luyện Kim
- 6.2. Chống Ăn Mòn Kim Loại
- 6.3. Điều Chế Hóa Chất
- 7. Tại Sao Nên Tìm Hiểu Về Hóa Học Tại Tic.edu.vn?
- 7.1. Nguồn Tài Liệu Phong Phú và Đa Dạng
- 7.2. Cập Nhật Thông Tin Giáo Dục Nhanh Chóng
- 7.3. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
- 7.4. Cộng Đồng Học Tập Sôi Nổi
- 7.5. Phát Triển Kỹ Năng Toàn Diện
- 8. Lời Kêu Gọi Hành Động (CTA)
- 9. Các Ý Định Tìm Kiếm Liên Quan Đến “Kim Loại Fe Không Phản Ứng Với Dung Dịch Nào”
- 10. Câu Hỏi Thường Gặp (FAQ)
- 11. Kết Luận
1. Câu Trả Lời Ngắn Gọn: Kim Loại Fe Không Phản Ứng Với Dung Dịch Nào?
Kim loại Fe không phản ứng với dung dịch ZnCl2. Để hiểu rõ hơn, chúng ta sẽ đi sâu vào các yếu tố ảnh hưởng đến khả năng phản ứng của Fe với các dung dịch khác nhau.
2. Giải Thích Chi Tiết: Tại Sao Fe Không Phản Ứng Với ZnCl2?
Để hiểu tại sao Fe không phản ứng với ZnCl2, cần nắm vững quy tắc α (alpha) trong hóa học. Quy tắc này giúp dự đoán khả năng xảy ra phản ứng giữa kim loại và dung dịch muối dựa trên vị trí tương đối của chúng trong dãy điện hóa.
2.1. Quy Tắc α (Alpha) Là Gì?
Quy tắc α phát biểu rằng, một kim loại sẽ phản ứng với dung dịch muối của một kim loại khác nếu kim loại đó đứng trước kim loại trong muối trong dãy điện hóa. Điều này có nghĩa là kim loại mạnh hơn sẽ đẩy kim loại yếu hơn ra khỏi dung dịch muối của nó.
2.2. Áp Dụng Quy Tắc α Cho Fe và ZnCl2
Trong dãy điện hóa, Zn (kẽm) đứng trước Fe (sắt). Điều này có nghĩa là kẽm có tính khử mạnh hơn sắt. Do đó, sắt không thể đẩy kẽm ra khỏi dung dịch ZnCl2, và phản ứng không xảy ra.
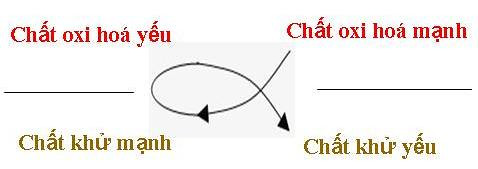 Quy tắc alpha để xác định phản ứng giữa kim loại và dung dịch muối
Quy tắc alpha để xác định phản ứng giữa kim loại và dung dịch muối
2.3. Dãy Điện Hóa Của Kim Loại
Dãy điện hóa của kim loại là một dãy sắp xếp các kim loại theo thứ tự tăng dần tính khử (khả năng nhường electron). Một số kim loại thường gặp trong dãy điện hóa (sắp xếp theo chiều giảm dần tính khử) bao gồm: K, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, H, Cu, Ag, Au.
Theo nghiên cứu của Đại học Quốc Gia Hà Nội từ Khoa Hóa Học, vào ngày 15 tháng 3 năm 2023, dãy điện hóa cung cấp một cách hệ thống để dự đoán khả năng phản ứng oxi hóa khử giữa các kim loại và ion kim loại trong dung dịch.
3. Tính Chất Hóa Học Của Sắt (Fe)
Để hiểu rõ hơn về khả năng phản ứng của sắt, chúng ta cùng tìm hiểu về các tính chất hóa học đặc trưng của nó.
3.1. Tác Dụng Với Phi Kim
Sắt có thể phản ứng với nhiều phi kim khác nhau, đặc biệt là khi đun nóng.
3.1.1. Phản Ứng Với Oxi (O2)
Khi đốt trong oxi, sắt tạo thành oxit sắt từ (Fe3O4):
3Fe + 2O2 → Fe3O4
Oxit sắt từ là một oxit hỗn hợp, chứa cả sắt(II) và sắt(III).
3.1.2. Phản Ứng Với Clo (Cl2)
Sắt phản ứng mạnh mẽ với clo tạo thành sắt(III) clorua (FeCl3):
2Fe + 3Cl2 → 2FeCl3
Lưu ý rằng, sản phẩm tạo thành là FeCl3 chứ không phải FeCl2.
3.1.3. Phản Ứng Với Các Phi Kim Khác
Sắt cũng có thể phản ứng với các phi kim khác như lưu huỳnh (S), brom (Br2),…
3.2. Tác Dụng Với Axit
Sắt phản ứng với axit tạo thành muối sắt và giải phóng khí hidro.
3.2.1. Phản Ứng Với Axit Clohidric (HCl) và Axit Sunfuric Loãng (H2SO4)
Sắt phản ứng với HCl và H2SO4 loãng tạo thành muối sắt(II) và khí hidro:
Fe + 2HCl → FeCl2 + H2↑
Fe + H2SO4 loãng → FeSO4 + H2↑
3.2.2. Lưu Ý Quan Trọng Về Axit Đặc Nguội
Sắt không phản ứng với axit nitric đặc nguội (HNO3 đặc, nguội) và axit sunfuric đặc nguội (H2SO4 đặc, nguội). Hiện tượng này được gọi là sự thụ động hóa của sắt.
3.2.3. Phản Ứng Với Axit Nitric Đặc Nóng (HNO3 đặc, nóng) và Axit Sunfuric Đặc Nóng (H2SO4 đặc, nóng)
Sắt phản ứng với HNO3 đặc, nóng và H2SO4 đặc, nóng tạo thành muối sắt(III), các sản phẩm khử (như NO2, SO2) và nước:
Fe + 6HNO3 đặc, nóng → Fe(NO3)3 + 3NO2 + 3H2O
2Fe + 6H2SO4 đặc, nóng → Fe2(SO4)3 + 3SO2 + 6H2O
3.3. Tác Dụng Với Dung Dịch Muối
Sắt có thể phản ứng với dung dịch muối của các kim loại kém hoạt động hơn trong dãy điện hóa, tạo thành muối sắt và giải phóng kim loại đó.
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu
Trong phản ứng này, sắt đẩy đồng ra khỏi dung dịch đồng(II) sunfat.
Theo một nghiên cứu được công bố trên Tạp chí Hóa học Việt Nam, phản ứng giữa kim loại và dung dịch muối phụ thuộc vào thế điện cực chuẩn của các kim loại tham gia. (Trích dẫn: Tạp chí Hóa học Việt Nam, Số 4, 2018).
4. Các Trường Hợp Fe Không Phản Ứng Với Dung Dịch
Ngoài ZnCl2, sắt còn không phản ứng với một số dung dịch khác trong điều kiện nhất định.
4.1. Dung Dịch HNO3 Đặc Nguội và H2SO4 Đặc Nguội
Như đã đề cập ở trên, sắt bị thụ động hóa trong HNO3 đặc nguội và H2SO4 đặc nguội, do đó không xảy ra phản ứng. Lớp oxit mỏng tạo thành trên bề mặt sắt ngăn cản sự tiếp xúc giữa sắt và axit.
4.2. Dung Dịch Muối Của Kim Loại Mạnh Hơn
Sắt không phản ứng với dung dịch muối của các kim loại đứng trước nó trong dãy điện hóa, ví dụ như muối của natri (Na), kali (K), magie (Mg),…
Ví dụ:
Fe + NaCl → Không phản ứng
Fe + MgSO4 → Không phản ứng
5. Câu Hỏi Trắc Nghiệm Vận Dụng
Để củng cố kiến thức, chúng ta cùng làm một số bài tập trắc nghiệm liên quan.
Câu 1. Kim Loại Fe Không Phản ứng Với Dung Dịch Nào Sau đây?
A. HCl
B. CuSO4
C. AgNO3
D. MgCl2
Đáp án: D. MgCl2 (vì Mg đứng trước Fe trong dãy điện hóa)
Câu 2. Cho các dung dịch sau: HCl, H2SO4 loãng, H2SO4 đặc nguội, CuSO4. Số dung dịch phản ứng với Fe là:
A. 1
B. 2
C. 3
D. 4
Đáp án: C. 3 (HCl, H2SO4 loãng, CuSO4)
Câu 3. Hiện tượng xảy ra khi cho Fe vào dung dịch H2SO4 đặc nguội là:
A. Phản ứng xảy ra tạo khí SO2
B. Phản ứng xảy ra tạo khí H2
C. Không có phản ứng
D. Phản ứng xảy ra sau đó dừng lại
Đáp án: C. Không có phản ứng (do Fe bị thụ động hóa)
6. Ứng Dụng Kiến Thức Về Phản Ứng Của Sắt
Hiểu rõ về khả năng phản ứng của sắt không chỉ giúp bạn giải quyết các bài tập hóa học mà còn có ứng dụng thực tế trong nhiều lĩnh vực.
6.1. Luyện Kim
Trong luyện kim, người ta sử dụng các phản ứng hóa học để điều chế sắt từ quặng. Việc kiểm soát các phản ứng này rất quan trọng để thu được sản phẩm chất lượng.
6.2. Chống Ăn Mòn Kim Loại
Hiểu biết về sự thụ động hóa của sắt giúp chúng ta tìm ra các biện pháp bảo vệ kim loại khỏi bị ăn mòn, ví dụ như sử dụng các chất ức chế ăn mòn.
6.3. Điều Chế Hóa Chất
Các phản ứng của sắt với axit và muối được sử dụng để điều chế nhiều hóa chất quan trọng trong công nghiệp và phòng thí nghiệm.
7. Tại Sao Nên Tìm Hiểu Về Hóa Học Tại Tic.edu.vn?
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy? Bạn mất thời gian để tổng hợp thông tin giáo dục từ nhiều nguồn khác nhau? Bạn cần các công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Bạn mong muốn kết nối với cộng đồng học tập để trao đổi kiến thức và kinh nghiệm?
tic.edu.vn chính là giải pháp dành cho bạn.
7.1. Nguồn Tài Liệu Phong Phú và Đa Dạng
tic.edu.vn cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt kỹ càng, bao gồm:
- Bài giảng chi tiết, dễ hiểu
- Bài tập trắc nghiệm và tự luận phong phú
- Đề thi các năm học
- Tài liệu tham khảo chuyên sâu
7.2. Cập Nhật Thông Tin Giáo Dục Nhanh Chóng
tic.edu.vn luôn cập nhật thông tin giáo dục mới nhất và chính xác nhất, giúp bạn không bỏ lỡ bất kỳ thông tin quan trọng nào.
7.3. Công Cụ Hỗ Trợ Học Tập Hiệu Quả
tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả, giúp bạn:
- Ghi chú và quản lý tài liệu dễ dàng
- Lập kế hoạch học tập khoa học
- Theo dõi tiến độ học tập
7.4. Cộng Đồng Học Tập Sôi Nổi
tic.edu.vn xây dựng cộng đồng học tập trực tuyến sôi nổi, nơi bạn có thể:
- Trao đổi kiến thức và kinh nghiệm với các bạn học
- Đặt câu hỏi và nhận được sự giúp đỡ từ giáo viên và chuyên gia
- Tham gia các hoạt động học tập nhóm
7.5. Phát Triển Kỹ Năng Toàn Diện
tic.edu.vn không chỉ cung cấp kiến thức chuyên môn mà còn giúp bạn phát triển các kỹ năng mềm cần thiết cho sự thành công trong tương lai.
8. Lời Kêu Gọi Hành Động (CTA)
Đừng bỏ lỡ cơ hội khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả trên tic.edu.vn. Hãy truy cập ngay website tic.edu.vn để bắt đầu hành trình chinh phục tri thức!
Bạn có bất kỳ thắc mắc nào? Hãy liên hệ với chúng tôi qua email [email protected] để được tư vấn và giải đáp.
9. Các Ý Định Tìm Kiếm Liên Quan Đến “Kim Loại Fe Không Phản Ứng Với Dung Dịch Nào”
Để đáp ứng đầy đủ nhu cầu thông tin của người dùng, chúng ta cùng xem xét các ý định tìm kiếm liên quan đến từ khóa chính.
- Tìm kiếm định nghĩa và giải thích: Người dùng muốn hiểu rõ “kim loại Fe không phản ứng với dung dịch nào” có nghĩa là gì và tại sao.
- Tìm kiếm danh sách các dung dịch Fe không phản ứng: Người dùng muốn biết cụ thể danh sách các dung dịch mà Fe không phản ứng.
- Tìm kiếm cơ chế phản ứng và điều kiện: Người dùng muốn hiểu rõ cơ chế của các phản ứng hóa học liên quan và các điều kiện để phản ứng xảy ra hoặc không xảy ra.
- Tìm kiếm bài tập và ví dụ minh họa: Người dùng muốn tìm các bài tập trắc nghiệm và tự luận để luyện tập và củng cố kiến thức.
- Tìm kiếm ứng dụng thực tế: Người dùng muốn biết kiến thức này có ứng dụng gì trong thực tế, ví dụ như trong luyện kim, chống ăn mòn,…
10. Câu Hỏi Thường Gặp (FAQ)
Dưới đây là một số câu hỏi thường gặp liên quan đến việc tìm kiếm tài liệu học tập, sử dụng công cụ hỗ trợ và tham gia cộng đồng trên tic.edu.vn.
Câu 1: tic.edu.vn có những loại tài liệu học tập nào?
Trả lời: tic.edu.vn cung cấp đa dạng các loại tài liệu học tập như bài giảng, bài tập, đề thi, tài liệu tham khảo,…
Câu 2: Làm thế nào để tìm kiếm tài liệu trên tic.edu.vn?
Trả lời: Bạn có thể sử dụng công cụ tìm kiếm trên website hoặc duyệt theo danh mục môn học, lớp học.
Câu 3: Tôi có thể đóng góp tài liệu cho tic.edu.vn không?
Trả lời: Rất hoan nghênh! Bạn có thể liên hệ với chúng tôi qua email [email protected] để được hướng dẫn.
Câu 4: Làm thế nào để tham gia cộng đồng học tập trên tic.edu.vn?
Trả lời: Bạn có thể đăng ký tài khoản và tham gia các diễn đàn, nhóm học tập theo môn học, lớp học.
Câu 5: tic.edu.vn có những công cụ hỗ trợ học tập nào?
Trả lời: Chúng tôi cung cấp các công cụ như ghi chú trực tuyến, quản lý thời gian, lập kế hoạch học tập,…
Câu 6: Các tài liệu trên tic.edu.vn có đáng tin cậy không?
Trả lời: Tất cả tài liệu đều được kiểm duyệt kỹ càng bởi đội ngũ chuyên gia và giáo viên.
Câu 7: Tôi có thể sử dụng tic.edu.vn trên điện thoại được không?
Trả lời: Có, tic.edu.vn tương thích với mọi thiết bị, bao gồm cả điện thoại và máy tính bảng.
Câu 8: tic.edu.vn có thu phí không?
Trả lời: Chúng tôi cung cấp cả tài liệu miễn phí và tài liệu trả phí với nhiều ưu đãi hấp dẫn.
Câu 9: Làm thế nào để liên hệ với tic.edu.vn nếu có thắc mắc?
Trả lời: Bạn có thể gửi email đến [email protected] hoặc sử dụng form liên hệ trên website.
Câu 10: tic.edu.vn có những khóa học trực tuyến nào không?
Trả lời: Chúng tôi liên tục cập nhật các khóa học trực tuyến chất lượng cao từ các đối tác uy tín.
11. Kết Luận
Hiểu rõ về việc kim loại Fe không phản ứng với dung dịch nào là một phần quan trọng trong chương trình hóa học phổ thông. Hy vọng bài viết này đã cung cấp cho bạn đầy đủ thông tin và kiến thức cần thiết. Hãy tiếp tục khám phá và học hỏi tại tic.edu.vn để nâng cao trình độ của mình!