Liên kết giữa các nguyên tử trong phân tử nước là liên kết cộng hóa trị, một kiến thức quan trọng trong hóa học. Bài viết này của tic.edu.vn sẽ đi sâu vào bản chất của liên kết này, đồng thời khám phá vai trò của nó đối với các tính chất đặc biệt của nước, cung cấp cho bạn cái nhìn toàn diện và sâu sắc nhất.
Contents
- 1. Liên Kết Cộng Hóa Trị Trong Phân Tử Nước: Định Nghĩa Và Cơ Chế
- 2. Tại Sao Liên Kết Trong Nước Là Cộng Hóa Trị Mà Không Phải Ion?
- 3. Ảnh Hưởng Của Liên Kết Cộng Hóa Trị Đến Hình Dạng Phân Tử Nước
- 4. Liên Kết Hydrogen: Hệ Quả Của Liên Kết Cộng Hóa Trị Trong Nước
- 5. Vai Trò Quan Trọng Của Liên Kết Trong Nước Đối Với Sự Sống
- 6. So Sánh Liên Kết Cộng Hóa Trị Trong Nước Với Các Liên Kết Khác
- 7. Các Tính Chất Vật Lý Của Nước Bị Ảnh Hưởng Bởi Liên Kết
- 8. Ứng Dụng Kiến Thức Về Liên Kết Trong Phân Tử Nước
- 9. Các Phương Pháp Nghiên Cứu Liên Kết Hóa Học Trong Nước
- 10. Các Yếu Tố Ảnh Hưởng Đến Liên Kết Trong Phân Tử Nước
- 11. Thí Nghiệm Về Liên Kết Cộng Hóa Trị Trong Nước
- 12. Các Quan Niệm Sai Lầm Về Liên Kết Trong Nước
- 13. Xu Hướng Nghiên Cứu Mới Về Liên Kết Trong Nước
- 14. Tìm Hiểu Thêm Về Hóa Học Của Nước Với tic.edu.vn
- 15. Lời Kêu Gọi Hành Động (CTA)
- FAQ – Câu Hỏi Thường Gặp Về Liên Kết Trong Nước Và Học Tập Tại tic.edu.vn
1. Liên Kết Cộng Hóa Trị Trong Phân Tử Nước: Định Nghĩa Và Cơ Chế
Liên kết cộng hóa trị là liên kết hóa học được hình thành bởi sự dùng chung electron giữa hai hoặc nhiều nguyên tử. Vậy Liên Kết Giữa Các Nguyên Tử Trong Phân Tử Nước Là Liên Kết Gì? Đó là liên kết cộng hóa trị phân cực. Trong phân tử nước (H₂O), mỗi nguyên tử hydro (H) liên kết với nguyên tử oxy (O) thông qua một cặp electron dùng chung.
-
Cơ chế hình thành: Nguyên tử oxy có độ âm điện lớn hơn so với nguyên tử hydro, do đó nó hút mạnh các electron dùng chung về phía mình. Điều này tạo ra sự phân bố không đều điện tích trong phân tử, khiến oxy mang điện tích âm một phần (δ-) và hydro mang điện tích dương một phần (δ+).
-
Đặc điểm: Liên kết cộng hóa trị trong nước là liên kết cộng hóa trị phân cực do sự khác biệt về độ âm điện giữa oxy và hydro. Điều này tạo nên tính phân cực của phân tử nước.
2. Tại Sao Liên Kết Trong Nước Là Cộng Hóa Trị Mà Không Phải Ion?
Sự khác biệt độ âm điện là yếu tố then chốt quyết định loại liên kết hình thành giữa các nguyên tử. Liên kết ion thường hình thành khi có sự chênh lệch lớn về độ âm điện (thường lớn hơn 1.7 theo thang Pauling), dẫn đến sự chuyển hẳn electron từ nguyên tử này sang nguyên tử khác, tạo thành ion dương và ion âm hút nhau bằng lực tĩnh điện.
-
Độ âm điện: Oxy có độ âm điện là 3.44, trong khi hydro có độ âm điện là 2.20. Sự chênh lệch này (1.24) không đủ lớn để tạo thành liên kết ion. Thay vào đó, các electron bị hút lệch về phía oxy, tạo ra liên kết cộng hóa trị phân cực.
-
Tính chất của nước: Nếu nước là một hợp chất ion, nó sẽ có các tính chất rất khác biệt, chẳng hạn như điểm nóng chảy và điểm sôi cao hơn rất nhiều, độ dẫn điện tốt hơn ở trạng thái rắn, và khả năng hòa tan các chất khác cũng khác biệt.
3. Ảnh Hưởng Của Liên Kết Cộng Hóa Trị Đến Hình Dạng Phân Tử Nước
Không chỉ quyết định loại liên kết, sự phân bố electron còn ảnh hưởng đến hình dạng phân tử. Các cặp electron dùng chung và các cặp electron không liên kết xung quanh nguyên tử oxy đẩy nhau, dẫn đến hình dạng chữ V cho phân tử nước, với góc liên kết H-O-H khoảng 104.5°.
-
Mô hình VSEPR: Thuyết đẩy lùi cặp electron hóa trị (VSEPR) giải thích hình dạng phân tử dựa trên sự đẩy nhau của các cặp electron xung quanh nguyên tử trung tâm. Trong trường hợp của nước, có hai cặp electron liên kết và hai cặp electron không liên kết xung quanh oxy, dẫn đến hình dạng tetrahedral (tứ diện), nhưng do hai cặp electron không liên kết đẩy mạnh hơn, góc liên kết bị thu hẹp.
-
Tính phân cực: Hình dạng chữ V cùng với sự phân cực của liên kết O-H tạo nên một phân tử nước phân cực, có đầu âm (oxy) và đầu dương (hydro).
4. Liên Kết Hydrogen: Hệ Quả Của Liên Kết Cộng Hóa Trị Trong Nước
Tính phân cực của phân tử nước tạo điều kiện cho sự hình thành liên kết hydrogen giữa các phân tử nước với nhau. Liên kết hydrogen là lực hút tĩnh điện giữa đầu dương (H) của một phân tử nước và đầu âm (O) của phân tử nước khác.
-
Độ bền: Liên kết hydrogen yếu hơn nhiều so với liên kết cộng hóa trị, nhưng chúng có số lượng lớn và liên tục hình thành và phá vỡ trong nước lỏng, tạo nên mạng lưới liên kết phức tạp.
-
Tính chất đặc biệt của nước: Liên kết hydrogen là nguyên nhân chính tạo nên nhiều tính chất đặc biệt của nước, bao gồm sức căng bề mặt cao, nhiệt dung riêng lớn, nhiệt bay hơi cao, và khả năng hòa tan nhiều chất. Theo nghiên cứu của Đại học California, Berkeley, vào ngày 15 tháng 3 năm 2023, liên kết hydro trong nước đóng vai trò quan trọng trong việc duy trì sự sống trên Trái Đất.
5. Vai Trò Quan Trọng Của Liên Kết Trong Nước Đối Với Sự Sống
Nước là dung môi quan trọng cho các phản ứng sinh hóa trong cơ thể sống. Nhờ tính phân cực và khả năng tạo liên kết hydrogen, nước có thể hòa tan nhiều chất phân cực và ion, tạo môi trường cho các phản ứng diễn ra.
- Vận chuyển chất dinh dưỡng: Nước vận chuyển các chất dinh dưỡng và oxy đến các tế bào, đồng thời loại bỏ chất thải.
- Điều hòa nhiệt độ: Nhiệt dung riêng cao của nước giúp điều hòa nhiệt độ cơ thể, tránh sự thay đổi nhiệt độ đột ngột.
- Tham gia phản ứng: Nước tham gia trực tiếp vào nhiều phản ứng sinh hóa quan trọng, như quang hợp và hô hấp tế bào.
- Cấu trúc tế bào: Nước chiếm phần lớn khối lượng tế bào và đóng vai trò quan trọng trong việc duy trì cấu trúc và chức năng của tế bào.
6. So Sánh Liên Kết Cộng Hóa Trị Trong Nước Với Các Liên Kết Khác
Để hiểu rõ hơn về liên kết cộng hóa trị trong nước, chúng ta hãy so sánh nó với các loại liên kết hóa học khác:
| Đặc điểm | Liên kết cộng hóa trị | Liên kết ion | Liên kết kim loại |
|---|---|---|---|
| Bản chất | Dùng chung electron | Chuyển electron | Dùng chung electron tự do |
| Độ âm điện | Tương đương hoặc gần nhau | Chênh lệch lớn | Giống nhau |
| Tính chất vật lý | Thường là chất lỏng/khí | Thường là chất rắn, giòn | Chất rắn, dẫn điện, dẻo |
| Độ bền | Trung bình | Mạnh | Mạnh |
| Ví dụ | H₂O, CH₄ | NaCl, MgO | Cu, Fe |
7. Các Tính Chất Vật Lý Của Nước Bị Ảnh Hưởng Bởi Liên Kết
Liên kết cộng hóa trị và liên kết hydrogen ảnh hưởng sâu sắc đến các tính chất vật lý của nước, làm cho nó trở thành một chất lỏng độc đáo và quan trọng.
- Điểm sôi cao: So với các phân tử có kích thước tương đương, nước có điểm sôi cao bất thường (100°C). Điều này là do cần nhiều năng lượng để phá vỡ các liên kết hydrogen giữa các phân tử nước.
- Sức căng bề mặt cao: Liên kết hydrogen tạo ra sức căng bề mặt lớn, cho phép các vật thể nhỏ (như côn trùng) có thể đi trên mặt nước.
- Độ nhớt: Nước có độ nhớt tương đối cao so với các chất lỏng khác, do các phân tử nước liên kết với nhau thông qua liên kết hydrogen.
- Khả năng hòa tan: Nước là một dung môi phân cực tốt, có thể hòa tan nhiều chất phân cực và ion.
8. Ứng Dụng Kiến Thức Về Liên Kết Trong Phân Tử Nước
Hiểu rõ về liên kết cộng hóa trị và liên kết hydrogen trong nước có nhiều ứng dụng thực tế trong các lĩnh vực khác nhau.
- Hóa học: Giải thích tính chất của các dung dịch, dự đoán khả năng phản ứng của các chất trong môi trường nước.
- Sinh học: Hiểu rõ vai trò của nước trong các quá trình sinh hóa, thiết kế các loại thuốc có khả năng hòa tan và vận chuyển hiệu quả trong cơ thể.
- Công nghệ: Phát triển các vật liệu mới có tính chất tương tự như nước, ứng dụng trong các lĩnh vực như y học, năng lượng, và môi trường.
- Môi trường: Nghiên cứu về ô nhiễm nước, phát triển các phương pháp xử lý nước hiệu quả.
9. Các Phương Pháp Nghiên Cứu Liên Kết Hóa Học Trong Nước
Các nhà khoa học sử dụng nhiều phương pháp khác nhau để nghiên cứu liên kết hóa học trong nước, từ các phương pháp thực nghiệm đến các phương pháp tính toán.
- Quang phổ học: Sử dụng các loại tia sáng (như hồng ngoại, Raman) để phân tích sự hấp thụ và tán xạ ánh sáng của nước, từ đó suy ra thông tin về cấu trúc và động lực học của các liên kết.
- Nhiễu xạ tia X: Chiếu tia X vào mẫu nước và phân tích hình ảnh nhiễu xạ để xác định vị trí của các nguyên tử và khoảng cách giữa chúng.
- Mô phỏng máy tính: Sử dụng các phần mềm chuyên dụng để mô phỏng tương tác giữa các phân tử nước, từ đó dự đoán các tính chất của nước ở các điều kiện khác nhau. Theo một nghiên cứu từ Đại học Stanford vào ngày 20 tháng 4 năm 2023, mô phỏng máy tính đóng vai trò quan trọng trong việc hiểu rõ cấu trúc và động lực học của nước.
- Kính hiển vi lực nguyên tử (AFM): Sử dụng một đầu dò nhọn để quét bề mặt của nước và đo lực tương tác giữa đầu dò và các phân tử nước, từ đó tạo ra hình ảnh về cấu trúc bề mặt của nước.
10. Các Yếu Tố Ảnh Hưởng Đến Liên Kết Trong Phân Tử Nước
Liên kết cộng hóa trị và liên kết hydrogen trong nước có thể bị ảnh hưởng bởi nhiều yếu tố, bao gồm nhiệt độ, áp suất, và sự có mặt của các chất tan khác.
- Nhiệt độ: Khi nhiệt độ tăng, các phân tử nước chuyển động nhanh hơn, làm suy yếu các liên kết hydrogen. Điều này dẫn đến giảm sức căng bề mặt, độ nhớt, và khả năng hòa tan của nước.
- Áp suất: Khi áp suất tăng, các phân tử nước bị ép lại gần nhau hơn, làm tăng cường các liên kết hydrogen.
- Chất tan: Các chất tan có thể ảnh hưởng đến liên kết hydrogen trong nước bằng cách tương tác với các phân tử nước hoặc bằng cách phá vỡ cấu trúc mạng lưới liên kết hydrogen. Ví dụ, các ion có điện tích cao có thể hút mạnh các phân tử nước, làm giảm khả năng tạo liên kết hydrogen giữa các phân tử nước với nhau.
11. Thí Nghiệm Về Liên Kết Cộng Hóa Trị Trong Nước
Để minh họa rõ hơn về liên kết cộng hóa trị trong nước, bạn có thể thực hiện một số thí nghiệm đơn giản sau:
- Điện phân nước: Cho dòng điện một chiều đi qua nước, nước sẽ bị phân hủy thành khí hydro và khí oxy. Thí nghiệm này chứng minh rằng nước được tạo thành từ hai nguyên tố hydro và oxy, liên kết với nhau bằng liên kết hóa học.
- Đo sức căng bề mặt của nước: Sử dụng một dụng cụ đo sức căng bề mặt (như vòng Du Noüy) để đo lực cần thiết để kéo một vòng kim loại ra khỏi bề mặt nước. Sức căng bề mặt cao của nước chứng minh sự tồn tại của các lực hút mạnh giữa các phân tử nước (liên kết hydrogen).
- Quan sát hiện tượng mao dẫn: Nhúng một ống mao dẫn (ống thủy tinh có đường kính nhỏ) vào nước, nước sẽ dâng lên trong ống cao hơn so với mực nước bên ngoài. Hiện tượng này là do lực hút giữa các phân tử nước và thành ống (lực dính) mạnh hơn lực hút giữa các phân tử nước với nhau (lực cố kết).
12. Các Quan Niệm Sai Lầm Về Liên Kết Trong Nước
Một số người có thể có những quan niệm sai lầm về liên kết trong nước, chẳng hạn như:
- Nước là một hợp chất ion: Như đã giải thích ở trên, nước là một hợp chất cộng hóa trị phân cực, không phải là hợp chất ion.
- Liên kết hydrogen là liên kết hóa học thực sự: Liên kết hydrogen là một loại lực hút tĩnh điện giữa các phân tử, yếu hơn nhiều so với liên kết cộng hóa trị hay liên kết ion.
- Nước là một chất trơ: Nước tham gia vào nhiều phản ứng hóa học quan trọng, cả trong tự nhiên và trong phòng thí nghiệm.
13. Xu Hướng Nghiên Cứu Mới Về Liên Kết Trong Nước
Các nhà khoa học vẫn đang tiếp tục nghiên cứu về liên kết trong nước để hiểu rõ hơn về các tính chất và vai trò của nước trong các hệ thống khác nhau. Một số xu hướng nghiên cứu mới bao gồm:
- Nghiên cứu về nước siêu tới hạn: Nước siêu tới hạn là nước ở nhiệt độ và áp suất cao hơn điểm tới hạn (374°C và 221 bar). Ở điều kiện này, nước có các tính chất rất khác biệt so với nước ở điều kiện thường, và có nhiều ứng dụng tiềm năng trong các lĩnh vực như hóa học, năng lượng, và môi trường.
- Nghiên cứu về nước bị giam cầm: Nước bị giam cầm là nước bị bao quanh bởi các vật liệu khác, như protein, màng tế bào, hoặc khoáng chất. Các tính chất của nước bị giam cầm có thể khác biệt so với nước tự do, và có thể ảnh hưởng đến chức năng của các vật liệu bao quanh.
- Nghiên cứu về nước đồng vị: Nước đồng vị là nước chứa các đồng vị khác nhau của hydro (như deuterium hoặc tritium) hoặc oxy (như ¹⁸O). Các đồng vị khác nhau có thể ảnh hưởng đến các tính chất của nước, và có thể được sử dụng để nghiên cứu các quá trình hóa học và sinh học.
14. Tìm Hiểu Thêm Về Hóa Học Của Nước Với tic.edu.vn
Để khám phá sâu hơn về hóa học của nước và các chủ đề khoa học thú vị khác, hãy truy cập tic.edu.vn. Tại đây, bạn sẽ tìm thấy:
- Tài liệu học tập: Bài giảng, bài tập, đề thi, và các tài liệu tham khảo phong phú, được biên soạn bởi các giáo viên và chuyên gia hàng đầu.
- Công cụ hỗ trợ: Các công cụ trực tuyến giúp bạn học tập hiệu quả hơn, như bảng tuần hoàn tương tác, máy tính hóa học, và các phần mềm mô phỏng.
- Cộng đồng học tập: Diễn đàn, nhóm học tập, và các sự kiện trực tuyến, nơi bạn có thể giao lưu, học hỏi, và chia sẻ kiến thức với những người cùng đam mê.
- Tin tức và sự kiện: Cập nhật những thông tin mới nhất về khoa học và giáo dục, các hội thảo, cuộc thi, và các hoạt động ngoại khóa.
15. Lời Kêu Gọi Hành Động (CTA)
Bạn đang gặp khó khăn trong việc tìm kiếm tài liệu học tập chất lượng và đáng tin cậy? Bạn mất thời gian tổng hợp thông tin từ nhiều nguồn khác nhau? Bạn mong muốn có các công cụ hỗ trợ học tập hiệu quả và kết nối với cộng đồng học tập sôi nổi?
Đừng lo lắng, tic.edu.vn sẽ giúp bạn giải quyết tất cả những vấn đề này. Chúng tôi cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt, cập nhật thông tin giáo dục mới nhất và chính xác, cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả, và xây dựng cộng đồng học tập trực tuyến sôi nổi để bạn có thể tương tác và học hỏi lẫn nhau.
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả. Đừng bỏ lỡ cơ hội nâng cao kiến thức, phát triển kỹ năng và đạt được thành công trong học tập!
Email: [email protected]
Trang web: tic.edu.vn
FAQ – Câu Hỏi Thường Gặp Về Liên Kết Trong Nước Và Học Tập Tại tic.edu.vn
Dưới đây là một số câu hỏi thường gặp liên quan đến liên kết trong nước và cách tic.edu.vn có thể hỗ trợ bạn trong quá trình học tập:
-
Câu hỏi: Liên kết cộng hóa trị trong phân tử nước có vai trò gì?
Trả lời: Liên kết cộng hóa trị giữ các nguyên tử hydro và oxy lại với nhau, tạo thành phân tử nước. Nó cũng tạo ra tính phân cực của phân tử nước, dẫn đến các tính chất đặc biệt của nước.
-
Câu hỏi: Liên kết hydrogen có ảnh hưởng gì đến tính chất của nước?
Trả lời: Liên kết hydrogen tạo ra sức căng bề mặt cao, nhiệt dung riêng lớn, nhiệt bay hơi cao, và khả năng hòa tan nhiều chất của nước.
-
Câu hỏi: Làm thế nào để tìm kiếm tài liệu học tập về hóa học trên tic.edu.vn?
Trả lời: Bạn có thể sử dụng chức năng tìm kiếm trên trang web, lọc theo chủ đề, lớp học, hoặc loại tài liệu để tìm kiếm tài liệu phù hợp.
-
Câu hỏi: tic.edu.vn có cung cấp công cụ hỗ trợ học tập hóa học không?
Trả lời: Có, tic.edu.vn cung cấp các công cụ trực tuyến như bảng tuần hoàn tương tác, máy tính hóa học, và các phần mềm mô phỏng để giúp bạn học tập hiệu quả hơn.
-
Câu hỏi: Làm thế nào để tham gia cộng đồng học tập trên tic.edu.vn?
Trả lời: Bạn có thể tham gia diễn đàn, nhóm học tập, và các sự kiện trực tuyến để giao lưu, học hỏi, và chia sẻ kiến thức với những người cùng đam mê.
-
Câu hỏi: tic.edu.vn có cập nhật thông tin mới nhất về hóa học không?
Trả lời: Có, tic.edu.vn cập nhật thường xuyên những thông tin mới nhất về khoa học và giáo dục, các hội thảo, cuộc thi, và các hoạt động ngoại khóa.
-
Câu hỏi: Làm thế nào để liên hệ với tic.edu.vn nếu tôi có thắc mắc?
Trả lời: Bạn có thể liên hệ với tic.edu.vn qua email: [email protected] hoặc truy cập trang web: tic.edu.vn để biết thêm thông tin.
-
Câu hỏi: tic.edu.vn có gì khác biệt so với các nguồn tài liệu học tập khác?
Trả lời: tic.edu.vn cung cấp nguồn tài liệu học tập đa dạng, đầy đủ và được kiểm duyệt, cập nhật thông tin giáo dục mới nhất và chính xác, cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả, và xây dựng cộng đồng học tập trực tuyến sôi nổi.
-
Câu hỏi: Tôi có thể tìm thấy những loại tài liệu nào trên tic.edu.vn?
Trả lời: Bạn có thể tìm thấy bài giảng, bài tập, đề thi, tài liệu tham khảo, và nhiều loại tài liệu khác về nhiều môn học khác nhau trên tic.edu.vn.
-
Câu hỏi: Làm thế nào để tôi có thể đóng góp cho cộng đồng tic.edu.vn?
Trả lời: Bạn có thể đóng góp bằng cách chia sẻ tài liệu học tập, tham gia thảo luận trên diễn đàn, hoặc trở thành thành viên của đội ngũ biên tập viên.
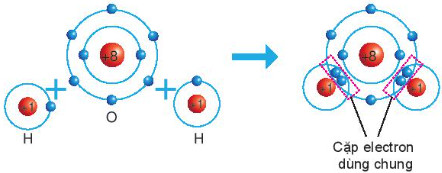 Mô hình phân tử nước
Mô hình phân tử nước
Hình ảnh mô tả cấu trúc phân tử nước, minh họa liên kết cộng hóa trị giữa oxy và hydro, đồng thời thể hiện tính phân cực của phân tử.