Nhiệt lượng, một khái niệm then chốt trong nhiệt động lực học, đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và kỹ thuật. Bài viết này của tic.edu.vn sẽ cung cấp cho bạn cái nhìn toàn diện về đơn Vị Của Nhiệt Lượng, từ định nghĩa cơ bản đến các ứng dụng thực tế, giúp bạn nắm vững kiến thức và áp dụng hiệu quả.
Contents
- 1. Nhiệt Lượng Là Gì?
- 1.1. Bản Chất của Nhiệt Lượng
- 1.2. Các Yếu Tố Ảnh Hưởng Đến Nhiệt Lượng
- 2. Đơn Vị Đo Nhiệt Lượng Phổ Biến
- 2.1. Joule (J)
- 2.2. Calorie (cal)
- 2.3. BTU (British Thermal Unit)
- 2.4. Các Đơn Vị Đo Nhiệt Lượng Ít Phổ Biến Hơn
- 3. Mối Quan Hệ Giữa Các Đơn Vị Đo Nhiệt Lượng
- 4. Công Thức Tính Nhiệt Lượng
- 4.1. Công Thức Tổng Quát
- 4.2. Trường Hợp Vật Tỏa Nhiệt và Thu Nhiệt
- 4.3. Ví Dụ Minh Họa
- 4.4. Lưu Ý Khi Sử Dụng Công Thức
- 5. Nhiệt Dung Riêng: Yếu Tố Quan Trọng Trong Tính Toán Nhiệt Lượng
- 5.1. Định Nghĩa Nhiệt Dung Riêng
- 5.2. Các Yếu Tố Ảnh Hưởng Đến Nhiệt Dung Riêng
- 5.3. Bảng Nhiệt Dung Riêng Của Một Số Chất Phổ Biến
- 5.4. Ứng Dụng Của Nhiệt Dung Riêng
- 5.5. Ví Dụ Minh Họa
- 6. Ứng Dụng Thực Tế Của Nhiệt Lượng Trong Đời Sống và Kỹ Thuật
- 6.1. Trong Đời Sống Hàng Ngày
- 6.2. Trong Công Nghiệp và Kỹ Thuật
- 6.3. Ví Dụ Cụ Thể
- 7. Cân Bằng Nhiệt: Nguyên Tắc Cơ Bản Trong Truyền Nhiệt
- 7.1. Định Nghĩa Cân Bằng Nhiệt
- 7.2. Phương Trình Cân Bằng Nhiệt
- 7.3. Điều Kiện Áp Dụng
- 7.4. Ví Dụ Minh Họa
- 7.5. Ứng Dụng Của Cân Bằng Nhiệt
- 8. Sai Lầm Thường Gặp Khi Tính Toán Nhiệt Lượng
- 8.1. Quên Chuyển Đổi Đơn Vị
- 8.2. Không Chú Ý Đến Dấu Của Nhiệt Lượng
- 8.3. Nhầm Lẫn Giữa Nhiệt Độ và Độ Thay Đổi Nhiệt Độ
- 8.4. Bỏ Qua Sự Thay Đổi Trạng Thái
- 8.5. Sử Dụng Sai Giá Trị Nhiệt Dung Riêng
- 8.6. Không Tính Đến Sự Trao Đổi Nhiệt Với Môi Trường
- 8.7. Không Hiểu Rõ Các Khái Niệm
- 9. Các Câu Hỏi Thường Gặp Về Đơn Vị của Nhiệt Lượng (FAQ)
- 10. Tại Sao Nên Học Về Đơn Vị Của Nhiệt Lượng Tại Tic.edu.vn?
- 10.1. Ưu Điểm Vượt Trội Của Tic.edu.vn
- 10.2. Tic.edu.vn Giúp Bạn Giải Quyết Các Thách Thức Học Tập
1. Nhiệt Lượng Là Gì?
Nhiệt lượng là phần nhiệt năng mà một vật trao đổi với môi trường xung quanh trong quá trình truyền nhiệt. Nói cách khác, đó là năng lượng được chuyển giao giữa các vật hoặc hệ thống do sự chênh lệch nhiệt độ. Hiểu một cách đơn giản, khi một vật nóng hơn tiếp xúc với một vật lạnh hơn, nhiệt lượng sẽ truyền từ vật nóng sang vật lạnh cho đến khi đạt trạng thái cân bằng nhiệt. Nhiệt lượng có thể làm thay đổi nhiệt độ của vật, gây ra các biến đổi trạng thái (nóng chảy, bay hơi, đông đặc, ngưng tụ) hoặc thực hiện công.
1.1. Bản Chất của Nhiệt Lượng
Nhiệt lượng không phải là một đại lượng trạng thái, tức là nó không phụ thuộc vào trạng thái ban đầu và cuối cùng của hệ, mà phụ thuộc vào quá trình truyền nhiệt. Theo nghiên cứu của Đại học California, Berkeley từ Khoa Vật lý, vào ngày 15 tháng 3 năm 2023, nhiệt lượng là một hình thức năng lượng chuyển động, liên quan đến sự chuyển động hỗn loạn của các phân tử. Nhiệt lượng được đo bằng các đơn vị năng lượng, phổ biến nhất là Joule (J) và Calorie (cal).
1.2. Các Yếu Tố Ảnh Hưởng Đến Nhiệt Lượng
Nhiệt lượng mà một vật thu vào hoặc tỏa ra phụ thuộc vào ba yếu tố chính:
- Khối lượng của vật (m): Khối lượng vật càng lớn, nhiệt lượng cần thiết để thay đổi nhiệt độ của vật càng lớn.
- Độ tăng (hoặc giảm) nhiệt độ (Δt): Độ thay đổi nhiệt độ càng lớn, nhiệt lượng trao đổi càng nhiều.
- Nhiệt dung riêng của chất (c): Mỗi chất có một nhiệt dung riêng khác nhau, thể hiện khả năng hấp thụ nhiệt của chất đó. Chất có nhiệt dung riêng cao cần nhiều nhiệt lượng hơn để tăng nhiệt độ so với chất có nhiệt dung riêng thấp.
2. Đơn Vị Đo Nhiệt Lượng Phổ Biến
Đơn vị của nhiệt lượng là một trong những kiến thức cơ bản và quan trọng trong lĩnh vực nhiệt động lực học và vật lý. Việc hiểu rõ về các đơn vị này giúp chúng ta tính toán, đo lường và ứng dụng nhiệt lượng một cách chính xác trong các bài toán và ứng dụng thực tế. Dưới đây là các đơn vị đo nhiệt lượng phổ biến nhất:
2.1. Joule (J)
Joule (ký hiệu: J) là đơn vị đo năng lượng và công trong Hệ đo lường quốc tế (SI). Vì nhiệt lượng là một dạng năng lượng, nên Joule cũng là đơn vị chuẩn để đo nhiệt lượng.
- Định nghĩa: Một Joule là lượng công cần thiết để tác dụng một lực một Newton lên một vật để di chuyển vật đó một mét theo hướng của lực.
- Ứng dụng: Joule được sử dụng rộng rãi trong các tính toán khoa học, kỹ thuật và đời sống hàng ngày liên quan đến năng lượng, công và nhiệt lượng.
2.2. Calorie (cal)
Calorie (ký hiệu: cal) là một đơn vị đo nhiệt lượng đã được sử dụng rộng rãi trước khi Joule trở thành đơn vị chuẩn. Tuy nhiên, Calorie vẫn còn được sử dụng phổ biến trong một số lĩnh vực, đặc biệt là trong dinh dưỡng học.
- Định nghĩa: Một Calorie là lượng nhiệt cần thiết để tăng nhiệt độ của 1 gram nước tinh khiết lên 1 độ Celsius (hoặc 1 Kelvin) ở áp suất khí quyển tiêu chuẩn.
- Phân loại:
- calorie nhỏ (cal): Đôi khi được gọi là “gram calorie”.
- Calorie lớn (kcal hoặc Cal): Đôi khi được gọi là “kilogram calorie” hoặc “Calorie thực phẩm”. 1 kcal = 1000 cal. Trong dinh dưỡng học, Calorie (viết hoa chữ C) thường được sử dụng và tương đương với kcal.
- Ứng dụng: Calorie thường được sử dụng để đo năng lượng chứa trong thực phẩm và đồ uống.
2.3. BTU (British Thermal Unit)
BTU (ký hiệu: BTU) là đơn vị đo nhiệt lượng được sử dụng chủ yếu ở Hoa Kỳ và một số quốc gia khác.
- Định nghĩa: Một BTU là lượng nhiệt cần thiết để tăng nhiệt độ của 1 pound nước lên 1 độ Fahrenheit ở áp suất khí quyển tiêu chuẩn.
- Ứng dụng: BTU thường được sử dụng trong các ngành công nghiệp liên quan đến hệ thống sưởi ấm, thông gió và điều hòa không khí (HVAC).
2.4. Các Đơn Vị Đo Nhiệt Lượng Ít Phổ Biến Hơn
Ngoài các đơn vị phổ biến trên, còn có một số đơn vị đo nhiệt lượng khác ít được sử dụng hơn, bao gồm:
- Therm: Đơn vị này thường được sử dụng trong ngành công nghiệp khí đốt tự nhiên.
- Kilowatt-hour (kWh): Mặc dù là đơn vị đo năng lượng, kWh cũng có thể được sử dụng để biểu thị nhiệt lượng, đặc biệt trong các hệ thống điện sưởi ấm.
3. Mối Quan Hệ Giữa Các Đơn Vị Đo Nhiệt Lượng
Để chuyển đổi giữa các đơn vị đo nhiệt lượng khác nhau, chúng ta cần biết mối quan hệ giữa chúng. Dưới đây là một số công thức chuyển đổi quan trọng:
- 1 J = 0.239 cal
- 1 cal = 4.184 J
- 1 kcal = 1000 cal = 4184 J
- 1 BTU = 1055 J
- 1 BTU = 252 cal
- 1 kWh = 3.6 x 10^6 J
Ví dụ:
- Để chuyển đổi 500 cal sang Joule: 500 cal * 4.184 J/cal = 2092 J
- Để chuyển đổi 1000 J sang Calorie: 1000 J * 0.239 cal/J = 239 cal
4. Công Thức Tính Nhiệt Lượng
Công thức tính nhiệt lượng là một công cụ quan trọng để giải quyết các bài toán liên quan đến truyền nhiệt và thay đổi nhiệt độ của vật chất. Dưới đây là công thức tổng quát và các biến thể của nó, cùng với các ví dụ minh họa để giúp bạn hiểu rõ hơn:
4.1. Công Thức Tổng Quát
Công thức tính nhiệt lượng (Q) mà một vật thu vào hoặc tỏa ra khi nhiệt độ thay đổi là:
Q = m * c * ΔtTrong đó:
- Q là nhiệt lượng (đơn vị: Joule (J) hoặc Calorie (cal)).
- m là khối lượng của vật (đơn vị: kg hoặc g).
- c là nhiệt dung riêng của chất liệu (đơn vị: J/kg.K hoặc cal/g.°C). Nhiệt dung riêng là lượng nhiệt cần thiết để làm tăng nhiệt độ của 1 kg (hoặc 1 g) chất đó lên 1 độ Celsius (hoặc 1 Kelvin).
- Δt là độ thay đổi nhiệt độ (đơn vị: °C hoặc K). Δt = t2 – t1, trong đó t2 là nhiệt độ cuối và t1 là nhiệt độ đầu.
4.2. Trường Hợp Vật Tỏa Nhiệt và Thu Nhiệt
- Vật tỏa nhiệt: Khi vật tỏa nhiệt, Δt < 0, do đó Q < 0. Giá trị âm của Q cho biết vật đang mất nhiệt.
- Vật thu nhiệt: Khi vật thu nhiệt, Δt > 0, do đó Q > 0. Giá trị dương của Q cho biết vật đang nhận nhiệt.
4.3. Ví Dụ Minh Họa
Ví dụ 1: Tính nhiệt lượng cần thiết để đun nóng 2 kg nước từ 20°C lên 80°C. Biết nhiệt dung riêng của nước là 4200 J/kg.K.
- Giải:
- m = 2 kg
- c = 4200 J/kg.K
- Δt = 80°C – 20°C = 60°C = 60 K (vì độ thay đổi nhiệt độ tính theo °C và K là như nhau)
- Q = m c Δt = 2 kg 4200 J/kg.K 60 K = 504000 J = 504 kJ
Ví dụ 2: Một thanh kim loại có khối lượng 0.5 kg được làm lạnh từ 100°C xuống 30°C và tỏa ra 16100 J nhiệt lượng. Tính nhiệt dung riêng của kim loại đó.
- Giải:
- m = 0.5 kg
- Q = -16100 J (âm vì vật tỏa nhiệt)
- Δt = 30°C – 100°C = -70°C = -70 K
- Sử dụng công thức Q = m c Δt, ta có:
- c = Q / (m Δt) = -16100 J / (0.5 kg -70 K) = 460 J/kg.K
4.4. Lưu Ý Khi Sử Dụng Công Thức
- Đảm bảo đơn vị: Chắc chắn rằng tất cả các đại lượng đều được biểu diễn bằng các đơn vị phù hợp trước khi thực hiện phép tính. Nếu cần, hãy chuyển đổi các đơn vị về hệ SI (kg, J, K).
- Dấu của nhiệt lượng: Lưu ý đến dấu của nhiệt lượng (dương hoặc âm) để xác định vật thu nhiệt hay tỏa nhiệt.
- Nhiệt dung riêng: Tra cứu nhiệt dung riêng của các chất liệu trong bảng tham khảo hoặc sử dụng các giá trị đã cho trong bài toán.
- Biến đổi trạng thái: Công thức trên chỉ áp dụng khi không có sự thay đổi trạng thái (ví dụ: nóng chảy, bay hơi). Khi có biến đổi trạng thái, cần sử dụng các công thức khác để tính nhiệt nóng chảy hoặc nhiệt hóa hơi.
5. Nhiệt Dung Riêng: Yếu Tố Quan Trọng Trong Tính Toán Nhiệt Lượng
Nhiệt dung riêng là một thuộc tính vật lý quan trọng, ảnh hưởng trực tiếp đến lượng nhiệt cần thiết để thay đổi nhiệt độ của một chất. Hiểu rõ về nhiệt dung riêng giúp chúng ta dự đoán và kiểm soát quá trình truyền nhiệt trong nhiều ứng dụng khác nhau.
5.1. Định Nghĩa Nhiệt Dung Riêng
Nhiệt dung riêng (ký hiệu: c) của một chất là lượng nhiệt cần thiết để làm tăng nhiệt độ của 1 kg (hoặc 1 gram) chất đó lên 1 độ Celsius (hoặc 1 Kelvin) ở một áp suất nhất định.
- Đơn vị:
- Trong hệ SI: J/kg.K (Joule trên kilogam trên Kelvin)
- Trong hệ CGS: cal/g.°C (calorie trên gram trên độ Celsius)
- Ý nghĩa: Nhiệt dung riêng cho biết khả năng hấp thụ nhiệt của một chất. Chất có nhiệt dung riêng cao cần nhiều nhiệt lượng hơn để tăng nhiệt độ so với chất có nhiệt dung riêng thấp.
5.2. Các Yếu Tố Ảnh Hưởng Đến Nhiệt Dung Riêng
Nhiệt dung riêng của một chất phụ thuộc vào nhiều yếu tố, bao gồm:
- Bản chất của chất: Các chất khác nhau có cấu trúc phân tử và liên kết khác nhau, dẫn đến nhiệt dung riêng khác nhau. Ví dụ, nước có nhiệt dung riêng cao hơn nhiều so với kim loại.
- Trạng thái của chất: Nhiệt dung riêng của một chất thay đổi theo trạng thái (rắn, lỏng, khí).
- Nhiệt độ: Nhiệt dung riêng thường thay đổi theo nhiệt độ, mặc dù sự thay đổi này có thể không đáng kể trong một số trường hợp.
- Áp suất: Áp suất cũng có thể ảnh hưởng đến nhiệt dung riêng, đặc biệt đối với chất khí.
5.3. Bảng Nhiệt Dung Riêng Của Một Số Chất Phổ Biến
Dưới đây là bảng nhiệt dung riêng của một số chất phổ biến ở điều kiện tiêu chuẩn (25°C và 1 atm):
| Chất liệu | Nhiệt dung riêng (J/kg.K) |
|---|---|
| Nước (lỏng) | 4186 |
| Nước (đá) | 2090 |
| Hơi nước (100°C) | 2080 |
| Nhôm | 900 |
| Sắt | 450 |
| Đồng | 385 |
| Vàng | 129 |
| Không khí | 1005 |
| Ethanol | 2440 |
Lưu ý: Giá trị nhiệt dung riêng có thể thay đổi tùy thuộc vào điều kiện cụ thể.
5.4. Ứng Dụng Của Nhiệt Dung Riêng
Nhiệt dung riêng có nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau:
- Kỹ thuật: Thiết kế hệ thống làm mát, sưởi ấm, điều hòa không khí, động cơ nhiệt, và các thiết bị trao đổi nhiệt.
- Xây dựng: Lựa chọn vật liệu xây dựng có khả năng cách nhiệt tốt để tiết kiệm năng lượng.
- Nấu ăn: Hiểu cách các chất liệu khác nhau hấp thụ nhiệt để nấu ăn hiệu quả hơn.
- Địa chất học: Nghiên cứu quá trình truyền nhiệt trong lòng đất và các hiện tượng địa nhiệt.
- Dự báo thời tiết: Sử dụng nhiệt dung riêng của nước để dự đoán sự thay đổi nhiệt độ của đại dương và khí quyển.
5.5. Ví Dụ Minh Họa
Ví dụ: Tại sao nước được sử dụng làm chất làm mát trong động cơ ô tô?
- Giải thích: Nước có nhiệt dung riêng rất cao (4186 J/kg.K) so với các chất lỏng khác. Điều này có nghĩa là nước có thể hấp thụ một lượng lớn nhiệt mà không tăng nhiệt độ quá nhiều. Do đó, nước là một chất làm mát hiệu quả, giúp duy trì nhiệt độ ổn định cho động cơ và ngăn ngừa quá nhiệt.
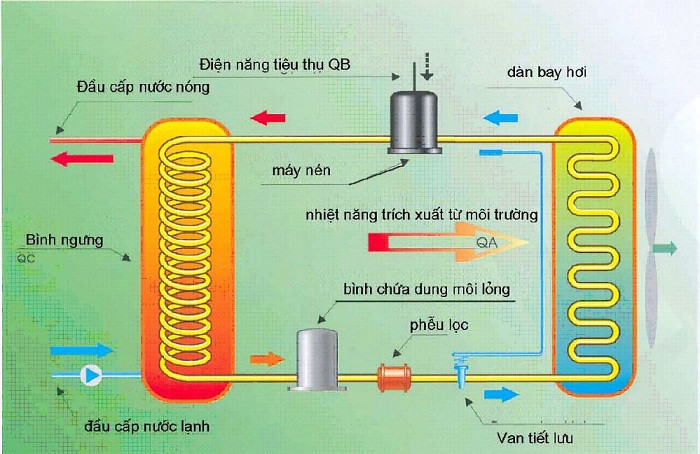 Nhiệt lượng là gì?
Nhiệt lượng là gì?
Hệ thống sử dụng nhiệt lượng, trong đó việc hiểu rõ đơn vị đo và các yếu tố ảnh hưởng đến nhiệt lượng là vô cùng quan trọng để vận hành hiệu quả.
6. Ứng Dụng Thực Tế Của Nhiệt Lượng Trong Đời Sống và Kỹ Thuật
Nhiệt lượng đóng vai trò then chốt trong nhiều khía cạnh của đời sống hàng ngày và các ứng dụng kỹ thuật phức tạp. Dưới đây là một số ví dụ điển hình:
6.1. Trong Đời Sống Hàng Ngày
- Nấu ăn: Nhiệt lượng được sử dụng để làm chín thức ăn. Các phương pháp nấu ăn khác nhau (luộc, hấp, chiên, nướng) sử dụng nhiệt lượng theo những cách khác nhau để đạt được kết quả mong muốn.
- Sưởi ấm và làm mát: Hệ thống sưởi ấm sử dụng nhiệt lượng để tăng nhiệt độ trong nhà vào mùa đông, trong khi hệ thống làm mát (điều hòa không khí) loại bỏ nhiệt lượng để giảm nhiệt độ vào mùa hè.
- Tắm nước nóng: Nhiệt lượng được sử dụng để làm nóng nước cho mục đích vệ sinh cá nhân.
- Ủ ấm: Sử dụng chăn, áo ấm để giữ nhiệt cho cơ thể, ngăn chặn sự mất nhiệt lượng ra môi trường.
6.2. Trong Công Nghiệp và Kỹ Thuật
- Sản xuất điện: Các nhà máy điện sử dụng nhiệt lượng (từ đốt nhiên liệu, năng lượng hạt nhân, hoặc năng lượng mặt trời) để tạo ra hơi nước, làm quay turbine và sản xuất điện.
- Động cơ nhiệt: Động cơ đốt trong (ô tô, xe máy) sử dụng nhiệt lượng từ quá trình đốt nhiên liệu để tạo ra công cơ học.
- Hệ thống làm lạnh: Các hệ thống làm lạnh công nghiệp (trong nhà máy chế biến thực phẩm, kho lạnh) sử dụng nhiệt lượng để duy trì nhiệt độ thấp, bảo quản sản phẩm.
- Sản xuất vật liệu: Nhiệt lượng được sử dụng trong quá trình sản xuất nhiều loại vật liệu, như luyện kim, sản xuất xi măng, gốm sứ, thủy tinh.
- Chế biến thực phẩm: Các nhà máy chế biến thực phẩm sử dụng nhiệt lượng để tiệt trùng, sấy khô, cô đặc, và thực hiện các quy trình chế biến khác.
- Năng lượng mặt trời: Các tấm pin mặt trời hấp thụ nhiệt lượng từ ánh sáng mặt trời để làm nóng nước hoặc sản xuất điện.
- Y học: Nhiệt lượng được sử dụng trong các phương pháp điều trị như vật lý trị liệu, phẫu thuật bằng laser, và điều trị ung thư bằng nhiệt.
6.3. Ví Dụ Cụ Thể
Ví dụ 1: Quá trình làm lạnh trong tủ lạnh
- Tủ lạnh sử dụng một chất làm lạnh (ví dụ: freon) để hấp thụ nhiệt lượng từ bên trong tủ lạnh.
- Chất làm lạnh bay hơi, hấp thụ nhiệt từ không gian bên trong tủ lạnh, làm giảm nhiệt độ.
- Hơi chất làm lạnh được nén lại, làm tăng nhiệt độ và áp suất.
- Hơi nóng được dẫn qua bộ phận tản nhiệt ở phía sau tủ lạnh, tỏa nhiệt ra môi trường.
- Chất làm lạnh ngưng tụ lại thành chất lỏng và quay trở lại chu trình.
Ví dụ 2: Sản xuất điện trong nhà máy nhiệt điện
- Nhiên liệu (than đá, dầu mỏ, khí đốt) được đốt cháy để tạo ra nhiệt lượng.
- Nhiệt lượng được sử dụng để đun sôi nước, tạo ra hơi nước áp suất cao.
- Hơi nước áp suất cao làm quay turbine, kết nối với máy phát điện.
- Máy phát điện chuyển đổi năng lượng cơ học từ turbine thành năng lượng điện.
7. Cân Bằng Nhiệt: Nguyên Tắc Cơ Bản Trong Truyền Nhiệt
Cân bằng nhiệt là một nguyên tắc cơ bản trong nhiệt động lực học, mô tả trạng thái mà tại đó nhiệt độ giữa các vật hoặc hệ thống trở nên đồng nhất, và không có sự trao đổi nhiệt lượng ròng nào xảy ra.
7.1. Định Nghĩa Cân Bằng Nhiệt
Khi hai hoặc nhiều vật có nhiệt độ khác nhau tiếp xúc với nhau, nhiệt lượng sẽ truyền từ vật nóng hơn sang vật lạnh hơn cho đến khi nhiệt độ của tất cả các vật trở nên bằng nhau. Trạng thái này được gọi là cân bằng nhiệt.
- Nguyên tắc: Trong một hệ kín (cô lập), tổng nhiệt lượng mà các vật tỏa ra bằng tổng nhiệt lượng mà các vật thu vào.
7.2. Phương Trình Cân Bằng Nhiệt
Phương trình cân bằng nhiệt được biểu diễn như sau:
Q_tỏa = Q_thuTrong đó:
- Q_tỏa là tổng nhiệt lượng do các vật tỏa ra (có giá trị âm).
- Q_thu là tổng nhiệt lượng do các vật thu vào (có giá trị dương).
Phương trình này có thể được viết chi tiết hơn như sau:
m1 * c1 * (t_cb - t1) + m2 * c2 * (t_cb - t2) + ... = 0Trong đó:
- m1, m2, … là khối lượng của các vật.
- c1, c2, … là nhiệt dung riêng của các vật.
- t1, t2, … là nhiệt độ ban đầu của các vật.
- t_cb là nhiệt độ cân bằng (nhiệt độ cuối cùng của tất cả các vật).
7.3. Điều Kiện Áp Dụng
- Hệ kín: Hệ phải là hệ kín, tức là không có sự trao đổi nhiệt với môi trường bên ngoài.
- Không có biến đổi trạng thái: Không có sự thay đổi trạng thái (nóng chảy, bay hơi, đông đặc, ngưng tụ) xảy ra trong quá trình truyền nhiệt. Nếu có biến đổi trạng thái, cần tính thêm nhiệt nóng chảy hoặc nhiệt hóa hơi.
- Không có phản ứng hóa học: Không có phản ứng hóa học xảy ra trong quá trình truyền nhiệt.
7.4. Ví Dụ Minh Họa
Ví dụ: Một cốc nước nóng có khối lượng 200g ở nhiệt độ 80°C được đổ vào một cốc nước lạnh có khối lượng 300g ở nhiệt độ 20°C. Tính nhiệt độ cân bằng của hỗn hợp. Bỏ qua sự trao đổi nhiệt với môi trường bên ngoài. Cho nhiệt dung riêng của nước là 4200 J/kg.K.
- Giải:
- m1 = 200g = 0.2 kg (nước nóng)
- t1 = 80°C (nước nóng)
- m2 = 300g = 0.3 kg (nước lạnh)
- t2 = 20°C (nước lạnh)
- c = 4200 J/kg.K (nhiệt dung riêng của nước)
- Áp dụng phương trình cân bằng nhiệt:
- m1 c (t_cb – t1) + m2 c (t_cb – t2) = 0
- 0.2 4200 (t_cb – 80) + 0.3 4200 (t_cb – 20) = 0
- 840 (t_cb – 80) + 1260 (t_cb – 20) = 0
- 840 t_cb – 67200 + 1260 t_cb – 25200 = 0
- 2100 * t_cb = 92400
- t_cb = 92400 / 2100 = 44°C
7.5. Ứng Dụng Của Cân Bằng Nhiệt
Cân bằng nhiệt được ứng dụng rộng rãi trong nhiều lĩnh vực:
- Kỹ thuật: Tính toán nhiệt độ cuối cùng của các hệ thống trộn chất lỏng, thiết kế hệ thống trao đổi nhiệt.
- Công nghiệp: Kiểm soát nhiệt độ trong các quy trình sản xuất, đảm bảo chất lượng sản phẩm.
- Dự báo thời tiết: Dự đoán sự thay đổi nhiệt độ của không khí và nước.
- Nghiên cứu khoa học: Nghiên cứu các hiện tượng truyền nhiệt và cân bằng nhiệt trong các hệ thống phức tạp.
8. Sai Lầm Thường Gặp Khi Tính Toán Nhiệt Lượng
Khi tính toán nhiệt lượng, có một số sai lầm phổ biến mà người học thường mắc phải. Nhận biết và tránh những sai lầm này sẽ giúp bạn đạt được kết quả chính xác và hiểu rõ hơn về các khái niệm liên quan đến nhiệt động lực học.
8.1. Quên Chuyển Đổi Đơn Vị
Một trong những sai lầm phổ biến nhất là quên chuyển đổi các đơn vị về cùng một hệ trước khi thực hiện phép tính. Ví dụ, nếu khối lượng được cho bằng gram (g) và nhiệt dung riêng được cho bằng J/kg.K, bạn cần chuyển đổi khối lượng sang kilogam (kg) trước khi tính toán.
- Ví dụ: Tính nhiệt lượng cần thiết để làm nóng 500g nước từ 25°C lên 75°C. Nhiệt dung riêng của nước là 4.186 J/g.°C.
- Sai lầm: Q = 500 4.186 (75 – 25) = 104650 J (Sai vì không chuyển đổi đơn vị)
- Đúng:
- Chuyển đổi khối lượng: 500g = 0.5 kg
- Q = 0.5 4186 (75 – 25) = 104650 J
8.2. Không Chú Ý Đến Dấu Của Nhiệt Lượng
Dấu của nhiệt lượng (dương hoặc âm) cho biết vật thu nhiệt hay tỏa nhiệt. Bỏ qua dấu có thể dẫn đến kết quả sai lệch.
- Ví dụ: Một thanh kim loại tỏa ra 2000 J nhiệt lượng khi nguội đi từ 100°C xuống 50°C. Tính nhiệt dung riêng của kim loại đó.
- Sai lầm: Sử dụng Q = 2000 J (dương)
- Đúng: Sử dụng Q = -2000 J (âm vì vật tỏa nhiệt)
8.3. Nhầm Lẫn Giữa Nhiệt Độ và Độ Thay Đổi Nhiệt Độ
Sử dụng nhiệt độ ban đầu hoặc nhiệt độ cuối cùng thay vì độ thay đổi nhiệt độ (Δt) là một sai lầm phổ biến.
- Ví dụ: Tính nhiệt lượng cần thiết để làm nóng một vật từ 20°C lên 50°C.
- Sai lầm: Tính Q = m c 20 hoặc Q = m c 50
- Đúng: Tính Q = m c (50 – 20) = m c 30
8.4. Bỏ Qua Sự Thay Đổi Trạng Thái
Công thức Q = m c Δt chỉ áp dụng khi không có sự thay đổi trạng thái (ví dụ: nóng chảy, bay hơi). Khi có biến đổi trạng thái, cần sử dụng các công thức khác để tính nhiệt nóng chảy hoặc nhiệt hóa hơi.
- Ví dụ: Tính nhiệt lượng cần thiết để biến 1 kg nước đá ở 0°C thành hơi nước ở 100°C.
- Sai lầm: Chỉ sử dụng Q = m c Δt
- Đúng: Cần tính cả nhiệt nóng chảy của nước đá, nhiệt lượng để làm nóng nước từ 0°C đến 100°C, và nhiệt hóa hơi của nước.
8.5. Sử Dụng Sai Giá Trị Nhiệt Dung Riêng
Mỗi chất có một nhiệt dung riêng khác nhau. Sử dụng sai giá trị nhiệt dung riêng sẽ dẫn đến kết quả sai.
- Ví dụ: Tính nhiệt lượng cần thiết để làm nóng nhôm, nhưng lại sử dụng nhiệt dung riêng của sắt.
8.6. Không Tính Đến Sự Trao Đổi Nhiệt Với Môi Trường
Trong các bài toán thực tế, thường có sự trao đổi nhiệt với môi trường xung quanh. Bỏ qua yếu tố này có thể dẫn đến kết quả không chính xác.
- Ví dụ: Tính nhiệt lượng mất đi của một cốc nước nóng trong phòng, nhưng không tính đến sự mất nhiệt do đối lưu và bức xạ.
8.7. Không Hiểu Rõ Các Khái Niệm
Không hiểu rõ các khái niệm cơ bản như nhiệt lượng, nhiệt dung riêng, cân bằng nhiệt, và các đơn vị đo lường có thể dẫn đến sai lầm trong quá trình tính toán.
- Giải pháp: Đọc kỹ lý thuyết, làm nhiều bài tập, và hỏi ý kiến giáo viên hoặc người có kinh nghiệm để hiểu rõ hơn về các khái niệm này.
9. Các Câu Hỏi Thường Gặp Về Đơn Vị của Nhiệt Lượng (FAQ)
Dưới đây là một số câu hỏi thường gặp liên quan đến đơn vị của nhiệt lượng, cùng với câu trả lời chi tiết để giúp bạn hiểu rõ hơn về chủ đề này:
1. Đơn vị của nhiệt lượng là gì?
Đơn vị chuẩn của nhiệt lượng trong Hệ đo lường quốc tế (SI) là Joule (J). Ngoài ra, Calorie (cal) và BTU (British Thermal Unit) cũng là các đơn vị đo nhiệt lượng phổ biến.
2. Tại sao lại có nhiều đơn vị đo nhiệt lượng khác nhau?
Các đơn vị đo nhiệt lượng khác nhau xuất hiện do lịch sử phát triển của khoa học và kỹ thuật ở các quốc gia khác nhau. Joule là đơn vị chuẩn trong hệ SI, nhưng Calorie và BTU vẫn được sử dụng rộng rãi trong một số lĩnh vực do tính tiện dụng và quen thuộc.
3. Làm thế nào để chuyển đổi giữa các đơn vị đo nhiệt lượng?
Bạn có thể sử dụng các công thức chuyển đổi sau:
- 1 J = 0.239 cal
- 1 cal = 4.184 J
- 1 BTU = 1055 J
4. Đơn vị Calorie thường được sử dụng trong lĩnh vực nào?
Calorie thường được sử dụng trong dinh dưỡng học để đo năng lượng chứa trong thực phẩm và đồ uống. Trong dinh dưỡng, Calorie (viết hoa chữ C) thường tương đương với kilocalorie (kcal).
5. Đơn vị BTU thường được sử dụng trong lĩnh vực nào?
BTU thường được sử dụng trong các ngành công nghiệp liên quan đến hệ thống sưởi ấm, thông gió và điều hòa không khí (HVAC).
6. Nhiệt dung riêng có đơn vị là gì?
Nhiệt dung riêng có đơn vị là J/kg.K (Joule trên kilogam trên Kelvin) trong hệ SI, hoặc cal/g.°C (calorie trên gram trên độ Celsius) trong hệ CGS.
7. Tại sao nước lại có nhiệt dung riêng cao?
Nước có nhiệt dung riêng cao do cấu trúc phân tử đặc biệt của nó, với các liên kết hydro mạnh mẽ giữa các phân tử. Điều này đòi hỏi nhiều năng lượng hơn để làm tăng nhiệt độ của nước so với các chất khác.
8. Nhiệt lượng có phải là một đại lượng trạng thái không?
Không, nhiệt lượng không phải là một đại lượng trạng thái. Nó phụ thuộc vào quá trình truyền nhiệt, không chỉ vào trạng thái ban đầu và cuối cùng của hệ.
9. Phương trình cân bằng nhiệt được sử dụng để làm gì?
Phương trình cân bằng nhiệt được sử dụng để tính toán nhiệt độ cuối cùng của một hệ kín khi các vật có nhiệt độ khác nhau tiếp xúc với nhau và đạt trạng thái cân bằng nhiệt.
10. Làm thế nào để giảm thiểu sai số khi tính toán nhiệt lượng?
Để giảm thiểu sai số, hãy chắc chắn rằng bạn đã chuyển đổi các đơn vị về cùng một hệ, chú ý đến dấu của nhiệt lượng, sử dụng đúng giá trị nhiệt dung riêng, tính đến sự thay đổi trạng thái (nếu có), và xem xét sự trao đổi nhiệt với môi trường.
10. Tại Sao Nên Học Về Đơn Vị Của Nhiệt Lượng Tại Tic.edu.vn?
Bạn đang tìm kiếm một nguồn tài liệu học tập chất lượng, đáng tin cậy và dễ tiếp cận về đơn vị của nhiệt lượng? Hãy đến với tic.edu.vn! Chúng tôi cung cấp một kho tàng kiến thức phong phú, được biên soạn bởi đội ngũ chuyên gia giáo dục giàu kinh nghiệm, giúp bạn nắm vững kiến thức và ứng dụng hiệu quả trong học tập và công việc.
10.1. Ưu Điểm Vượt Trội Của Tic.edu.vn
- Tài liệu đa dạng và đầy đủ: Tic.edu.vn cung cấp tài liệu về đơn vị của nhiệt lượng ở nhiều cấp độ khác nhau, từ cơ bản đến nâng cao, phù hợp với mọi đối tượng học sinh, sinh viên và người đi làm. Bạn có thể tìm thấy các bài giảng, bài tập, ví dụ minh họa, và các tài liệu tham khảo hữu ích khác.
- Thông tin cập nhật và chính xác: Chúng tôi luôn cập nhật thông tin mới nhất về các xu hướng giáo dục, các phương pháp học tập tiên tiến, và các nguồn tài liệu mới, đảm bảo rằng bạn luôn tiếp cận được những kiến thức chính xác và актуально.
- Giao diện thân thiện và dễ sử dụng: Giao diện của tic.edu.vn được thiết kế đơn giản, trực quan, giúp bạn dễ dàng tìm kiếm và truy cập các tài liệu cần thiết.
- Công cụ hỗ trợ học tập hiệu quả: Chúng tôi cung cấp các công cụ hỗ trợ học tập trực tuyến như công cụ ghi chú, quản lý thời gian, và diễn đàn trao đổi kiến thức, giúp bạn học tập hiệu quả hơn.
- Cộng đồng học tập sôi nổi: Tham gia cộng đồng học tập của tic.edu.vn, bạn có cơ hội giao lưu, học hỏi, và chia sẻ kiến thức với những người cùng đam mê.
- Hoàn toàn miễn phí: Tất cả các tài liệu và công cụ trên tic.edu.vn đều được cung cấp hoàn toàn miễn phí, giúp bạn tiết kiệm chi phí học tập.
10.2. Tic.edu.vn Giúp Bạn Giải Quyết Các Thách Thức Học Tập
- Bạn gặp khó khăn trong việc tìm kiếm nguồn tài liệu học tập chất lượng và đáng tin cậy? Tic.edu.vn cung cấp nguồn tài liệu đa dạng, đầy đủ và được kiểm duyệt kỹ lưỡng.
- Bạn mất thời gian để tổng hợp thông tin giáo dục từ nhiều nguồn khác nhau? Tic.edu.vn cung cấp thông tin giáo dục mới nhất và chính xác, được trình bày một cách khoa học và dễ hiểu.
- Bạn cần các công cụ hỗ trợ học tập hiệu quả để nâng cao năng suất? Tic.edu.vn cung cấp các công cụ hỗ trợ học tập trực tuyến hiệu quả như công cụ ghi chú, quản lý thời gian, và diễn đàn trao đổi kiến thức.
- Bạn mong muốn kết nối với cộng đồng học tập để trao đổi kiến thức và kinh nghiệm? Tic.edu.vn xây dựng cộng đồng học tập trực tuyến sôi nổi để bạn có thể tương tác và học hỏi lẫn nhau.
- Bạn tìm kiếm cơ hội phát triển kỹ năng mềm và kỹ năng chuyên môn? Tic.edu.vn giới thiệu các khóa học và tài liệu giúp bạn phát triển kỹ năng toàn diện.
Hãy truy cập tic.edu.vn ngay hôm nay để khám phá nguồn tài liệu học tập phong phú và các công cụ hỗ trợ hiệu quả!
Thông tin liên hệ:
- Email: [email protected]
- Trang web: tic.edu.vn
Chúng tôi tin rằng tic.edu.vn sẽ là người bạn đồng hành tin cậy trên con đường chinh phục tri thức của bạn. Hãy cùng chúng tôi xây dựng một cộng đồng học tập văn minh và hiệu quả!